Ruim 40% van de patiënten met een (hemato-)oncologische aandoening gebruikt complementaire en alternatieve medicatie naast behandeling met conventionele antikankermiddelen
- Rubriek: Korte bijdrage
- Identificatie: 2023;8:a1773
Kernpunten
- Meer dan 40% van de onderzochte patiënten met een (hemato-)oncologische aandoening gebruikt complementaire en alternatieve medicatie (CAM) naast behandeling met conventionele antikankermiddelen.
- Tenminste 10% van alle beoordeelde CAM heeft een relevante interactie met de antikankertherapie.
- Open communicatie over CAM tussen zorgverleners en patiënten is belangrijk om de veiligheid en effectiviteit van de conventionele behandeling te kunnen waarborgen.
Abstract
Over 40% of the (hemato-) oncology population uses complementary and alternative medications (CAM) while receiving anticancer treatment
Background
The use of complementary and alternative medications (CAM) is popular amongst cancer patients. CAM includes herbs, vitamins, minerals, homeopathy, nutritional supplements and probiotics. Use of CAM may lead to unwanted risks by interacting with anticancer drugs.
Objective
To describe the prevalence and risk of CAM use in an adult Dutch cancer population.
Design and methods
A descriptive, observational study was conducted at Amsterdam UMC, between August 2021 and July 2022. Data regarding the use of CAM was obtained by medication reconciliation reviews with in- and outpatients with cancer, who were receiving systemic anticancer treatment. Acquired data was evaluated by the research team and the risks of interaction were classified into relevant, potential, unknown or no interaction. Ultimately, patient-specific recommendations on the use of CAM were provided.
Results
Of the 100 included patients 73% used CAM during the past year and 41% used CAM actively, while receiving anticancer treatment. The most common CAM were vitamins and multivitamins (both 28%). 10% of CAM were classified as giving a relevant interaction with one or more concurrently used anticancer drugs. No association between age or gender and CAM use was found, while outpatients use significantly more CAM than inpatients (72.7% versus 32.1%; P = 0.001). All patients received a customized advice from the hospital pharmacy about their CAM use.
Conclusion
More than 40% of our oncology patients use CAM while receiving anticancer treatment, leading to unwanted risks. The most used CAM are multivitamins and vitamins. 10% of CAM-therapy interactions were classified as relevant, mostly caused by herbs.
Inleiding
In 2021 werd in Nederland bij 124.000 patiënten kanker gediagnostiseerd [1]. Het grootste deel van deze patiënten maakt gebruik van conventionele antikankertherapie. Daarnaast passen patiënten met een oncologische aandoening met regelmaat complementaire en alternatieve geneeswijzen toe [2]. Onder complementaire en alternatieve medicatie (CAM) vallen onder andere vitaminen, mineralen, fytotherapie, homeopathie, voedingssupplementen en probiotica. Na het krijgen van de kankerdiagnose neemt het gebruik van dit soort middelen toe [2, 3]. Op de website van het College ter Beoordeling van Geneesmiddelen (CBG) worden de tien meest gebruikte kruiden in Nederland benoemd [4]. Bij drie van de tien (kurkuma, knoflook en Sint-Janskruid) wordt beschreven dat zij een interactie hebben met tenminste één oncologisch geneesmiddel en wordt benadrukt dat het van belang is dat zorgverleners op de hoogte zijn van het gebruik van kruidengeneesmiddelen [4]. In de huidige praktijk blijkt dit laatste vaak niet het geval. Dat is zorgelijk want het gebruik van dergelijke middelen naast de conventionele behandeling is niet zonder risico. Veel antikankermiddelen hebben namelijk een smalle therapeutische breedte waardoor interacties kunnen zorgen voor toxiciteit maar ook verminderde werkzaamheid van de therapie. McCune et al. stellen zelfs dat 27% van de patiënten die kruiden of vitaminen gebruiken een klinisch relevante CAM-cytostatica interactie zou hebben [5].
Molassiotis et al. hebben in 2005 onderzoek gedaan naar het gebruik van complementaire en alternatieve geneeswijzen bij kankerpatiënten in 33 Europese landen (exclusief Nederland) [2]. Dit onderzoek liet zien dat 15,2% van de kankerpatiënten kruiden gebruikten, 5,3% medicinale thee, 5,2% vitaminen en mineralen en 3,5% andere dieetsupplementen. Het gebruik van (het soort) CAM wordt sterk beïnvloed door het land waar de patiënt woont [2, 3]. In Nederland is de afgelopen decennia zeer beperkt onderzoek uitgevoerd naar het gebruik van CAM bij volwassen oncologiepatiënten. Van der Zouwe et al. voerden in de periode 1984-1987 een onderzoek uit onder 949 patiënten uit verschillende ziekenhuizen [6]. Hiervan gebruikten 9 patiënten ‘middeltjes en remedies’, 13 patiënten homeopathie, 6 patiënten Iscador-injecties (maretak) en 6 patiënten gebruikten kruiden. Van Dam et al. vroegen in 2002 op de poliklinieken van het Antoni van Leeuwenhoek ziekenhuis eveneens het gebruik van CAM uit. Uit dit onderzoek bleek dat 13% van de ondervraagde patiënten gebruikmaakten van voedingssupplementen, homeopathische en orthomoleculaire middelen [7]. Een iets recenter onderzoek uit Nederland (2012) bij 122 Nederlandse kinderen met kanker toonde aan dat 26,5% ‘over the counter remedies’ gebruikten [8]. Een recent overzicht van het CAM-gebruik binnen de volwassenen oncologische populatie in Nederland is niet beschikbaar.
Het doel van dit onderzoek was het gebruik van CAM en de kans op interacties met de gebruikte antikankermiddelen in kaart te brengen bij patiënten met een (hemato-)oncologische aandoening die daarvoor worden behandeld met systemische antikankermiddelen. Daarnaast is gekeken of er patiëntkarakteristieken zijn die voorspellend zijn voor het gebruik van CAM. Er werd een geïndividualiseerd advies aan de patiënt gegeven ten aanzien van het gebruik van CAM.
Methoden
Studieopzet
Dit prospectieve observationele onderzoek werd uitgevoerd van augustus 2021 tot en met juli 2022 in het Amsterdam UMC, locatie Vrije Universiteit. De Medisch Ethische Toetsingscommissie heeft de studie goedgekeurd (METC nummer 2021.0293).
De onderzoekspopulatie bestond uit klinische en poliklinische patiënten, met een gestelde diagnose van kanker, die op moment van inclusie gingen starten met systemische behandeling met antikankermiddelen of deze reeds gebruikten en die in aanmerking kwamen voor een medicatieverificatiegesprek volgens de lokale protocollen. Onder antikankermiddelen vallen alle geneesmiddelen die onder ATC L01 vallen én geneesmiddelen die worden toegepast in het kader van een (hemato-)oncologische studie. Exclusiecriteria waren een leeftijd < 18 jaar, het niet goed beheersen van de Nederlandse of Engelse taal en een behandeling met antikankermiddelen langer dan drie maanden geleden.
Tijdens het reguliere medicatieverificatiegesprek werd de patiënt gevraagd om deel te nemen aan de studie. Na het tekenen van informed consent werd expliciet en uitgebreid gevraagd naar het gebruik van CAM. Deze uitvraag was gestandaardiseerd. De gesprekken werden gevoerd door apothekersassistenten of apothekers (in opleiding) die een aanvullende training hadden gevolgd over CAM en het inzetten van gesprekstechnieken om hierover op een niet-oordelende wijze met de patiënt te communiceren. De inhoud van deze training was afgestemd met vertegenwoordigers van de patiëntenorganisaties International Brain Tumor Alliance en Digestive Cancers Europe.
Op basis van de verzamelde data werden potentiële interacties tussen CAM en de antikankermiddelen in kaart gebracht, beoordeeld en geclassificeerd door de onderzoeksgroep, bestaande uit (ziekenhuis)apothekers (in opleiding). Interacties werden geclassificeerd als relevante, potentiële (interactie niet uit te sluiten op basis van beperkte literatuur, bijvoorbeeld in-vitro data), onbekende (geen literatuur beschikbaar) of geen interactie. Alle beoordelingen werden gedaan door ten minste drie apothekers (in opleiding). De patiënten ontvingen per email een gepersonaliseerd advies ten aanzien van hun CAM-gebruik.
Dataverzameling en -analyse
Tijdens het medicatieverificatiegesprek werd de volgende informatie verzameld en in het patiëntendossier vastgelegd: gebruik van CAM in het afgelopen jaar en op het moment van gesprek, inclusief soort, merk, dosering, reden van gebruik en manier van gebruik. Demografische gegevens werden uit het elektronisch patiëntendossier Epic gehaald. Alle informatie werd in een beveiligd Excel-document opgeslagen. De data werden geanonimiseerd en geëxporteerd naar Statistical Package for Social Sciences (SPSS version 26). Voor analyse van het CAM-gebruik, het soort CAM dat actief en in het afgelopen jaar werd gebruikt en de kans op interacties per CAM werd beschrijvende statistiek gebruikt. De chi-kwadraattoets werd gebruikt om associatie tussen verschillende patiëntkarakteristieken en CAM-gebruik te onderzoeken. Een P-waarde van ≤ 0,05 werd als statistisch significant beschouwd.
Resultaten
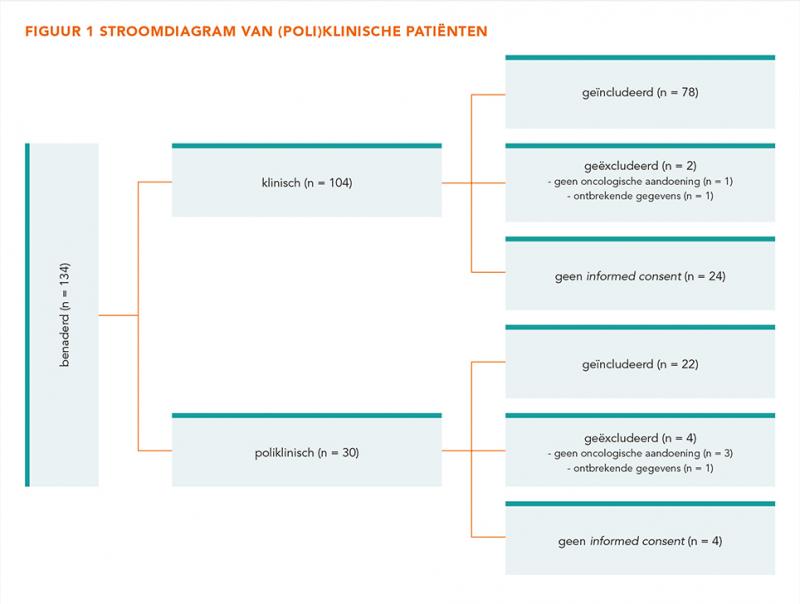
In totaal zijn 134 patiënten benaderd om deel te nemen aan het onderzoek. Hiervan tekende 106 patiënten de informed consent (studierespons: 79,1%) en voldeden 100 patiënten aan de inclusiecriteria (74,6%), zie figuur 1. De patiëntkarakteristieken zijn weergegeven in tabel 1.
CAM-gebruik
Van de 100 patiënten die deelnamen aan de studie gaven 73 patiënten (73%) aan CAM te hebben gebruikt in het afgelopen jaar en 41 patiënten (41%) gebruikten actief CAM op het moment van het medicatieverificatiegesprek. In totaal werden 195 verschillende CAM gerapporteerd die werden gebruikt in het afgelopen jaar en 98 op het moment van gesprek. De patiënten die actief CAM gebruikten, namen per patiënt tussen de 1 en de 8 CAM in met een mediaan van 2. In figuur 2 is de verdeling van de verschillende categorieën van CAM weergegeven van alle genoemde CAM (links) en de actief gebruikte middelen (rechts). De grootste groep was die van de vitaminen (30% en 28%), gevolgd door multivitaminen (24% en 28%). Het meest genoemd werd vitamine D (16x) en multivitaminen (12x).
Interacties
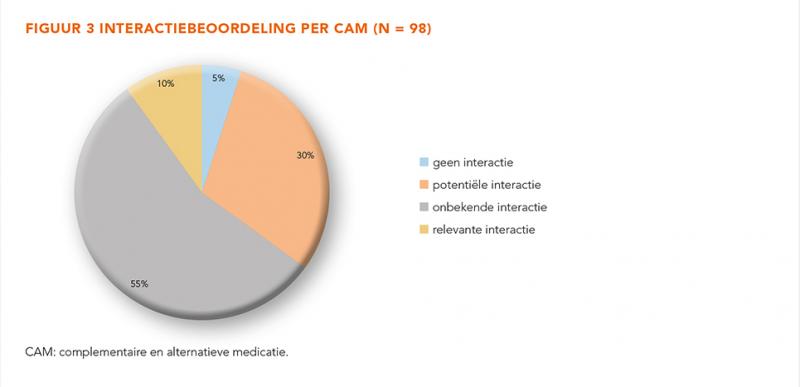
Elke CAM is beoordeeld op de kans op interacties wanneer deze gelijktijdig met de antikankerbehandeling zou worden gebruikt, zie figuur 3. Hieruit kwam dat 10% (n = 10) van de gerapporteerde CAM zou kunnen leiden tot een relevante interactie met één of meer van de antikankermiddelen. Van de 41 patiënten die actief CAM gebruikten en een persoonlijk advies ontvingen, gebruikten 7 patiënten ten minste één CAM met een relevante interactie (17%). Onder deze CAM vielen veelal middelen met hoge doseringen antioxidanten en kruiden die CYP-enzymen beïnvloeden, onder andere kurkuma, groene thee en Ginkgo. Afhankelijk van het schema van de antikankermiddelen werd geadviseerd het middel geheel te staken of deze rondom de kuur niet te gebruiken. Bij een CYP-remmer was het advies om drie dagen voor de kuur te stoppen en bij een CYP-inductor een week voor de kuur. 5% van de CAM (n = 5) werd beoordeeld als geen risico op interactie en 30% (n = 29) zou potentieel voor een interactie kunnen zorgen. Van meer dan de helft van de middelen (55%; n = 54) werd de kans op een interactie als ‘onbekend’ geclassificeerd.
Patiëntkarakteristieken en associatie met CAM-gebruik
De patiëntkarakteristieken van de geïncludeerde patiënten zijn weergegeven in tabel 1. In totaal hebben 68 mannelijke patiënten en 32 vrouwelijke patiënten deelgenomen aan de studie, waarvan 41,2% en 40,6% respectievelijk aangaf actief CAM te gebruiken. De mediane leeftijd van de deelnemers aan de studie was 58,5 jaar (range 18-90 jaar). De meeste patiënten (n = 32) zaten in de leeftijdsgroep van 65-79 jaar en in deze leeftijdscategorie was ook het CAM-gebruik het hoogst (46,9%). Er werd geen significante associatie aangetoond tussen CAM-gebruik en geslacht (P = 0,958) of leeftijd (P = 0,112). In totaal werden 78 klinische en 22 poliklinische patiënten geïncludeerd waarvan 32,1% en 72,7% respectievelijk aangaf actief CAM te gebruiken (P = 0,001). In tabel 1 is bovendien een overzicht weergegeven van de oncologische indicaties. De top 3 meest voorkomende kankersoorten waren hoofd-halskanker, lymfoom en sarcoom.
Beschouwing
Uit dit onderzoek blijkt dat 73% van patiënten met een (hemato-)oncologische aandoening CAM heeft gebruikt in het afgelopen jaar en 41% CAM gebruikt naast de behandeling met antikankermiddelen. Deze getallen liggen hoger dan de prevalentiecijfers van CAM-gebruik die in het verleden in de Nederlandse literatuur zijn beschreven [6, 7]. Het is bekend dat de afgelopen jaren het CAM-gebruik is toegenomen [2]. Echter, doordat de definities van CAM in de literatuur erg verschillen, blijkt vergelijken moeilijk. Dit geldt eveneens voor de verschillende categorieën waarin CAM-soorten worden ingedeeld.
In dit onderzoek gaf 10% van alle CAM een relevante interactie met ten minste één antikankermiddel van de patiënt. Deze relevante interacties werden in 8 van de 10 gevallen veroorzaakt door een preparaat dat kruiden bevat. Kruiden hebben een grote kans op interacties met antikankermiddelen omdat zij regelmatig CYP450-enzymen beïnvloeden en daarnaast vaak een antioxidante werking hebben. Helaas was het voor 55% van de gerapporteerde CAM op basis van de huidige literatuur niet mogelijk om een wetenschappelijk onderbouwd advies te geven ten aanzien van het CAM-gebruik. Dit toont aan dat er nog grote kennishiaten zijn en dat meer onderzoek naar CAM noodzakelijk is. De onderzoekers hebben wel een gepersonaliseerd advies gegeven waarbij de kans op interacties zo veel mogelijk werd uitgesloten, bijvoorbeeld door het geven van een toedieningsinstructie (bijvoorbeeld: niet innemen 2 dagen voor de kuur tot en met 2 dagen daarna). In sommige gevallen (bij de vitaminen en mineralen) was de dosis lager dan de aanbevolen dagelijkse hoeveelheid (ADH) en kon het middel dus veilig worden doorgebruikt. Als vuistregel werd gehanteerd dat gebruik tot 150% van de ADH veilig is. Er werd geen associatie gevonden tussen leeftijd of geslacht en CAM-gebruik. Echter, eerdere onderzoeken vonden dat vrouwen en patiënten van een jongere leeftijd meer CAM gebruiken [2, 3]. Of dit ook voor de Nederlandse populatie geldt zou kunnen worden onderzocht door het huidige onderzoek uit te breiden en over meerdere centra uit te voeren. De onderzochte populatie is mogelijk te klein om dit aan te kunnen tonen.
Poliklinische patiënten (72,7%) gebruiken significant meer CAM dan klinische patiënten (32,1%). Een mogelijke verklaring hiervoor is dat de poliklinische patiënten over het algemeen minder ziek zijn en hun medicatie zonder tussenkomst van een zorgverlener innemen. Opvallend is dat alle poliklinische patiënten een hemato-oncologische aandoening hebben. Dit komt doordat in het Amsterdam UMC ten tijden van het onderzoek alleen hematologische patiënten op de dagbehandeling in aanmerking kwamen voor een medicatieverificatiegesprek en hierdoor zijn er geen poliklinische oncologiepatiënten geïncludeerd. Of er een verschil zit tussen hemato-oncologische en oncologische poliklinische patiënten zou moeten worden onderzocht door poliklinische patiënten met solide tumoren in het onderzoek te includeren. De Europese studie van Molassiotis et al. laat zien dat hematologiepatiënten over het algemeen juist minder geneigd zijn om CAM te gebruiken dan patiënten met veel andere kankersoorten [2]. In dit overzicht is echter gekeken naar alle complementaire en aanvullende geneeswijzen (dus niet alleen medicatie) en waren er geen Nederlandse patiënten geïncludeerd. Van andere patiëntengroepen, zoals borstkankerpatiënten, is bekend dat zij juist méér CAM gebruiken [9]. Om een betere representatie van de gehele oncologische populatie in Nederland en de verschillen tussen verschillende kankersoorten aan te kunnen tonen, is een multicenter onderzoek gewenst. De meest voorkomende kankersoorten in dit onderzoek komen namelijk niet overeen met de algemene top kankersoorten in Nederland. Dit is te verklaren doordat het Amsterdam UMC, locatie VUmc, expertisecentrum is voor hoofd-halskanker en hemato-oncologie.
Patiënten met kanker gebruiken relatief vaak CAM. Het uitvragen van CAM-gebruik is noodzakelijk om adviezen te kunnen geven waarbij de veiligheid en effectiviteit van de conventionele therapie gewaarborgd blijft. Voor zover bekend is dit het eerste onderzoek waarbij CAM-gebruik werd onderzocht met behulp van het voeren van medicatieverificatiegesprekken. De onderzoekers zijn van mening dat dit een geschikte manier is om CAM-gebruik te onderzoeken. De apothekersassistente is een benaderbare zorgverlener waaraan patiënten het gebruik van CAM durven te vertellen en door de gestandaardiseerde en uitgebreide uitvraag werd voorkomen dat patiënten CAM vergeten te benoemen. Patiënten zien namelijk niet alle middelen die zij gebruiken als medicatie en dus als risico. Dit kan een reden zijn waarom de gevonden CAM-prevalentie hoger ligt dan bij andere onderzoeken en dan in de dagelijkse praktijk wordt teruggezien (buiten onderzoeksverband). De kennis van de apotheker over geneesmiddelinteracties is noodzakelijk om een goede risicoafweging te kunnen maken. Het gepersonaliseerde advies dat patiënten ontvingen in onze studie, werd door de patiënten zeer op prijs gesteld.
Conclusie
Dit onderzoek toont aan dat meer dan 40% van de patiënten met een (hemato-)oncologische aandoening CAM gebruikt naast de conventionele behandeling met antikankermiddelen. De meest gebruikte CAM zijn multivitaminen of vitaminen. Bij 10% van de beoordeelde CAM werd een relevante interactie gezien, welke in de meeste gevallen werd veroorzaakt door een kruidenpreparaat.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Integraal Kankercentrum Nederland (IKNL). 124.000 nieuwe kankerpatiënten in 2021 [Internet], 2 februari 2022. https://iknl.nl/nieuws/2022/124-000-nieuwe-kankerpatienten-in-2021#:~:text=In%202021%20werd%20bij%20124.000,aandeel%20ouderen%20in%20de%20bevolking
2. Molassiotis A, Fernández-Ortega P, Pud D, et al. Use of complementary and alternative medicine in cancer patients: a European survey. Ann Oncol. 2005 aPR;16(4):655-63.
3. Kemppainen LM, Kemppainen TT, Reippainen JA, Salmenniemi ST, Vuolanto PH. Use of complementary and alternative medicine in Europe: Health-related and sociodemographic determinants. Scand J Public Health. 2018 Jun;46(4):448-55.
4. College ter Beoordeling van Geneesmiddelen (CBG). Veelgebruikte kruiden [Internet].
https://www.cbg-meb.nl/onderwerpen/medicijninformatie-kruiden/veelgebruikte-kruiden.
5. McCune JS, Hatfield AJ, Blackburn AA, Leith PO, Livingston RB, Ellis GK. Potential of chemotherapy-herb interactions in adult cancer patients. Support Care Cancer. 2004 Jun;12(6):454-62.
6. van der Zouwe N, van Dam FS, Aaronson NK, Hanewald GJ. [Alternative treatments in cancer; extent and background of utilization]. Ned Tijdschr Geneeskd. 1994 Feb;138(6):300-6.
7. van Dam FS, Goudsmit M, Jonker T, Eeltink CJ, Muller MJ. [Less use of alternative treatments by cancer patients in 2002 than in 1999]. Ned Tijdschr Geneeskd. 2003 Sep;147(36):1731-4.
8. Singendonk M, Kaspers GJ, Naafs-Wilstra M, Meeteren AS, Loeffen J, Vlieger A. High prevalence of complementary and alternative medicine use in the Dutch pediatric oncology population: a multicenter survey. Eur J Pediatr. 2013 Jan;172(1):31-7.
9. Lo-Fo-Wong DNN, Ranchor AV, de Haes HCJM, Sprangers MAG, Henselmans I. Complementary and alternative medicine use of women with breast cancer: self-help CAM attracts other women than guided CAM therapies. Patient Educ Couns. 2012 Dec;89(3):529-36.
Referentie
Citeer als: Rombouts MD, Karg RMY, Raddjoe SSP, Crul M. Ruim 40% van de patiënten met een (hemato-)oncologische aandoening gebruikt complementaire en alternatieve medicatie naast behandeling met conventionele antikankermiddelen. Nederlands Platform voor Farmaceutisch Onderzoek. 2023;8:a1773.
DOI
https://www.knmp.nl/resolveuid/5f281555d69a446f9e4350a3d335241bOpen access



Reactie toevoegen