Vancomycine als continue infusie bij obese IC-patiënten: evaluatie van het huidige doseerprotocol (VANCOBESE)
- Rubriek: Korte bijdrage
- Identificatie: 2024;9:a1775
Kernpunten
- Slechts 21,2% van de obese (body mass index [BMI] ≥ 30 kg/m2) intensive care (IC)-patiënten had een adequate vancomycineconcentratie binnen 12-24 uur na start van de behandeling.
- Van de geïncludeerde patiënten werd slechts 41% behandeld conform het huidige doseerprotocol voor vancomycine.
- Patiënten met continue venoveneuze hemofiltratie (CVVH) hadden significant vaker sub- dan supratherapeutische vancomycinespiegels.
Abstract
Vancomycin as continuous infusion in obese ICU patients: evaluation of the current dosing protocol
Background
Vancomycin is frequently used in the intensive care unit (ICU). Inadequate and late vancomycin target attainment may negatively affect outcomes. Obesity and critical illness are both associated with pathophysiological changes, which can lead to altered vancomycin pharmacokinetics and possibly suboptimal exposure. There is a lack of evidence for the optimal vancomycin loading and maintenance dose in obese critically ill patients.
Objective
To evaluate the efficacy of the current vancomycin dosing protocol in achieving early (≤ 24 hours) adequate vancomycin concentrations in adult obese (BMI ≥ 30 kg/m2) ICU patients.
Design
Retrospective observational study, conducted at the ICU of the UMCG.
Methods
Adult obese ICU patients treated with vancomycin continuous infusion were included. Demographic and clinical data were extracted from the hospital’s electronic database. The current vancomycin dosing protocol consists of a single loading dose of 20 mg/kg of total body weight (TBW), followed by a continuous infusion (10, 20 or 30 mg/kg TBW over 24 hours depending on renal function). Vancomycin concentrations were measured routinely within 24 hours after start of treatment, with a target of 20-25 mg/L.
Results
We included 104 patients, 43 patients (41%) were treated according to the protocol. Adequate vancomycin concentrations were obtained in 21.2%, within 12-24 hours after start of treatment. When treated according to the protocol, 30.2% met the target. Patients on continuous veno-venous hemofiltration had significantly more often sub- than supratherapeutic vancomycin concentrations (P-value 0.004).
Conclusion
With the current vancomycin dosing protocol, early adequate vancomycin concentrations are achieved only in a small proportion of adult obese ICU patients.
Inleiding
Vancomycine wordt frequent toegepast op de intensive care (IC) [1]. Obesitas en kritisch ziek zijn, zijn beide geassocieerd met pathofysiologische veranderingen die kunnen leiden tot veranderingen in de farmacokinetiek (PK) van vancomycine en mogelijk een suboptimale blootstelling [2,3]. Het vertraagd bereiken van adequate vancomycineconcentraties kan behandeluitkomsten negatief beïnvloeden [4]. Derhalve wordt bij kritisch zieke patiënten geadviseerd om een eenmalige oplaaddosering op basis van totaal lichaamsgewicht (TBW) te geven, gevolgd door continue infusie op basis van nierfunctie [1]. Toename in TBW is gecorreleerd met een toename in verdelingsvolume (Vd) en klaring (CL) van vancomycine [3]. Aangezien de toename in Vd niet proportioneel is met toename in TBW, wordt voor obese patiënten een maximale oplaaddosering van 3000 mg geadviseerd [1].
Er is gebrek aan bewijs voor de optimale vancomycine oplaad- en onderhoudsdosering toegediend als continue infusie bij obese IC-patiënten. Retrospectief onderzoek toonde aan dat obese IC-patiënten een significant lagere vancomycine onderhoudsdosering per kilogram lichaamsgewicht als continue infusie nodig hadden dan niet-obese IC-patiënten, om de streefspiegel van 20 mg/L te bereiken [5]. Er zijn doseeradviezen opgesteld voor vancomycine als continue infusie bij relatief gezonde obese patiënten zonder verminderde nierfunctie [6], maar deze doseeradviezen kunnen niet zonder meer geëxtrapoleerd worden naar obese IC-patiënten.
Het is essentieel om inzicht te krijgen in de effectiviteit van de huidige doseerprotocollen voor vancomycine, gezien de toename van het aantal obese patiënten en de variabiliteit in PK [7]. Het doel van dit onderzoek is om de effectiviteit van het huidige doseerprotocol voor vancomycine in het vroegtijdig (≤ 24 uur) bereiken van adequate vancomycineconcentraties in volwassen obese IC-patiënten te evalueren.
Methoden
Studieopzet en populatie
Dit retrospectieve observationele onderzoek is uitgevoerd op de IC van het Universitair Medisch Centrum Groningen (UMCG). Volwassen (≥ 18 jaar) obese (BMI ≥ 30 kg/m2) patiënten die in de periode januari 2018 tot januari 2022 werden behandeld met vancomycine werden geïncludeerd. Hierbij moesten de eenmalige oplaaddosering en de onderhoudsdosering als continue infusie zijn gestart op de IC. Ook moest 12-24 uur na start een vancomycinespiegel bepaald zijn. Patiënten die in de voorgaande 72 uur vancomycine hadden ontvangen, werden geëxcludeerd. Demografische en klinische patiëntgegevens werden verzameld uit het elektronisch patiëntdossier.
De Medisch Ethische Toetsingscommissie van het UMCG heeft dit onderzoek als niet-WMO-plichtig bestempeld.
Vancomycine doseerprotocol
Het IC vancomycine doseerprotocol bestaat uit een eenmalige oplaaddosering van 20 mg/kg TBW, gevolgd door een onderhoudsdosering als continue infusie afhankelijk van de glomerulaire filtratiesnelheid (GFR). Bij een GFR < 30 mL/min is de onderhoudsdosering 10 mg/kg/24 uur, bij een GFR 30-50 mL/min is dat 20 mg/kg/24 uur en bij een GFR > 50 mL/min is het 30 mg/kg/24 uur. Bij patiënten met continue venoveneuze hemofiltratie (CVVH) wordt een onderhoudsdosering van 10 mg/kg/24 uur geadviseerd. Vancomycineconcentraties worden 12-24 uur na start van de behandeling bepaald, met een streefwaarde van 20-25 mg/L.
Eindpunten en definities
Het primaire eindpunt was het percentage patiënten met een vancomycineconcentratie van 20-25 mg/L binnen 12-24 uur na start van de behandeling. Secundaire eindpunten waren de tijd tussen start vancomycinebehandeling en eerste spiegelafname, de mate van dosisaanpassing na eerste vancomycineconcentratie, uitgedrukt in % ten opzichte van de initiële onderhoudsdosering vancomycine, en factoren geassocieerd met een inadequate vancomycineconcentratie op moment van eerste spiegelafname.
Conform doseerprotocol was de oplaaddosering vancomycine 20 ± 2 mg/kg en de onderhoudsdosering passend bij CVVH of creatinineklaring op basis van 24-uurs urine (marge ± 10% in mg/kg/24 uur). Indien geen urineverzameling beschikbaar was, werd de nierfunctie geschat met behulp van de Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI)-formule.
Data-analyse
Beschrijvende statistiek werd gebruikt voor alle variabelen. Continue variabelen zijn weergegeven als mediaan met spreiding en categoriale variabelen als frequentie met percentage. Voor alle geïncludeerde patiënten werden de volgende variabelen vergeleken: leeftijd, geslacht, lichaamsgewicht, BMI, serumcreatinine, creatinineklaring op basis van 24-uurs urineverzameling, CVVH, invasieve beademing, gebruik noradrenaline en Acute Physiology and Chronic Health Evaluation (APACHE) IV-score. Continue variabelen werden getoetst met een Kruskall-Wallistoets en categoriale variabelen met een chi-kwadraattoets. Alle statistische toetsen werden tweezijdig uitgevoerd en een P-waarde < 0,05 werd als statistisch significant beschouwd. Post-hoc is gekeken tussen welke categorieën een verschil zit door middel van een Mann-Whitneytoets bij continue variabelen en een chi-kwadraattoets bij categoriale variabelen. Er werd gecorrigeerd voor multiple testing met behulp van de Holm-Bonferroni-methode. Alle berekeningen werden uitgevoerd met IBM Statistics SPSS (versie 28). Er werd een subanalyse uitgevoerd op de patiënten die conform protocol waren behandeld.
Resultaten
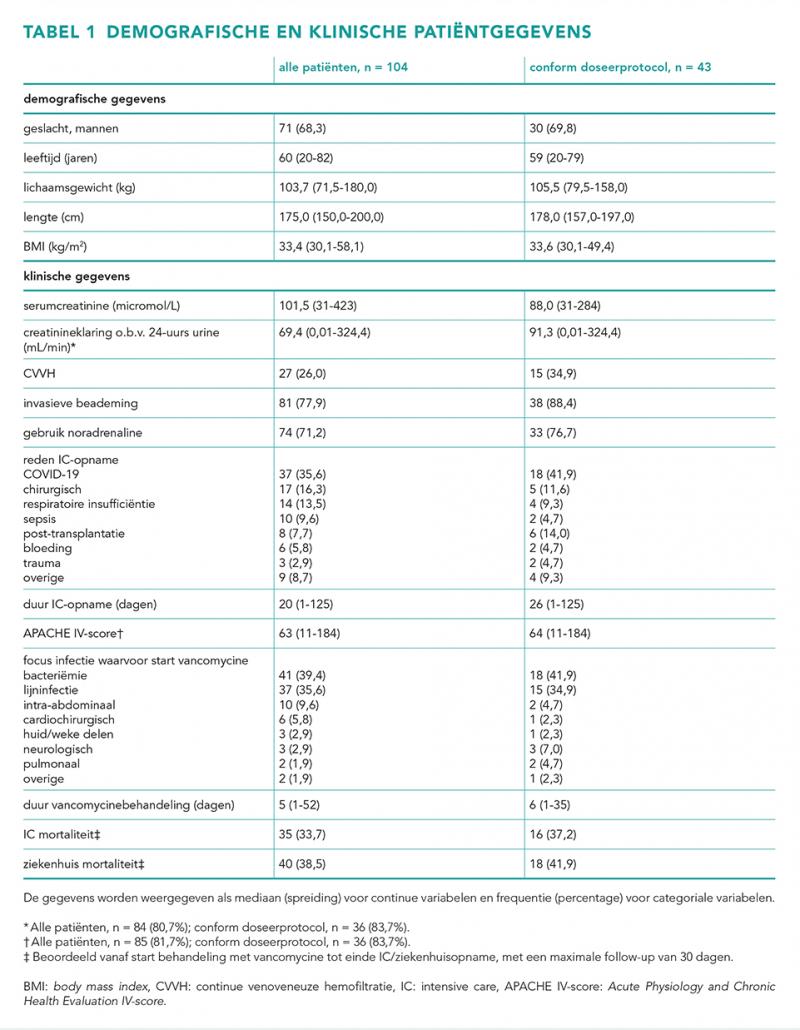
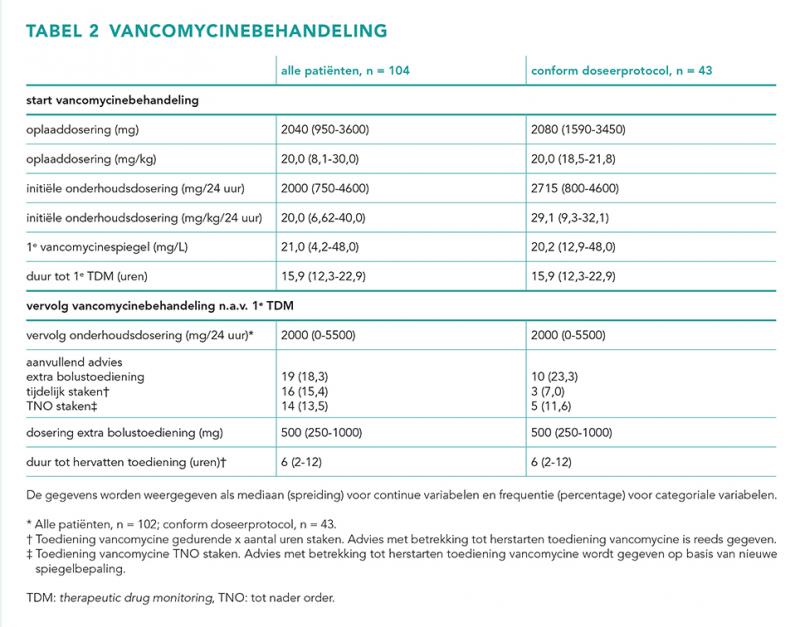
In totaal zijn 104 patiënten geïncludeerd, waarvan 43 (41%) werden behandeld conform het doseerprotocol voor vancomycine. Patiëntkarakteristieken van de totale patiëntengroep en de subgroep die werd behandeld conform protocol zijn weergegeven in tabel 1. Karakteristieken van de vancomycinebehandeling zijn weergeven in tabel 2.
Primaire eindpunt
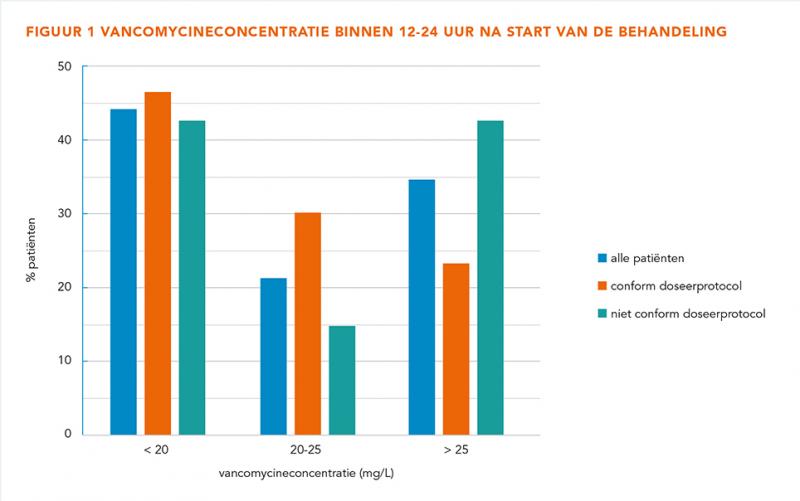
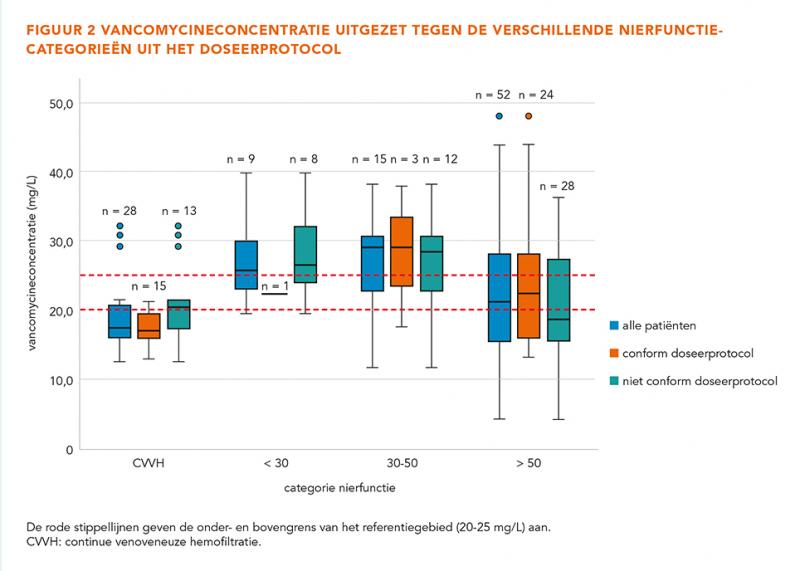
21,2% van de patiënten had een adequate vancomycineconcentratie binnen 12-24 uur na start van de behandeling. In de conform doseerprotocol-groep had 30,2% van de patiënten een adequate spiegel. Er werden zowel veel sub- als supratherapeutische concentraties gevonden, zie figuur 1. In figuur 2 is de vancomycineconcentratie uitgezet tegen de verschillende nierfunctiecategorieën uit het doseerprotocol. Bij CVVH-patiënten werden vooral subtherapeutische concentraties gevonden.
Secundaire eindpunten
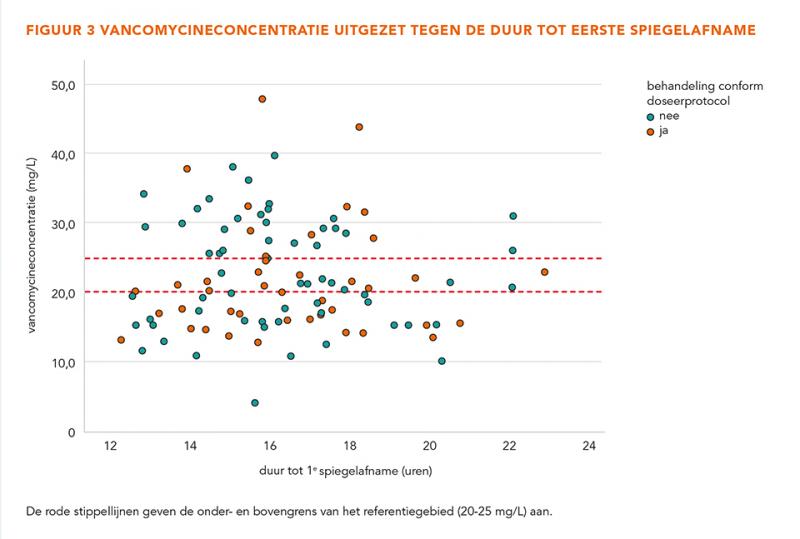
De mediane tijd tussen start van de vancomycinebehandeling en de eerste spiegelafname was 15,9 uur (12,3-22,9). Er werd geen verband gezien tussen moment van spiegelafname en de vancomycineconcentratie (figuur 3). De mediane dosisaanpassing was 0,0% (−100 tot 92,3) ten opzichte van de initiële onderhoudsdosering. De mediane dosisaanpassing in de conform doseerprotocol-groep was 9,9% (−100 tot 92,3). In tabel 2 zijn voor beide groepen de overige adviezen naar aanleiding van de eerste vancomycinespiegel weergegeven.
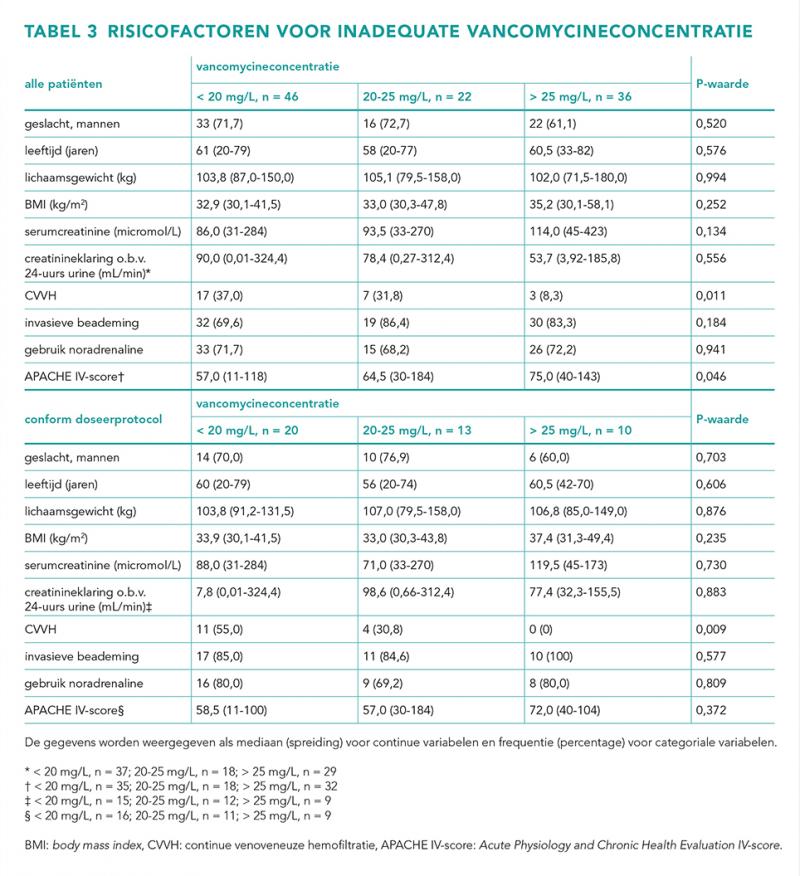
Karakteristieken van patiënten met een adequate, sub- ensupratherapeutische vancomycineconcentratie binnen 12-24 uur na start van de behandeling, zijn weergegeven in tabel 3. Er werden statistisch significante verschillen gevonden in CVVH en mediane APACHE IV-score (alleen voor alle patiënten) tussen de drie groepen. In de post-hoc analyse werd alleen een statistisch significant verschil gevonden voor CVVH; deze patiënten hadden significant vaker een sub- dan een supratherapeutische spiegel (P-waarde 0,004 voor zowel alle patiënten als conform doseerprotocol).
Beschouwing
Dit onderzoek laat zien dat met het huidige doseerprotocol voor vancomycine slechts een klein deel van de volwassen obese IC-patiënten vroegtijdig een adequate vancomycineconcentratie bereikt, waarbij CVVH werd gevonden als risicofactor voor onderbehandeling. Daarnaast bleek slechts 41% van de patiënten daadwerkelijk conform protocol te zijn behandeld.
Het percentage adequate vancomycineconcentraties dat in dit onderzoek werd gevonden is een stuk lager dan de circa 50% die eerder werd gevonden [8,9]. Deze onderzoeken waren echter niet specifiek gericht op obese IC-patiënten en hanteerden een hogere bovengrens van het referentiegebied, namelijk 30 mg/L. Het doseerregime voor vancomycine in beide onderzoeken was redelijk vergelijkbaar met het UMCG-protocol, behalve dat Cristallini et al. een hogere oplaaddosering van 35 mg/kg hanteerden [9]. Dit is ook een hogere oplaaddosering dan wordt geadviseerd bij kritisch zieke en obese patiënten [1].
Uit dit onderzoek blijkt dat CVVH-patiënten significant vaker een sub- dan een supratherapeutische vancomycineconcentratie hadden. Dit sluit aan bij eerder onderzoek bij IC-patiënten met continue dialyse, waarin 24 uur na start van de behandeling 50% een vancomycineconcentratie ≥ 20 mg/L had [10]. In verschillende onderzoeken is, in tegenstelling tot dit onderzoek, een relatie gevonden tussen serumcreatinine en inadequate vancomycineconcentraties [9,11]. Kijkend naar de nierfunctiecategorieën die in het doseerprotocol voor vancomycine worden gehanteerd, hadden patiënten met GFR > 50 mL/min een lagere mediane vancomycineconcentratie dan patiënten in de andere categorieën.
Tegen de verwachting in bleek slechts 41% van de patiënten te zijn behandeld conform protocol. Eerder onderzoek bij IC-patiënten rapporteerde een protocolnaleving van 55,5% [11]. In een Nederlands onderzoek dat ziekenhuisbreed werd uitgevoerd, was voor vancomycine continue infusie de protocolnaleving 30% [12]. In het UMCG zijn in het elektronisch patiëntendossier verschillende voorgedefinieerde medicatieorders aanwezig die aansluiten bij het doseerprotocol voor vancomycine, maar uiteindelijk is het aan de behandelend arts op welke wijze het doseerprotocol wordt toegepast. Hierbij zullen de klinische situatie van de patiënt en de afweging tussen risico op onderbehandeling en/of toxiciteit een rol spelen. Daarnaast kan het lastig zijn om een goede inschatting te maken van de daadwerkelijke nierfunctie van een IC-patiënt. Uit eerder onderzoek in het UMCG bij IC-patiënten blijkt dat creatinineklaring op basis van 24-uurs urine een betere correlatie heeft met de benodigde vancomycinedagdosering dan een schatting op basis van alleen serumcreatinine [13]. Echter, in de praktijk beschikt men op het moment dat vancomycine wordt gestart niet altijd over 24-uurs urineverzameling.
Sterktes van dit onderzoek zijn dat dit het eerste onderzoek is waarin het huidige doseerprotocol voor vancomycine wordt geëvalueerd en dat patiënten die niet exact conform protocol zijn behandeld niet werden geëxcludeerd. Door deze patiënten niet te excluderen is er juist meer inzicht gekregen in de toepassing van het protocol in de praktijk.
Een beperking van dit onderzoek is dat slechts een kleine groep patiënten daadwerkelijk conform protocol werd behandeld, waardoor het moeilijk was om groepen te vergelijken en risicofactoren voor een inadequate vancomycineconcentratie te identificeren. Desondanks werd CVVH gevonden als risicofactor voor onderbehandeling, wat de aanzet is voor vervolgonderzoek naar de optimale startdosering vancomycine bij deze patiënten. Een andere beperking is dat er geen controlegroep is meegenomen, waardoor resultaten niet kunnen worden vergeleken. Als vervolgonderzoek zou het interessant zijn om dit onderzoek te herhalen bij niet-obese IC-patiënten, zodat wel een vergelijking kan plaatsvinden.
Conclusie
Met het huidige doseerprotocol voor vancomycine werd slechts bij een klein deel van de volwassen obese IC-patiënten vroegtijdig een adequate vancomycineconcentratie bereikt. Dit onderzoek laat zien dat optimalisatie van de startdosering vancomycine nodig is, waarbij CVVH werd gevonden als risicofactor voor onderbehandeling.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Rybak MJ, Le J, Lodise TP, et al. Therapeutic monitoring of vancomycin for serious methicillin-resistant Staphylococcus aureus infections: A revised consensus guideline and review by the American Society of Health-System Pharmacists, the Infectious Diseases Society of America, the Pediatric Infectious Diseases Society, and the Society of Infectious Diseases Pharmacists. Am J Health Syst Pharm. 2020 May 19;77(11):835-864.
2. Roberts JA, Lipman J. Pharmacokinetic issues for antibiotics in the critically ill patient. Crit Care Med. 2009 Mar;37(3):840-8 51; quiz 859.
3. Alobaid AS, Hites M, Lipman J, Taccone FS, Roberts JA. Effect of obesity on the pharmacokinetics of antimicrobials in critically ill patients: A structured review. Int J Antimicrob Agents. 2016 Apr;47(4):259-268.
4. Evans L, Rhodes A, Alhazzani W, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2021. Crit Care Med. 2021 Nov;49(11):e1063-e1143.
5. Lin H, Yeh DD, Levine AR. Daily vancomycin dose requirements as a continuous infusion in obese versus non-obese SICU patients. Crit Care. 2016 Jul 1;20(1):205.
6. Smit C, Wasmann RE, Goulooze SC, et al. Population pharmacokinetics of vancomycin in obesity: Finding the optimal dose for (morbidly) obese individuals. Br J Clin Pharmacol. 2020 Feb;86(2):303-317.
7. VZinfo.nl: Trend overgewicht volwassenen [internet]. Rijksinstituut voor Volksgezondheid en Milieu (RIVM): Bilthoven. 2021 Jul 21 [geraadpleegd 2021 Nov 26].
https://www.volksgezondheidenzorg.info/onderwerp/overgewicht/cijfers-context/trends#node-trend-overgewicht-volwassenen
8. Saugel B, Gramm C, Wagner JY, et al. Evaluation of a dosing regimen for continuous vancomycin infusion in critically ill patients: an observational study in intensive care unit patients. J Crit Care. 2014 Jun;29(3):351-355.
9. Cristallini S, Hites M, Kabtouri H, et al. New Regimen for Continuous Infusion of Vancomycin in Critically Ill Patients. Antimicrob Agents Chemother. 2016 Jul 22;60(8):4750-4756.
10. Smeets TJL, Rietveld A, de Geus HRH, Koch BCP, Endeman H, Hunfeld NGM. Vancomycine bij intensivecare-patiënten met continue dialyse. Nederlands Platform voor Farmaceutisch Onderzoek. 2022;7:a1750.
11. De Waele JJ, Danneels I, Depuydt P, Decruyenaere J, Bourgeois M, Hoste E. Factors associated with inadequate early vancomycin levels in critically ill patients treated with continuous infusion. Int J Antimicrob Agents. 2013 May;41(5):434-438.
12. van Gelder TG, Mast L, de Hoogd S, Roescher N, van de Garde EMW. Te lage spiegels na toediening standaarddoses vancomycine. Pharm Weekbl. 2022 feb 4;157(5):12-15.
13. Selles K, Van Der Mast J, Volbeda M, et al. Measured creatinine clearance and its impact on vancomycin levels in critically ill COVID-19 patients. Intensive Care Med Exp. 2020;8(Suppl 2):001506.
Referentie
Citeer als: Schokkin M, Bult W, Brummelhuis-Visser P, Lub-de Hooge MN, Nijsten MWN, Touw DJ. Vancomycine als continue infusie bij obese IC-patiënten: evaluatie van het huidige doseerprotocol (VANCOBESE). Nederlands Platform voor Farmaceutisch Onderzoek. 2024;9:a1775.
DOI
https://www.knmp.nl/resolveuid/45c0e1c290e94383a4288f63b070a175Open access

Reactie toevoegen