Optimale antimicrobiële behandelduur voor een Streptococcus pneumoniae bacteriëmie: 5, 7 of 10 dagen?
- Rubriek: Korte bijdrage
- Identificatie: 2025;10:a1796
Kernpunten
- Bij patiënten met een Streptococcus pneumoniae (S. pneumoniae) bacteriëmie was de mortaliteit onafhankelijk van de behandelduur wanneer deze meer dan vijf dagen was.
- Het merendeel van de patiënten met een S. pneumoniae bacteriëmie die binnen dertig dagen na opname zijn overleden, overleed binnen drie dagen na start van antibiotica.
- Een hoge Pneumonia Severity Index (PSI)-score en een lage body mass index (BMI) waren onafhankelijke voorspellers voor overlijden binnen vijf dagen na start antibiotica.
- In onze regio bleek dat het ziekenhuis van opname en een hoge PSI-score een significante relatie hadden met de behandelduur.
Abstract
Optimal duration of antimicrobial treatment for patients with Streptococcus pneumoniae bacteraemia: 5, 7 or 10 days?
Objective
The primary aim of this study was to determine the optimal duration of antimicrobial treatment in patients with positive blood cultures for Streptococcus pneumoniae (S. pneumoniae) by examining whether mortality was an independent predictor. In addition, it was investigated whether patient characteristics were related to mortality. The secondary objective was to assess whether patient characteristics or other factors had a relation with the antimicrobial treatment duration.
Design
Retrospective observational multicentre study.
Methods
Adult patients with positive blood cultures for S. pneumoniae were included. Exclusion criteria were a documented complicated infection with well-defined requirement for prolonged treatment, polymicrobial bacteraemia, and an unknown treatment duration. Data were extracted from the BACON database. Mortality was defined as death due to any cause within 30 days after hospitalization. Correlation between antimicrobial treatment duration and mortality was analysed by a chisquare test. Multivariable regression models were used to correct the association between antimicrobial treatment duration and mortality for baseline demographic and clinical characteristics.
Results
A total of 692 patients was included in this study. Mortality within 30 days was 11.6% (80/692). Patients treated for 5 days or less showed a significant higher mortality when compared to patients treated for more than 5 days. However, no significant difference in mortality was observed between treatment durations of 7, 10 or 14 days. Also, in multivariable analysis, the treatment duration was not an independent predictor of 30-day mortality, while a lower body mass index (BMI) and a higher Pneumonia Severity Index (PSI) score were. In this cohort, the treatment duration depended strongly on the hospital of admission and the PSI score.
Conclusion
Mortality of patients with a bacteraemic pneumococcal infection was not associated with antimicrobial treatment duration when treated for more than 5 days. Extended antimicrobial treatment beyond 7 days showed no beneficial effect on outcome. Establishing national policies for the treatment duration of S. pneumoniae bacteraemia may further reduce antibiotic use and decrease antibiotic resistance, adverse events, and costs.
Inleiding
Bacteriëmie is wereldwijd een belangrijke oorzaak van mortaliteit en morbiditeit [1,2]. De afgelopen jaren is het aantal bacteriëmieën toegenomen door het toenemende gebruik van immunosuppressieve geneesmiddelen, meer invasieve ingrepen en een vergrijzende bevolking met onderliggende aandoeningen [3]. Een veelvoorkomende verwekker van een bacteriëmie is Streptococcus pneumoniae (S. pneumoniae) [4,5]. Deze bacterie kan leiden tot diverse infecties, variërend van milde, zelflimiterende infecties zoals otitis media en sinusitis tot ernstige invasieve infecties, zoals pneumonie, sepsis, osteomyelitis en meningitis [6]. Jaarlijks worden in Nederland ongeveer 10.000 mensen met een pneumokokkeninfectie opgenomen in het ziekenhuis, met name jonge kinderen en ouderen [6,7].
Bacteriëmieën zijn geassocieerd met een slechte klinische uitkomst, vooral wanneer adequate antimicrobiële therapie en source control uitblijven of vertraagd worden uitgevoerd. Inzet van breedspectrum antibiotica kan in de empirische fase daarom geïndiceerd zijn [8,9]. Om het totale antibioticagebruik te verminderen en daarmee antibioticaresistentie en bijwerkingen te voorkomen, is het zinvol om de inzet van antibiotica te beoordelen. De keuze voor het juiste middel met een smal spectrum en de juiste duur van therapie is noodzakelijk [10]. De Nederlandse Stichting Werkgroep Antibiotica Beleid (SWAB) heeft nationale richtlijnen ontwikkeld voor de behandeling van sepsis en Community Acquired Pneumoniae (CAP), echter ontbreken er richtlijnen voor de behandelduur bij patiënten met pneumokokkensepsis of -bacteriëmie [11-13].
Havey en collega’s publiceerden een onderbouwing voor de groeiende consensus dat CAP veilig kan worden behandeld met een therapieduur van vijf dagen, ongeacht of er sprake was van een bacteriëmie [3].
Het primaire doel van deze studie was om een optimale antimicrobiële behandelduur voor een S. pneumoniae bacteriëmie te bepalen. Derhalve is onderzocht of de duur van de antimicrobiële therapie bij patiënten met een positieve bloedkweek voor S. pneumoniae een onafhankelijke voorspeller is voor mortaliteit. Daarnaast is gekeken of bepaalde patiëntkarakteristieken een risicofactor zijn voor mortaliteit. Secundair is onderzocht of patiëntkarakteristieken van invloed zijn op de antimicrobiële behandelduur.
Methoden
Dit onderzoek betrof een retrospectief, observationeel multicenter onderzoek. Er is gebruik gemaakt van de database van de studie Genomic epistasis of invasive bacteria, ook wel de BACON (Bacteraemia Collection Oost-NL 2012-2020)-studie genoemd. Hiervoor werden tussen 01-01-2012 en 30-06-2020 gegevens verzameld van patiënten met een positieve bloedkweek voor S. pneumoniae, opgenomen in één van de vier deelnemende ziekenhuizen (Canisius Wilhelmina Ziekenhuis [CWZ], Maasziekenhuis Pantein Boxmeer [P], Rijnstate Arnhem [RA] en Radboudumc Nijmegen [RN]). In alle deelnemende ziekenhuizen was toestemming gegeven door de lokale haalbaarheidscommissie voor het uitvoeren van de studie.
Alle patiënten (≥ 18 jaar) met een positieve bloedkweek voor S. pneumoniae kwamen in aanmerking voor inclusie. Exclusiecriteria waren een gedocumenteerde gecompliceerde infectie met een therapieduur van ≥ 10 dagen (zoals empyeem, meningitis, etc.) [13-15], polymicrobiële bacteriëmieën en een onbekende behandelduur. Gegevens van de geïncludeerde patiënten op het moment van opname werden verzameld, waaronder leeftijd, geslacht, lengte, gewicht, comorbiditeit, het ziekenhuis van opname, de mate van ziekte uitgedrukt in de ‘Ademhaling, Mentale toestand, Bloeddruk, Ureum, 65 jaar’ (AMBU-65)-score, de Pneumonia Severity Index (PSI) en de Systemic Inflammatory Response Syndrome (SIRS)-criteria. Andere verzamelde gegevens omvatten behandelduur, mortaliteit, kweekuitslagen en de locatie van infectie.
Voor de primaire uitkomstmaat mortaliteit werden de patiënten onderverdeeld in groepen afhankelijk van de behandelduur in dagen: groep A: ≤ 5 dagen, groep B: 6-8 dagen, groep C: 9-11 dagen en groep D: ≥ 12 dagen, overeenkomend met de regelmatig beschreven standaard behandelduurregimes van 5, 7, 10 of 14 dagen [16]. Mortaliteit werd in deze studie gedefinieerd als overlijden door alle oorzaken binnen dertig dagen na opname. Statistische analyses werden uitgevoerd met IBM SPSS Statistics 25. Een chi-kwadraattoets of Fisher-exacttoets werd gebruikt voor categorische gegevens en de Mann-Whitneytoets en Kruskall-Wallistoets voor continue gegevens. Wanneer er significante verschillen in mortaliteit tussen de groepen werden gevonden, werden patiëntkarakteristieken geanalyseerd met univariabele en multivariabele logistische regressie. Om vast te stellen welke patiëntkenmerken geassocieerd waren met een langere behandelduur werd eveneens een univariabele en multivariabele logistische regressie uitgevoerd. Een P-waarde van < 0,05 werd als significant beschouwd.
Resultaten
De totale BACON-database bevat gegevens van 1065 patiënten, waarvan 692 patiënten zijn geïncludeerd in dit onderzoek. De mediane leeftijd was 69 jaar, 53,2% van de patiënten was man en de mediane body mass index (BMI) was 25,2 (zie tabel 1). De bron van infectie was bij 652 patiënten (94,2%) een pneumonie. Met betrekking tot de ziekte-ernst, had 60,7% een AMBU-65-score van 2 of hoger, 72,1% een PSI-klasse III of hoger en 89,2% had een SIRS-score van 2 of hoger.
De totale sterfte binnen dertig dagen na opname in deze studiepopulatie was 11,6% (80/692). Van de overleden patiënten overleed de meerderheid (56%, 45/80) binnen drie dagen na start van antibiotica.
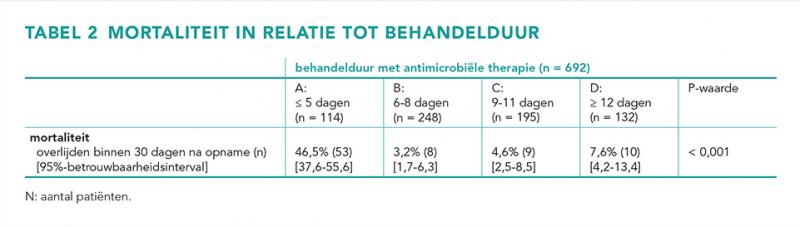
De mortaliteit per behandelduurgroep liet zien dat groep A een significant hogere mortaliteit had van 46,5% (53/114) (P < 0,001). Er was geen significant verschil in mortaliteit tussen de groepen B, C en D (zie tabel 2).
Het risico op overlijden binnen vijf dagen na start van antibiotica was groter bij patiënten met een hogere leeftijd, een lage BMI, hart- en vaatziekten in de voorgeschiedenis, een hogere AMBU-65-score en een hogere PSI-score. Daarnaast was het ziekenhuis van opname significant gerelateerd aan overlijden binnen vijf dagen. Na correctie in een multivariabele logistische regressie waren enkel BMI en PSI-score nog significant verschillend (P = 0,001 en P < 0,001, respectievelijk).
Een aantal patiëntkarakteristieken was geassocieerd met de behandelduur. In de univariabele analyse was een chronisch respiratoire aandoening (P = 0,025) en hart- en vaatziekten (P = 0,039) significant geassocieerd met de behandelduur. Tevens waren de PSI-score (P = 0,001) en het ziekenhuis van opname (P < 0,001) significant verschillend tussen de behandelduurgroepen. Na correctie met een multivariabele logistische regressie waren alleen de PSI-score en het ziekenhuis van opname significant gerelateerd aan de behandelduur (P = 0,001 en P < 0,001, respectievelijk).
De behandelduur per ziekenhuis was verschillend (zie figuur 1). Het CWZ behandelde de meeste patiënten 6-8 dagen (50,7%). RA hanteerde in vergelijking met de andere ziekenhuizen de langste behandelduur: 65,6% van de patiënten (164/250) werd meer dan acht dagen met antibiotica behandeld.
Beschouwing
De mortaliteit bij patiënten met een S. pneumoniae bacteriëmie was onafhankelijk van de duur van de antimicrobiële therapie bij een behandeling van meer dan vijf dagen.
Tussen de behandelgroepen B, C en D was geen significant verschil in mortaliteit en had een behandelduur van langer dan zeven dagen geen gunstiger effect. Ook Havey et al. gaven weer dat bacteriëmieën secundair aan verschillende infectiefocussen, waaronder CAP, succesvol konden worden behandeld met een behandelduur van 5-7 dagen [3].
Een antimicrobiële behandeling van vijf dagen of korter was geassocieerd met een verhoogd risico op sterfte; 46,5% van de patiënten overleed binnen vijf dagen na start van behandeling met antibiotica (groep A). Deze korte behandelduur lijkt echter eerder een gevolg dan een oorzaak van overlijden te zijn. Van de 80 sterftegevallen binnen 30 dagen overleden er zelfs 45 binnen 3 dagen. Ook Balakrishnan et al. beschreven dat 50% van de sterfgevallen in hun studiepopulatie overleed binnen 48 uur na opname [17].
De univariabele analyse liet zien dat deze groep een hogere leeftijd had, een lage BMI, hart- en vaatziekten en de ziekte-ernst uitgedrukt in AMBU-65- en PSI-scores was hoger. Dit impliceert dat de patiënten die kort na opname kwamen te overlijden, vooral erg kwetsbaar waren. Na correctie waren alleen de hogere PSI-score en een lage BMI nog significant. De link tussen een lage BMI en hogere mortaliteit wordt ook wel de ‘obesity survival paradox’ genoemd [18].
De behandelduur was geassocieerd met de PSI-score en het ziekenhuis van opname. Hoe hoger de PSI-score, hoe langer er werd behandeld. Dit zou een weergave kunnen zijn van de praktijk waarbij de behandelend arts op basis van infectieparameters en de klinische staat van de patiënt beoordeelt dat deze een langere behandelduur nodig heeft dan de richtlijnen aangeven. Groep D, met de langste behandelduur (≥ 12 dagen), lijkt in overeenstemming met dit gegeven een kwetsbaardere groep gezien de hogere geobserveerde mortaliteit (7,6%) vergeleken met groep B en C.
De behandelduur per ziekenhuis was verschillend. Een mogelijke verklaring hiervoor is het ontbreken van een Europese of landelijke richtlijn voor het behandelen van een S. pneumoniae bacteriëmie. In studies die de antimicrobiële behandelduur voor patiënten met een bacteriëmie vaststelden, werden patiënten over het algemeen 7-14 dagen behandeld, maar met een grote variatie [13]. De ziekenhuizen RA, RN en P hebben lokale behandelrichtlijnen voor S. pneumoniae bacteriëmie opgesteld. De behandelduur in het RA was ten tijde van de dataverzameling 10 dagen en in RN en P 7-10 dagen [14,15]. Dit is duidelijk terug te zien in figuur 1. CWZ heeft geen lokaal behandelbeleid en de behandelduur was daar nadrukkelijk korter, zonder verschil in mortaliteit.
In deze studiepopulatie komt de totale sterfte binnen 30 dagen van 11,6% overeen met het mortaliteitspercentage van 10-30% dat in de literatuur is beschreven [19,20]. De resultaten van deze studie zijn dus representatief en een antimicrobiële behandelduur van zeven dagen volstaat voor patiënten met een S. pneumoniae bacteriëmie met voornamelijk een longfocus. Patiënten met een gecompliceerde infectie zoals onder andere een meningitis of een empyeem waren geëxcludeerd in deze studie. Een sterk punt van deze studie is het grote ‘real life’-cohort dat is bestudeerd met een populatie van 692 patiënten opgenomen in 4 verschillende ziekenhuizen in Nederland, zowel perifeer als academisch.
Een grote beperking van deze studie is het retrospectieve karakter en de insteek van de gebruikte BACON-database. Het ontbreken van de initiële geplande behandelduur is een limitatie, aangezien dit van invloed kan zijn geweest op de verdeling in behandelduurgroepen. Daarnaast is het type antibioticum en de dosering niet meegenomen in de analyse en kan er geen uitspraak worden gedaan over de klinische genezing van de infectie. Het ontbreken van de gebruikte antibiotica is echter geen belemmering voor de associaties met behandelduur, aangezien de S. pneumoniae in Nederland goed gevoelig is voor alle gebruikte antibiotica [21].
Conclusie
Deze studie toonde aan dat de mortaliteit bij patiënten met een S. pneumoniae bacteriëmie onafhankelijk was van de duur van de antimicrobiële therapie, mits de behandeling langer dan vijf dagen duurde. Een langere antimicrobiële behandelduur dan zeven dagen had geen gunstiger effect op de uitkomst. Een maximale behandelduur van zeven dagen lijkt dus adequaat. Prospectief onderzoek en het opstellen van landelijk beleid voor de behandelduur van een S. pneumoniae bacteriëmie kan bijdragen aan het verder reduceren van antibioticagebruik en zorgen voor een reductie van antibioticaresistentie, bijwerkingen, Clostridioides difficile colitis en kosten.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Peker N, Couto N, Sinha B, Rossen JW. Diagnosis of bloodstream infections from positive blood cultures and directly from blood samples: recent developments in molecular approaches. Clin Microbiol Infect. 2018 Sep;24(9):944-955.
2. Loonen AJ, Wolffs PF, Bruggeman CA, van den Brule AJ. Developments for improved diagnosis of bacterial bloodstream infections. Eur J Clin Microbiol Infect Dis. 2014 Oct;33(10):1687-702.
3. Havey TC, Fowler RA, Daneman N. Duration of antibiotic therapy for bacteremia: a systematic review and meta-analysis. Crit Care. 2011;15(6):R267.
4. Daneman N, Rishu AH, Pinto R, et al. 7 versus 14 days of antibiotic treatment for critically ill patients with bloodstream infection: a pilot randomized clinical trial. Trials. 2018 Feb 17;19(1):111.
5. GBD 2015 LRI Collaborators. Estimates of the global, regional, and national morbidity, mortality, and aetiologies of lower respiratory tract infections in 195 countries: a systematic analysis for the Global Burden of Disease Study 2015. Lancet Infect Dis. 2017 Nov;17(11):1133-1161.
6. European Centre for Disease Prevention and Control. Factsheet for health professionals about pneumococcal disease [Internet]. Stockholm: ECDC; november 2023 [geraadpleegd 2021 Dec 28].
https://www.ecdc.europa.eu/en/pneumococcal-disease/facts.
7. Rijksinstituut voor Volksgezondheid en Milieu. Pneumococcal disease [Internet]. Bilthoven: RIVM [geraadpleegd 2021 Dec 28].
https://www.rivm.nl/en/pneumococci/pneumococcal-disease-0.
8. Timsit JF, Ruppé E, Barbier F, Tabah A, Bassetti M. Bloodstream infections in critically ill patients: an expert statement. Intensive Care Med. 2020 Feb;46(2):266-284.
9. Paul M, Shani V, Muchtar E, Kariv G, Robenshtok E, Leibovici L. Systematic review and meta-analysis of the efficacy of appropriate empiric antibiotic therapy for sepsis. Antimicrob Agents Chemother. 2010 Nov;54(11):4851-63.
10. Pulcini C, Mainardi JL. Antimicrobial stewardship: an international emergency. Clin Microbiol Infect. 2014 Oct;20(10):947-8.
11. Stichting Werkgroep Antibiotica Beleid (SWAB). Guideline for empirical antibacterial therapy of sepsis in adults. 2020.
12. Stichting Werkgroep Antibiotica Beleid (SWAB), Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (NVALT). Management of Community-Acquired Pneumonia in Adults: 2016 Guideline. Update 2017.
13. Stichting Werkgroep Antibiotica Beleid (SWAB). Antibacterial therapy of adult patients with Sepsis. 2010.
14. Antibiotica Commissie Radboudumc. Sepsis - pneumokokken - streptococcus pneumoniae [Internet]. Nijmegen: Radboudumc en Maasziekenhuis Pantein, 2020 [geraadpleegd 2021 Dec 16].
https://radboudumc.adult.nl.antibiotica.app/nl/node/327893.
15. Commissie Antibioticabeleid Rijnstate / Slingeland. Sepsis - S. pneumoniae (pneumokok) [Internet]. Arnhem, 2020 [geraadpleegd 2021 Dec 16].
https://rijnstate.adult.nl.antibiotica.app/nl/node/141134.
16. Davar K, Clark D, Centor RM, et al. Can the Future of ID Escape the Inertial Dogma of Its Past? The Exemplars of Shorter Is Better and Oral Is the New IV. Open Forum Infect Dis. 2022 Dec 29;10(1):ofac706.
17. Balakrishnan I, Crook P, Morris R, Gillespie SH. Early predictors of mortality in pneumococcal bacteraemia. J Infect. 2000 May;40(3):256-61.
18. Nie W, Zhang Y, Jee SH, Jung KJ, Li B, Xiu Q. Obesity survival paradox in pneumonia: a meta-analysis. BMC Med. 2014 Apr 10;12:61.
19. Wagenvoort GH, Sanders EA, Vlaminckx BJ, et al. Invasive pneumococcal disease: Clinical outcomes and patient characteristics 2-6 years after introduction of 7-valent pneumococcal conjugate vaccine compared to the pre-vaccine period, the Netherlands. Vaccine. 2016 Feb 17;34(8):1077-85.
20. Demirdal T, Sen P, Emir B. Predictors of mortality in invasive pneumococcal disease: a meta-analysis. Expert Rev Anti Infect Ther. 2021 Jul;19(7):927-944.
21. de Greef SC, Kolwijck E, Schoffelen AF, Verduin CM. NethMap 2022. Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands in 2021. Bilthoven: Rijksinstituut voor Volksgezondheid en Milieu (RIVM); juni 2022.
Referentie
Citeer als: Hemminga WL, Cremers AJH, Gisolf EH, Roovers L, de Maat MMR. Optimale antimicrobiële behandelduur voor een Streptococcus pneumoniae bacteriëmie: 5, 7 of 10 dagen? Nederlands Platform voor Farmaceutisch Onderzoek. 2025;10:a1796.
DOI
https://www.knmp.nl/resolveuid/54efa0e263cc4e478a8db0548ecc635dOpen access



Reactie toevoegen