Onderzoek naar zelfmanagement bij astma en goed geneesmiddelengebruik (SMARAGD-studie): een pilotonderzoek
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2018;3:a1667
Kernpunten
- Openbaar apothekers in Nederland spelen een belangrijke rol in het begeleiden van astmapatiënten om hun onderhoudsmedicatie op een doeltreffende manier te gebruiken.
- Het is haalbaar om de CARAT-vragenlijst voor tweewekelijkse metingen te gebruiken.
- Elektronische monitoring verbeterde ICS-therapietrouw bij astmapatiënten.
- De stabiliteit van de ziekte gemeten met CARAT-scores, werd niet beïnvloed door op de patiënt toegesneden interventies door de apotheker, vergeleken met de gebruikelijke begeleiding.
Abstract
Self-management research of asthma and good drug use (SMARAGD study): a pilot trial
BACKGROUND
Community pharmacists play an important role in supporting patients for optimal drug use.
OBJECTIVE
To assess the effectiveness of monitoring in asthma patients with inhaled corticosteroids (ICS) on disease control.
DESIGN
Asthma patients using ICS were invited from two intervention (IG) and two control pharmacies (CG).
METHODS
Participating patients completed questionnaires at the study start and at 6-month follow-up, including the Control of Allergic Rhinitis and Asthma Test (CARAT) questionnaire. IG patients completed the CARAT questionnaire every two weeks and received counselling on disease management, ICS adherence, and inhalation technique when scores were suboptimal, deteriorating, or absent. For Turbuhaler users, additional electronic monitoring (EMI) was available, with daily alerts for ICS intake. As the primary outcome, CARAT scores at follow-up were compared between IG and CG using linear regression. As secondary outcome, refill adherence was compared using logistic regression.
RESULTS
From March to July 2015, we enrolled 39 IG and 41 CG patients. At follow-up, CARAT scores did not differ between IG and CG (-0.19; 95% confidence interval [95% CI], -2.57 to 2.20), neither did patient numbers with ICS adherence > 80% (0.82; 95% CI, 0.28-2.37). Among EMI users, CARAT scores did not differ, but ICS adherence > 80% showed a 4.52-fold increase (95% CI, 1.56-13.1) compared with EMI nonusers.
CONCLUSION
Among community-dwelling asthma patients, pharmacist monitoring did not affect CARAT scores, but EMI use showed improved ICS refill adherence.
Inleiding
Naar schatting lijden er wereldwijd 235 miljoen mensen aan astma [1]. Onderhoudstherapie met inhalatiecorticosteroïden (ICS) speelt een centrale rol bij de behandeling van astma [2]. Interventies door openbaar apothekers kunnen aantoonbaar verbetering geven in een slechte inhalatietechniek, astmacontrole, patiëntgerapporteerde astmagerelateerde functionele status, de ernst van astma en symptomen [3]. Op dit moment interveniëren apothekers vooral gedurende afhaalmomenten [4, 5], maar sommige patiënten kunnen in de tussentijd verminderde ziektecontrole ontwikkelen en patiënten die niet therapietrouw zijn, komen herhaalrecepten mogelijk niet ophalen. Tijdige interventies, gericht op de patiënten die hun astma niet optimaal onder controle hebben, kunnen effectief zijn in het voorkomen van exacerbaties en verslechtering van ziektecontrole tussen de afhaalmomenten [6-8]. Om deze interventies mogelijk te maken, zijn instrumenten nodig waarmee de ziektecontrole en medicatie-inname continu gevolgd kunnen worden. Idealiter werken patiënten en apothekers samen om de symptomen en astmacontrole actief te monitoren.
Voor het uitvoeren van deze prospectieve monitoring, kunnen vragenlijsten over astmamanagement worden gebruikt en elektronische apparatuur om geneesmiddelinname te meten [9-12]. Een voorbeeld van het eerste is de CARAT-vragenlijst (control of allergic rhinitis and asthma test), gevalideerd voor ziektemanagement bij patiënten met astma en allergische rhinitis [13-17]. Het gebruik van medicatie kan ook worden gemeten met behulp van elektronische monitoring voor de inname van inhalatiemedicatie (EMI); een gevalideerde methode om medicatie-innamepatronen in kaart te brengen [10,11,18]. Elektronische monitoring is vele jaren uitgebreid onderzocht [19-23] en recent werd aangetoond dat het een positieve invloed kan hebben op het gebruik van inhalatiemedicatie [10, 24].
Regelmatig invullen van de CARAT-vragenlijst door de patiënt en continu gebruik van EMI maakt het mogelijk om het ziektemanagement en geneesmiddelengebruik van patiënten te volgen en meten. Het is echter nog grotendeels onduidelijk wat de bruikbaarheid van deze informatie is voor het tijdig aanbieden van interventies op maat in de klinische praktijk. In theorie kunnen zorgverleners op basis van de aangeleverde gegevens een persoonlijke benadering toepassen en patiënten een interventie en begeleiding bieden die ze nodig hebben. Sommige patiënten kunnen bijvoorbeeld worden geholpen door een vereenvoudiging van het doseerschema of met praktische tips over het koppelen van geneesmiddelinname aan vaste, dagelijkse routines. Daartegenover hebben patiënten die opzettelijk therapieontrouw zijn mogelijk meer baat bij een motiverend en informatief gesprek over hun ziekte, de werking en bijwerking van hun geneesmiddelen; en profiteren patiënten met een slechte inhalatietechniek van een goede instructie hoe de inhalator beter gebruikt kan worden [7].
In deze pilot-studie onderzochten we de effecten van begeleiding en interventies op maat door apothekers, op basis van de CARAT-scores van de patiënten, vergeleken met een controlegroep die de gebruikelijke begeleiding kreeg. Secundaire uitkomstmaten waren het effect van de interventie op de therapietrouw van ICS en het aantal exacerbaties. Aanvullend werden alle resultaten geanalyseerd met betrekking tot het gebruik van EMI in een geplande subgroepanalyse.
Methoden
Dit clustergecontroleerde onderzoek werd uitgevoerd tussen maart 2015 en januari 2016 in vier openbare apotheken in het zuiden van Nederland. Nederlandse apothekers hebben een professionele en juridische verantwoordelijkheid voor de farmaceutische behandeling van hun patiënten [25]. Aangezien de meeste patiënten in Nederland één vaste apotheek bezoeken, hebben apothekers meestal de beschikking over de volledige medicatiegeschiedenis van hun patiënten [26-28]. De vier deelnemende apotheken beschikten over een vergelijkbare zorgstructuur: ze werkten volgens een gecertificeerd kwaliteitszorgsysteem en werkten goed samen met huisartsen in een gestructureerde farmacotherapie-overleggroep (gemiddeld zes huisartsen per apotheek). Geblindeerd voor de patiënten werden twee apotheken aangewezen als interventiegroep (IG) waar het begeleidingsprogramma werd uitgevoerd. Er is voor deze structuur gekozen om in elke groep vergelijkbare procedures te realiseren. De patiënten in de andere twee apotheken ontvingen de gebruikelijke farmaceutische begeleiding (controlegroep; CG).
Inclusiecriteria
Patiënten werden uitgenodigd tijdens een regulier bezoek aan de apotheek of telefonisch, als ze volgens de apotheekdatabase voldeden aan de volgende selectiecriteria:
• leeftijd 18-60 jaar;
• gebruiker van onderhoudsmedicatie voor astma.
Als medicatie werd ICS of een combinatie van ICS en een langwerkende bèta-agonist (LABA) gebruikt; ATC-codes R03BA, R03AK06 en R03AK07 [29], met ten minste twee verstrekkingen in de voorgaande zes maanden. Een actuele diagnose van astma en afwezigheid van COPD werd geverifieerd op basis van informatie van de patiënt zelf en de huisarts. Patiënten konden deelnemen als ze Nederlands konden spreken, lezen en schrijven. Toestemming werd verkregen van alle deelnemers aan dit onderzoek. De follow-up duurde zes maanden na inclusie van de patiënt.
EMI kon worden gebruikt bij de inhalatiemedicatie budesonide en formoterol (Turbuhaler) [24]. Het apparaat werd door middel van Bluetooth gekoppeld aan een applicatie (app) op de smartphone van de patiënt en registreerde elke inhalatie. De app werd gratis aan de patiënt ter beschikking gesteld en patiënten deelden vrijwillig hun gegevens met de apotheker; de gegevens werden op een veilige manier geregistreerd en waren enkel zichtbaar voor de patiënt en apotheker. Informatie over geneesmiddelengebruik was zichtbaar in de app (voor een periode van maximaal zeven dagen) en in het persoonlijke webportaal (maximaal 30 dagen) voor zowel de patiënt als de apotheker. De app herinnerde patiënten er tweemaal per dag aan om de medicatie te gebruiken. Zowel de IG- als de CG-patiënten kwamen in aanmerking voor het gebruik van deze app als ze voldeden aan de volgende, extra inclusiecriteria:
• ten minste twee verstrekkingen van budesonide en formoterol Turbuhaler (ATC-code R03AK07) [26] in de voorgaande 6 maanden;
• bezit van een smartphone;
• vaardigheden om internet te gebruiken.
Interventies
IG-apothekers en -apothekersassistenten werden getraind op het gebied van de symptomen en behandeling van astma, de mogelijke bijwerkingen en stoppen met roken. Bovendien hebben ze een drie uur durende training gevolgd in motivational interviewing, gericht op het herkennen van ambivalentie of bereidheid tot gedragsverandering bij patiënten. Ze werden ook getraind in het geven van een inhalatie-instructie en het gebruik van de CARAT-vragenlijst. De apothekers en de assistenten van alle apotheken ontvingen informatie over de EMI; echter alleen IG-apothekers gebruikten ook het portaal om de gegevens van hun patiënten te monitoren.
CG-patiënten ontvingen de reguliere zorg en controles van hun inhalatietechniek; instructies werden uitsluitend gegeven op verzoek van de patiënt. IG-patiënten kregen een één-op-één intakegesprek met een apotheker of apothekersassistent. Afhankelijk van hun behoeften en inzicht in de eigen ziekte, kregen patiënten tijdens deze sessie op hun persoonlijke situatie toegesneden informatie over de pathofysiologie van astma (symptomen en triggers), zelfmanagement (bijvoorbeeld leefstijladvies), stoppen met roken (als de patiënt rookte), en de werking van hun astmamedicatie. Hiervoor werd de informatie gebruikt uit de officiële apothekersrichtlijnen over astma en patiëntbegeleiding bij geneesmiddelengebruik [30, 31]. Verschillende aspecten van de inhalatiemedicatie werden besproken, zoals de dosering en het tijdstip van inname, het belang van therapietrouw en problemen met het regelmatig nemen van geneesmiddelen, de bijwerkingen die patiënten ondervonden en het voorkomen van deze problemen (bijvoorbeeld het spoelen van de mond na inhalatie en een goede inhalatietechniek). Bovendien werd de inhalatietechniek van de patiënt gecontroleerd door middel van een demonstratie-inhalator.
Tijdens de follow-up konden de IG-patiënten de CARAT-vragenlijst eenvoudig invullen in een app op hun smartphone of tablet. IG-patiënten werd gevraagd de app te downloaden, waarna ze elke twee weken een herinnering kregen om de vragenlijst in te vullen en de scores naar de apotheker te sturen. De patiënten kregen via hun persoonlijke e-mailadres een grafische weergave van hun CARAT-scores die ze hadden ingevuld; de resultaten werden weergegeven als scores voor beide domeinen (onderste en bovenste luchtwegen) en als een totaalscore, en werden elke twee weken per e-mail toegezonden. De terugkoppeling van deze informatie bood de IG-patiënten mogelijkheden voor zelfcontrole en inzicht in hun klachten.
Als een CARAT-score niet binnen 16 dagen werd ontvangen, wanneer de score aangaf dat de ziekte niet stabiel was (CARAT-totaalscore ≤ 10) [15, 16] of als de CARAT-score aanzienlijk was gedaald (≥ 4) [15, 16], nam de IG-apotheker via e-mail of telefoon contact op met de IG-patiënten om de reden daarvan te achterhalen. Afhankelijk van de persoonlijke situatie van de patiënt bood de apotheker een interventie op maat aan. Voor IG-patiënten in de EMI-groep kon de apotheker de EMI-gegevens gebruiken om het actuele geneesmiddelengebruik te controleren.
Uitkomstmaten
De primaire uitkomst van het onderzoek was de ziektecontrole, gemeten met de CARAT-vragenlijst, vergeleken tussen IG- en CG-patiënten. De CARAT-vragenlijst is een lijst van tien vragen, ontwikkeld om de ziektecontrole van zowel astma als allergische rhinitis te meten [13-16]. Bij de eerste negen vragen kunnen patiënten een score geven van 0 (volledig ontbreken van controle) tot 3. Bij de laatste vraag over toegenomen geneesmiddelengebruik in de voorgaande week waren er drie antwoordmogelijkheden (‘nooit’ = 3 punten, ‘minder dan 7 dagen’ = 2 punten, ‘meer dan 7 dagen’ = 0 punten) en de optie ‘ik neem geen extra medicatie om mijn astma onder controle te krijgen’, wat ook 3 punten opleverde. De CARAT-score werd berekend als de som van de scores voor alle vragen en kon lopen van 0 tot 30 [14].
Secundaire uitkomsten waren het aantal exacerbaties en verschillen in ICS-therapietrouw, gemeten volgens de MARS-5-schaal (Medication Adherence Report Scale) en de ICS-afleverdata. Exacerbaties werden geteld op basis van de afleverdata van de Stichting Farmaceutische Kengetallen (SFK) [32], gemeten in de periode van zes maanden voorafgaand aan het onderzoek en de maanden van het onderzoek. Overeenkomstig de geldende klinische richtlijnen werd een exacerbatie gedefinieerd als een behandeling met een kuur systemische corticosteroïden (ATC-codes H02AB06 en H02BA07) [29] met een dosis van ten minste 20 mg of hoger gedurende een periode van 5-14 dagen [33].
IG- en CG-patiënten vulden aan het begin en het einde van het onderzoek de MARS-5-vragenlijst in. De MARS-5-vragenlijst omvat vijf vragen over therapietrouw en meet hoe vaak verschillende redenen om geneesmiddelen niet (goed) te nemen vóórkomen [34, 35].
Therapietrouw werd berekend op basis van de ICS-afleverdata als percentage van het aantal medicatiedagen (proportion of days covered, PDC) met een onderhoudsdosis ICS [36] – al dan niet in een vaste combinatie met een LABA (ATC-codes R03BA, R03AK06, R03AK07) [29] – op basis van de aflevergegevens van SFK. We berekenden de PDC-percentages voor de periode van zes maanden voorafgaand aan het onderzoek en de zes maanden dat het onderzoek duurde. In een geplande subgroepanalyse werden alle uitkomstmaten ook vergeleken tussen patiënten met en zonder EMI.
We berekenden de minimale steekproefgrootte om een verschil te meten van 4 punten [16] in de CARAT-scores bij een veronderstelde standaarddeviatie (SD) van 7 en een verschil in therapietrouw van 15% (SD = 20%) tussen het begin en einde van het onderzoek, met een statistische power van 80% bij een tweezijdig significantieniveau van 5%. Rekening houdend met een uitvalpercentage van 5% streefden we naar de inclusie van 80 patiënten [13, 14].
Ethische goedkeuring
Het onderzoeksprotocol werd goedgekeurd door de Ethische Commissie van het Radboudumc Nijmegen (nummer 2015-1569), en het onderzoek werd geregistreerd in het Nederlands Trialregister (nummer NTR5063). Alle procedures die tijdens onderzoeken met menselijke deelnemers worden doorlopen, voldeden aan de ethische normen van de institutionele en/of nationale onderzoekscommissie, de Verklaring van Helsinki uit 1964 en latere wijzigingen of vergelijkbare ethische normen. Schriftelijke toestemming werd verkregen van alle deelnemers aan dit onderzoek.
Statistische analyse
Middels een lineaire regressieanalyse werden de CARAT-scores en therapietrouw tijdens de follow-up tussen de IG- en CG-patiënten vergeleken, waarbij werd gecorrigeerd voor de metingen voor de patiënten aan het begin van het onderzoek en voor leeftijd en geslacht. Omdat de PDC, de MARS-5-scores en het aantal kuren orale corticosteroïden niet voldeden aan de vereisten voor een lineaire regressieanalyse (bijv. een normale verdeling), werd een logistische regressieanalyse voor gedichotomiseerde waarden gebruikt, gecorrigeerd voor de leeftijd, het geslacht en de status van patiënten aan het begin van het onderzoek. Alle analyses werden uitgevoerd met IBM Corp SPSS statistics, Chicago IL, USA, versie 23.
Resultaten
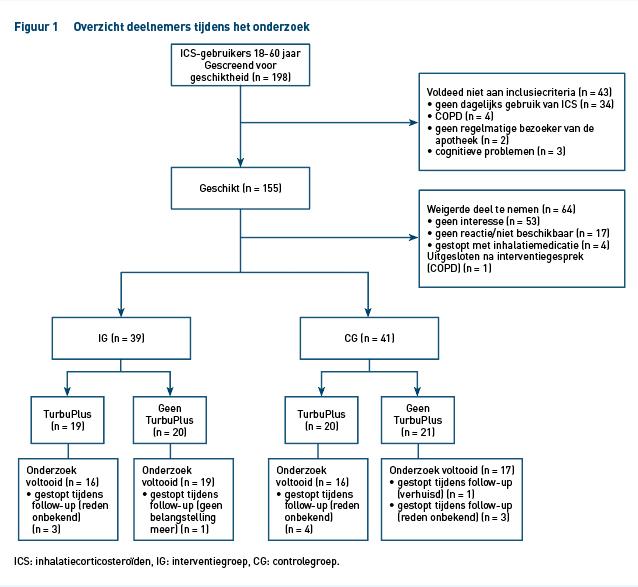
In de vier apotheken werden 198 patiënten gescreend voor geschiktheid, van wie er 155 (78,3%) voldeden aan alle inclusiecriteria (figuur 1). In totaal stemden 80 patiënten (52%) in met deelname: 41 in de CG-groep en 39 in de IG-groep. De twee studiegroepen waren vergelijkbaar qua aanvangskenmerken, zoals het type inhalatiecorticosteroïden (tabel 1). De gemiddelde leeftijd van de IG-patiënten was echter hoger dan die van de CG-patiënten: 44,95 versus 39,34 jaar; P = 0,015. Het onderzoek werd afgerond door 68 patiënten; 12 patiënten stopten tijdens de follow-up, grotendeels om onbekende redenen.
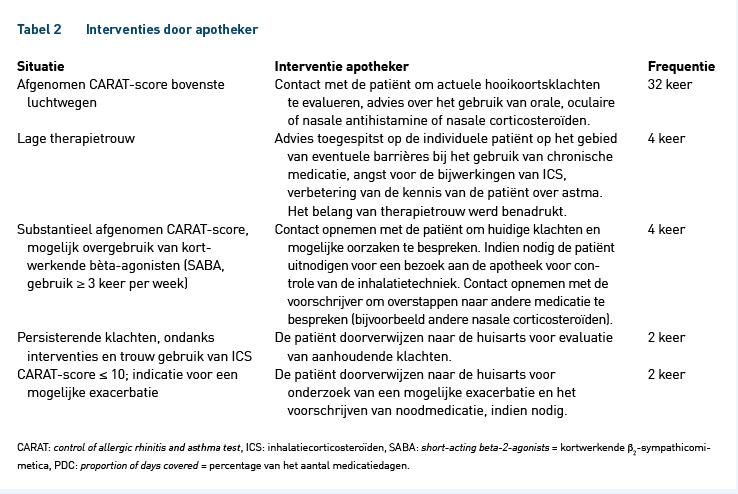
Van de 39 IG-patiënten vulden 27 alle 13 metingen in tijdens de follow-up. Op basis van verslechterende CARAT-scores werden 44 interventies uitgevoerd bij 24 (61,5%) IG-patiënten, met een maximum van vier interventies bij één patiënt (tabel 2).
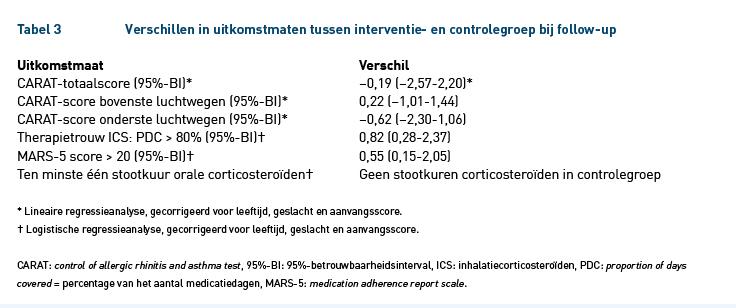
Bij de start van de studie waren de gemiddelde CARAT-scores tussen IG (20,36 punten) en CG (21,29 punten) vergelijkbaar. In een multivariate regressieanalyse verschilden de totale CARAT-scores bij de follow-up niet tussen IG en CG (tabel 3): het gemiddelde geschatte verschil was –0,19 voor de totale score; 95%-betrouwbaarheidsinterval (95%-BI), –2,57-2,20. Ook de CARAT-scores voor de bovenste luchtwegen (–0,22; 95%-BI –1,01-1,44) en onderste luchtwegen (–0,62; 95%-BI –2,30-1,06) verschilden niet. Er werd geen verschil gevonden tussen de groepen wat betreft de uitkomsten op therapietrouw: de waarschijnlijkheid van een periode waarin > 80% medicatie werden gebruikt verschilde niet tussen IG en CG (odds ratio 0,82; 95%-BI 0,28-2,37).
De waarschijnlijkheid van een score > 20 op de MARS-5-vragenlijst [28] aan het eind van het onderzoek verschilde niet tussen de twee groepen (0,55; 95%-BI 0,15-2,05). Ten slotte is er geen verschil tussen IG en CG gevonden voor het aantal exacerbaties, gemeten op basis van de kuren met orale corticosteroïden.
Er werd een geplande subgroepanalyse uitgevoerd voor de 39 patiënten met EMI vergeleken met de 41 patiënten zonder EMI. Deze groepen verschilden niet wat betreft de aanvangskenmerken, behalve de hogere gemiddelde leeftijd van de EMI-patiënten: 44,08 versus 40,17 jaar; P = 0,001 (tabel 4). In de EMI-subgroep vertoonde de therapietrouw > 80% een 4,52-voudige stijging: 95%-BI 1,56-13,1 vergeleken met de groep die geen EMI gebruikte. Er werden geen verschillen gevonden tussen de overige uitkomstmaten (tabel 5).
Discussie
Uit dit onderzoek bleek dat aanvullende, persoonlijke interventies op maat door de apotheker de controle van astma of de ICS-therapietrouw niet verbeterden, vergeleken met de gebruikelijke zorg. Met EMI zagen we effecten op de afhaaltrouw, maar niet op de CARAT- of MARS-5-scores.
Hoewel deze resultaten op het eerste gezicht teleurstellend lijken, zijn er een aantal verzachtende factoren. Ten eerste werd dit onderzoek opgezet als pilot, om het nut en de haalbaarheid van patiëntgerapporteerde monitoring in het meten van astmacontrole in de loop van de tijd te onderzoeken. In een aantal eerdere onderzoeken is gekeken naar het effect van interventies door de apotheker ter verbetering van astmacontrole, maar hierbij werd de ziektecontrole hoofdzakelijk beoordeeld met de Asthma Control Questionnaire of de Asthma Control Test in plaats van de CARAT-vragenlijst [2, 3].
Het aantal patiënten dat in aanmerking kwam en bereid was deel te nemen aan dit onderzoek was net voldoende om een verschil van 4 punten waar te nemen in de CARAT-scores tussen de studiegroepen; een waarde die wordt beschouwd als een klinisch relevante score volgens de ontwikkelaars van CARAT [16]. Bij de start van het onderzoek was er echter weinig bekend over de CARAT-scores van astmapatiënten in de eerste lijn. Ons onderzoek liet zien dat de CARAT-scores in deze populatie hoog lagen; gemiddeld 21 punten aan het begin van dit onderzoek. Tot op heden werden de CARAT-scores alleen maandelijks gemeten en was er weinig bekend over de ontwikkeling in de tijd. Het meten van CARAT-scores elke twee weken bleek haalbaar in de IG en garandeerde regelmatig contact tussen apotheker en patiënt tussen reguliere bezoeken om herhaalrecepten op te halen.
In de geplande subgroepanalyse voor EMI vertoonde de ICS-therapietrouw > 80% een 4,52-voudige stijging (95%-BI 1,56-13,1) vergeleken met die van niet-EMI-gebruikers. Wanneer uitsluitend patiënten met CARAT-scores lager dan 23 punten aan het begin van het onderzoek werden meegerekend, was de OR voor hogere CARAT-scores aan het eind van het onderzoek 2,87 (95%-BI 0,61-13,6) voor de EMI-groep in vergelijking met de niet-EMI-groep. Deze bevinding suggereert dat slechte astmacontrole vanwege het nemen van te weinig ICS als onderhoudsmedicatie in deze populatie effectiever kan worden verbeterd met EMI dan met persoonlijke interventies door de apotheker. De uitkomsten ten aanzien van het probleem om de effecten van persoonlijke interventies op ziektecontrole aan te tonen zijn niet uniek: een recent onderzoek naar persoonlijk advies over gezondheid en leefstijl aan patiënten met hart- en vaatziekten gaf ook aan dat er geen effect was op de primaire uitkomst [37]. Dit suggereert dat EMI voor astmapatiënten in de eerste lijn voldoende kan zijn om de therapietrouw te verbeteren, maar de effecten op de ziektecontrole zijn nog onduidelijk. Daarbij kan selectiebias in dit onderzoek niet volledig worden uitgesloten, omdat deelname aan het onderzoek en het gebruik van EMI vrijwillig was. Alle inwoners in Nederland zijn echter verplicht een zorgverzekering af te sluiten, die toegang biedt tot alle astmamedicatie. We verwachten daarom geen selectiebias van deze aard.
Het ontbreken van spirometrische bevestiging van de astmadiagnose kan worden gezien als een beperking. Apothekers hebben echter normaliter geen toegang tot deze gegevens. In overeenstemming met de klinische praktijk werd aanvankelijk uitgegaan van een astmadiagnose op basis van het gebruik van astmamedicatie; dit werd geverifieerd bij de patiënt en op basis van de geregistreerde contra-indicaties in het computersysteem van de huisarts, indien beschikbaar. Er was geen informatie beschikbaar over comorbiditeiten van de patiënten. Hoewel de deelnemende astmapatiënten relatief jong zijn en de leeftijd van patiënten in de groepen vergelijkbaar was, kunnen we niet volledig uitsluiten dat we misschien verschillen tussen de groepen op grond van comorbiditeit hebben gemist.
Het aantal exacerbaties en het gebruik van stootkuren met orale corticosteroïden was laag in beide groepen. Een subanalyse waarin de stootkuren tot een maat werden samengevoegd, vertoonde geen statistische significante uitkomsten.
Ten slotte kan het gebruik van EMI in zowel de IG als CG invloed hebben gehad op onze interventie. Echter, bij nadere analyse zagen we geen aanwijzing voor een effectmodificatie tussen de interventie en EMI-gebruik (P = 0,11).
Conclusie
In deze studie is geen effect aangetoond van interventies op maat door apothekers, op patiëntgerapporteerde ziektecontrole in een algemene astmapopulatie, vergeleken met de gebruikelijke zorg. Ten ondersteuning bij niet-intentionele therapieontrouw bij deze populatie kan EMI effectief zijn, maar deze strategie moet op klinische uitkomsten worden bevestigd op basis van een groter aantal patiënten gedurende een langere follow-up periode.
Verantwoording
We bedanken Kalinde Caland, Mariska van der Ham, Martika van Hedel, Helma Luijpen en Annemarie Vissers voor hun hulp bij dit onderzoek.
Dit werk werd gefinancierd met een onvoorwaardelijke onderzoeksbeurs van de Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie (KNMP) en AstraZeneca (subsidie nrs. PR16_1410, 2603949255). Vanwege de onvoorwaardelijke aard van de financiering hoeft geen van de auteurs een belangenconflict op te geven.
Dit artikel is een vertaling van: Kuipers E, Wensing M, de Smet P, Teichert M. Self-management research of asthma and good drug use (SMARAGD study): a pilot trial. Int J Clin Pharm. 2017 aug;39(4):888-896.
Literatuur
1. Asthma fact sheet 307 [internet]. World Health Organization; 2013 [geraadpleegd op 20 januari 2016]. http://www.who.int/mediacentre/factsheets/fs307/en/
2. Mehuys E, Van Bortel L, De Bolle L, et al. Effectiveness of pharmacist intervention for asthma control improvement. Eur Respir J. 2008;31(4):790-9.
3. Garcia-Cardenas V, Armour C, Benrimoj SI, Martinez-Martinez F, Rotta I, Fernandez-Llimos F. Pharmacists’ interventions on clinical asthma outcomes: a systematic review. Eur Respir J. 2016;47(4):1134-43.
4. Bereznicki BJ, Peterson G, Jackson S, et al. Uptake and effectiveness of a community pharmacy intervention programme to improve asthma management. J Clin Pharm Ther. 2013;38(3):212-8.
5. Bereznicki BJ, Peterson GM, Jackson SL, Walters EH, Fitzmaurice KD, Gee PR. Data-mining of medication records to improve asthma management. Med J Aust. 2008;189(1):21-5.
6. Van Boven JF, Stuurman-Bieze AG, Hiddink EG, Postma MJ, Vegter S. Medication monitoring and optimization: a targeted pharmacist program for effective and cost-effective improvement of chronic therapy adherence. J Manag Care Spec Pharm. 2014;20(8):786-92.
7. Van Boven JF, Trappenburg JC, van der Molen T, Chavannes NH. Towards tailored and targeted adherence assessment to optimize asthma management. NPJ Prim Care Respir Med. 2015;25:15046.
8. Thomas M. Why aren’t we doing better in asthma: time for personalised medicine? NPJ Prim Care Respir Med. 2015;25:15004.
9. Foster JM, Usherwood T, Smith L, et al. Inhaler reminders improve adherence with controller treatment in primary care patients with asthma. J Allergy Clin Immunol. 2014;134(6):1260-8.e3.
10. Riekert KA, Rand CS. Electronic monitoring of medication adherence: when is high-tech best? J Clin Psychol Med Set. 2002;9(1):25-34.
11. Tran N, Coffman JM, Sumino K, Cabana MD. Patient reminder systems and asthma medication adherence: a systematic review. J Asthma. 2014;51(5):536-43.
12. Tommelein E, Mehuys E, Van Tongelen I, Brusselle G, Boussery K. Accuracy of the Medication Adherence Report Scale (MARS-5) as a quantitative measure of adherence to inhalation medication in patients with COPD. Ann Pharmacother. 2014;48(5):589-95.
13. Azevedo P, Correia de Sousa J, Bousquet J, et al. Control of Allergic Rhinitis and Asthma Test (CARAT): dissemination and applications in primary care. Prim Care Respir J. 2013;22(1):112-6.
14. Fonseca JA, Nogueira-Silva L, Morais-Almeida M, et al. Validation of a questionnaire (CARAT10) to assess rhinitis and asthma in patients with asthma. Allergy. 2010;65(8):1042-8.
15. Fonseca JA, Nogueira-Silva L, Morais-Almeida M, et al. Control of Allergic Rhinitis and Asthma Test (CARAT) can be used to assess individual patients over time. Clin Transl Allergy. 2012;2(1):16.
16. Van der Leeuw S, van der Molen T, Dekhuijzen PN, et al. The minimal clinically important difference of the control of allergic rhinitis and asthma test (CARAT): cross-cultural validation and relation with pollen counts. NPJ Prim Care Respir Med. 2015;25:14107.
17. CARAT Questionnaire [internet]. CARATnetwork; [geraadpleegd op 24 juli 2015]. http://www.caratnetwork.org/index.php?option=com_fastcarat&lang=en
18. Sumino K, Cabana MD. Medication adherence in asthma patients. Curr Opin Pulm Med. 2013;19(1):49–53.
19. Meghani SH, Knafl GJ. Patterns of analgesic adherence predict health care utilization among outpatients with cancer pain. Patient Prefer Adherence. 2016;10:81-98.
20. Dunn KE, King VL, Brooner RK. Comparison of methods to assess psychiatric medication adherence in methadone-maintained patients with co-occurring psychiatric disorder. Drug Alcohol Depend. 2016;160:212-7.
21. Clifford S, Perez-Nieves M, Skalicky AM, Reaney M, Coyne KS. A systematic literature review of methodologies used to assess medication adherence in patients with diabetes. Curr Med Res Opin. 2014;30(6):1071-85.
22. Vrijens B, Urquhart J. Methods for measuring, enhancing, and accounting for medication adherence in clinical trials. Clin Pharmacol Ther. 2014;95(6):617-26.
23. Wamboldt FS, Bender BG, O’Connor SL, et al. Reliability of the model MC-311 MDI chronolog. J Allergy Clin Immunol. 1999;104(1):53-7.
24. Pilcher J, Shirtcliffe P, Patel M, et al. Three-month validation of a turbuhaler electronic monitoring device: implications for asthma clinical Int J Clin Pharm trial use. BMJ Open Respir Res. 2015;2(1):e000097.
25. WGBO: geneeskundige behandelingsovereenkomst [internet]. Nederlandse overheid; 2016 [geraadpleegd op 4 mei 2016]. http://wetten.overheid.nl/BWBR0007021/2006-02-01
26. Buurma H, Bouvy ML, de Smet PA, Floor-Schreudering A, Leufkens HG, Egberts AC. Prevalence and determinants of pharmacy shopping behaviour. J Clin Pharm Ther. 2008;33(1):17-23.
27. Ottenbros S, Teichert M, de Groot R, et al. Pharmacist-led intervention study to improve drug therapy in asthma and COPD patients. Int J Clin Pharm. 2014;36(2):336-44.
28. Teichert M, Schermer T, van den Nieuwenhof L, de Smet PA, Wensing M. Prevalence of inappropriate prescribing of inhaled corticosteroids for respiratory tract infections in the Netherlands: a retrospective cohort study. NPJ Prim Care Respir Med. 2014;24:14086.
29. ATC classifications system 2013 [internet]. Oslo: World Health Organization collaborating centre for drug statistics methodology; 2013 [geraadpleegd op 26 mei 2016]. http://www.whocc.no/atc_ddd_index
30. KNMP-richtlijn Ter hand stellen [internet]. Den Haag: KNMP; 2013 [geraadpleegd op 19 september 2014]. https://www.knmp.nl/praktijkvoering/bekostiging/begeleidingsgesprek-nieuw-geneesmiddel/knmp-richtlijn-ter-hand-stellen-juni-2013
31. Geneesmiddel informatie centrum. Standaarden voor zelfzorg [internet]. Den Haag: KNMP; 2014.
32. Mabotuwana T, Warren J, Harrison J, Kenealy T. What can primary care prescribing data tell us about individual adherence to long-term medication?-comparison to pharmacy dispensing data. Pharmacoepidemiol Drug Saf. 2009;18(10):956-64.
33. Nederlands Huisartsen Genootschap. NHG-Standaard Astma bij volwassenen (derde herziening). In: Huisarts Wet; 2015.
34. Menckeberg TT, Bouvy ML, Bracke M, JA, et al. Beliefs about medicines predict refill adherence to inhaled corticosteroids. J Psychosom Res. 2008;64(1):47-54.
35. Koster ES, Raaijmakers JA, Vijverberg SJ, Maitland-van der Zee AH. Inhaled corticosteroid adherence in paediatric patients: the PACMAN cohort study. Pharmacoepidemiol Drug Saf. 2011;20(10):1064-72.
36. Steiner JF, Prochazka AV. The assessment of refill compliance using pharmacy records: methods, validity, and applications. J Clin Epidemiol. 1997;50(1):105-16.
37. Van Lieshout J, Huntink E, Koetsenruijter J, Wensing M. Tailored implementation of cardiovascular risk management in general practice: a cluster randomized trial. Implement Sci. 2016;11:115.
Referentie
Citeer als: Kuipers E, Wensing M, de Smet P, Teichert M. Onderzoek naar zelfmanagement bij astma en goed geneesmiddelengebruik (SMARAGD-studie): een pilotonderzoek. Nederlands Platform voor Farmaceutisch Onderzoek. 2018;3:a1667.
DOI
https://www.knmp.nl/resolveuid/abc5809f9adb43af9603336aeb462b4bOpen access




Reactie toevoegen