Het effect van de introductie van een clinical decision support tool op het percentage adequaat voorgeschreven LMWH-tromboseprofylaxe
- Rubriek: Korte bijdrage
- Identificatie: 2024;9:a1778
Kernpunten
- Een aanzienlijk deel van de opgenomen niet-chirurgische patiënten ontvangt ten onrechte geen tromboseprofylaxe met een laag-molecuulgewicht heparine (LMWH).
- Implementatie van een clinical decision support tool in het elektronisch patiëntendossier had geen significant effect op het percentage adequaat voorgeschreven tromboseprofylaxe.
- Patiënten met een hoog risico op een veneuze trombo-embolie (VTE) kunnen goed geïdentificeerd worden met behulp van een clinical decision support tool.
Abstract
The effect of the implementation of a clinical decision support (CDS) tool on the percentage of adequately prescribed LMWH-thromboprophylaxis
Background
Non-surgical patients have an increased risk of developing a venous thromboembolism (VTE) during hospital admission. This risk can be reduced by thromboprophylaxis with low molecular weight heparins (LMWHs). In thromboprophylaxis guidelines the Padua Prediction Score (PPS) has been suggested as the best available model to assess the risk of VTE in these patients, but adherence to these guidelines is known to be low.
Objective
To increase the percentage of adequately prescribed thromboprophylaxis with a LMWH in patients with a high VTE risk by implementation of an intervention consisting of a clinical decision support (CDS) tool in the electronic health record. Secondary specificity and sensitivity of the CDS tool were determined.
Design and methods
Data on the PPS and thromboprophylaxis in non-surgical patients (≥ 18 years) were prospectively collected for a total of ten time points before and after the implementation of the intervention. Patients who recently (< 1 week) underwent a percutaneous coronary intervention, and palliative patients were excluded. A time series analysis was performed using an autoregressive integrated moving average (ARIMA) model to examine the effect of the intervention on the percentage of adequately prescribed LMWH thromboprophylaxis.
Results
400 patients were included, 200 patients pre- and 200 patients post-intervention. Assuming a direct effect of the intervention on the percentage of adequately prescribed LMWH thromboprophylaxis a level effect of 7.5% was calculated, this level effect was not significant (P = 0.19). The CDS tool had a sensitivity of 92% and a specificity of 68%.
Conclusion
The implementation of a CDS tool had no significant effect on the percentage of patients adequately treated with thromboprophylaxis in an interrupted time series analysis. The CDS tool was able to successfully identify patients with a high risk of developing a VTE.
Inleiding
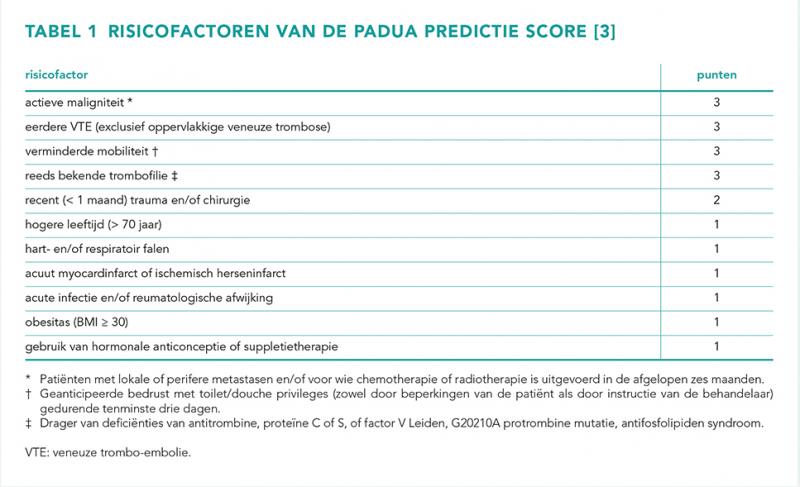
Veneuze trombo-embolie (VTE) is de op drie na meest voorkomende cardiovasculaire diagnose, met een jaarlijkse incidentie van ongeveer 1 per 1000 in personen van middelbare leeftijd tot bijna 1% in personen met een leeftijd tussen de 90 en 99 jaar [1]. Klinische patiënten hebben een verhoogde kans op het ontwikkelen van VTE. Ongeveer 3% van de opgenomen patiënten ontwikkelt een VTE en ongeveer 50% van alle gevallen van VTE treedt op tijdens of na een recente ziekenhuisopname Het effect van de introductie van een clinical decision support tool op het percentage adequaat voorgeschreven LMWH-tromboseprofylaxe [2,3]. De kans op het ontwikkelen van een VTE tijdens een ziekenhuisopname is te verlagen door het geven van tromboseprofylaxe aan patiënten met een verhoogd risico op VTE [3,4]. In de richtlijn voor tromboseprofylaxe van het American College of Chest Physicians (ACCP) en de richtlijn Antitrombotisch beleid van de Nederlandse Internisten Vereniging (NIV) wordt tromboseprofylaxe met een laag-molecuulgewicht heparine (LMWH) geadviseerd voor opgenomen patiënten met een verhoogd risico op VTE [5,6]. Voor het inschatten van het risico op VTE bij opgenomen niet-chirurgische patiënten wordt in deze richtlijnen de Padua Predictie Score (PPS) [3] als het best beschikbare model benoemd (tabel 1).
Uit onderzoek blijkt dat de naleving van de richtlijnen voor tromboseprofylaxe laag is [7-11]. Het Nivel publiceerde in 2017 een rapport waarin de toepassing van tromboseprofylaxe in Nederland werd geëvalueerd. Hieruit bleek dat 49% van de niet-chirurgische patiënten met een hoog risico op VTE tromboseprofylaxe kreeg conform de Nederlandse richtlijn [12]. Uit onderzoek van Jaspers et al. is gebleken dat een veelzijdige interventie de naleving van richtlijnen voor tromboseprofylaxe kan verbeteren, waarbij de ontwikkelde clinical decision support (CDS)-tool de meest effectieve interventie zou zijn [13]. Een CDS-tool is een ondersteuningstool voor klinische besluitvorming die informatie haalt uit het elektronisch patiëntendossier en op basis daarvan een geautomatiseerd advies aan de voorschrijver geeft. Het doel van deze studie is het verhogen van het percentage adequaat voorgeschreven LMWH-tromboseprofylaxe aan patiënten met een hoog risico op het ontwikkelen van een VTE door implementatie van een interventie bestaande uit een CDS-tool. Daarnaast is onderzocht hoe goed de CDS-tool in staat is om hoogrisicopatiënten te identificeren.
Methoden
De studie is uitgevoerd in het Medisch Centrum Leeuwarden, een topklinisch opleidingsziekenhuis met 653 bedden. De studie heeft een interrupted time series design, waarbij prospectief data over tromboseprofylaxe bij hoogrisicopatiënten is verzameld op vijf tijdspunten voor en vijf tijdspunten na interventie. De interventie bestond uit de implementatie van een CDS-tool bestaande uit een Best Practice Advisory (BPA) in Epic (Epic Systems, Verona, USA). De BPA geeft een geautomatiseerd advies aan de voorschrijver over de indicatie van LMWH-tromboseprofylaxe op basis van de PPS. Het advies wordt getoond als pop-up bij het openen van het patiëntendossier. Adequaat voorgeschreven tromboseprofylaxe is gedefinieerd als tromboseprofylaxe met een LMWH voorgeschreven bij patiënten met een PPS van ≥ 4. Mogelijke contra-indicaties voor tromboseprofylaxe, zoals een actieve bloeding, zijn niet meegenomen. Niet-chirurgische patiënten ≥ 18 jaar die gedurende minimaal 48 uur opgenomen waren op een niet-chirurgische verpleegafdeling met een berekende PPS van ≥ 4 werden geïncludeerd. Patiënten die recent (< 1 week) een percutane coronaire interventie (PCI) hadden ondergaan en patiënten met een palliatief of abstinerend beleid werden geëxcludeerd. Data voor de verschillende tijdspunten is verzameld tussen juni 2022 en juli 2023, waarbij elk tijdspunt staat voor een maand in de tijd. Data is verzameld vanaf de eerste werkdag van de maand, tot 40 patiënten per tijdspunt waren geïncludeerd. Het aantal te includeren patiënten per tijdspunt is vastgesteld op basis van beschikbare literatuur met betrekking tot uitvoering van een interrupted time series analyse [14,15]. De interventie is in maart 2023 geïmplementeerd. Voor de berekening van de sensitiviteit en specificiteit van de CDS-tool zijn 150 niet-chirurgische patiënten ≥ 18 jaar die minimaal 48 uur opgenomen waren geïncludeerd. De PPS is voor alle patiënten handmatig berekend, waarbij patiënten zijn verdeeld in laag- en hoogrisicopatiënten. Er is onderzocht bij welke patiënten de CDS-tool getriggerd heeft, om de sensitiviteit en specificiteit van de CDS-tool te kunnen berekenen.
De statistische analyses zijn uitgevoerd in IBM SPSS (versie 28). Het primaire eindpunt werd getoetst met een time series analyse waarbij gebruik werd gemaakt van een ARIMA-model. Een secundaire analyse werd uitgevoerd met de Fisher-exacttoets. Voor het vergelijken van de patiëntkarakteristieken werd gebruik gemaakt van de Mann-Whitneytoets voor continue variabelen en de Fisher-exacttoets voor categorische variabelen. Een P-waarde van < 0,05 werd als significant beschouwd.
Resultaten
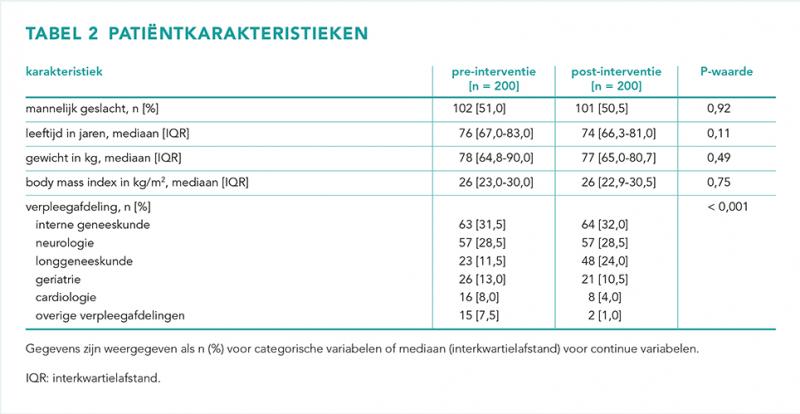
In totaal zijn 400 patiënten geïncludeerd, 40 patiënten per tijdspunt. Patiëntkarakteristieken worden weergegeven in tabel 2.
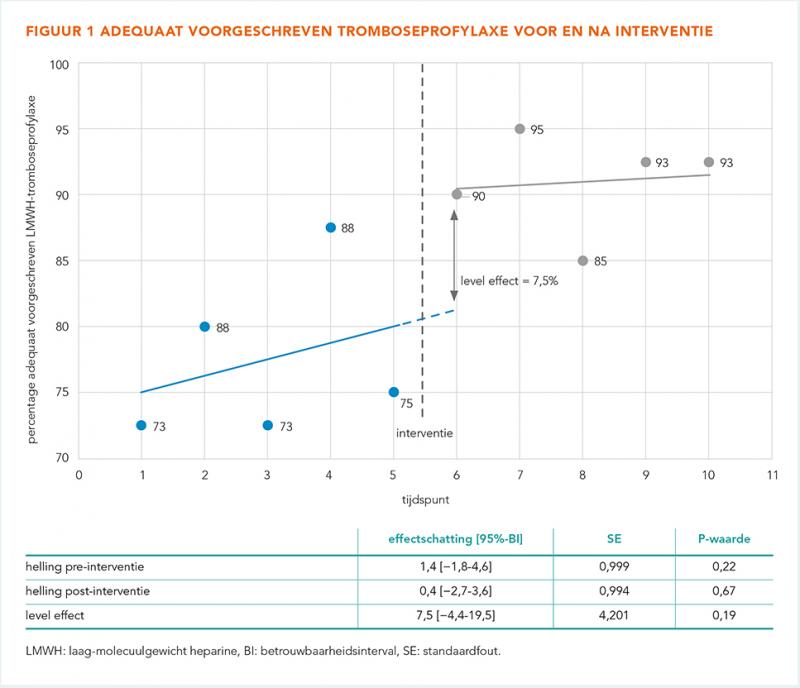
Vóór implementatie van de CDS-tool was een niet-significante toename te zien in adequaat voorgeschreven tromboseprofylaxe (helling 1,4%; betrouwbaarheidsinterval [BI]−1,8-4,6; P = 0,22), wat niet wijst op de aanwezigheid van een trend pre-interventie (figuur 1). Na implementatie van de CDS-tool was er een direct niet-significant positief effect van 7,5% te zien op het percentage adequaat voorgeschreven tromboseprofylaxe ([BI] −4,4-19,5; P = 0,19). Dit effect nam niet verder toe in de tijd. De toename in adequaat voorgeschreven tromboseprofylaxe postinterventie was niet-significant (helling 0,4%; [BI] −4,4-19,5; P = 0,67, zie figuur 1).
Uit de secundaire analyse, waarbij de data van alle tijdspunten voor en na interventie gecombineerd en met elkaar vergeleken is, blijkt een significante toename in het percentage adequaat voorgeschreven tromboseprofylaxe van 78% tot 91% na implementatie van de CDS-tool (P < 0,001).
De geïmplementeerde CDS-tool behaalde een sensitiviteit van 92% en een specificiteit van 68%.
Beschouwing
De implementatie van een interventie bestaande uit een CDS-tool in het elektronisch patiëntendossier, die voorschrijvers ondersteunt bij het voorschrijven van tromboseprofylaxe aan hoogrisicopatiënten, leidt niet tot een hoger percentage voorgeschreven LMWH-tromboseprofylaxe. De geïmplementeerde CDS-tool bleek in staat om patiënten met een hoog risico op het ontwikkelen van een VTE met een sensitiviteit van 92% en een specificiteit van 68% te identificeren.
Voor implementatie van de interventie werd een gemiddeld percentage van 78% adequaat voorgeschreven tromboseprofylaxe gevonden in de verschillende tijdspunten. In recent Nederlands onderzoek van Jaspers et al. werd een naleving van de tromboseprofylaxe richtlijn gevonden van 54,5% voor niet-chirurgische patiënten met een hoog risico op ontwikkelen van een VTE [13]. Een internationaal dwarsdoorsnedeonderzoek uitgevoerd in 32 landen rapporteerde dat gemiddeld 39,5% van de niet-chirurgische hoogrisicopatiënten adequate tromboseprofylaxe ontving [8]. Het door ons gevonden percentage van 78% pre-interventie is daarmee hoger dan verwacht op basis van eerdere studies. Dit kan mogelijk worden verklaard doordat in de afgelopen periode meer aandacht was voor tromboseprofylaxe door aanpassing van de landelijke doseeradviezen voor patiënten met een hoog BMI [16] of door de COVID-19 pandemie. De gevonden sensitiviteit en specificiteit van respectievelijk 92% en 68% komt overeen met andere ontwikkelde CDS-tools [17,18].
Een sterk punt van dit onderzoek is het interrupted time series design. Door verzameling van data op verschillende tijdspunten voor en na interventie wordt de invloed van potentiële onderliggende trends meegenomen. Dit is tegelijkertijd ook de zwakte van deze studie, aangezien de data verdeeld worden over verschillende tijdspunten, waarbij er voldoende tijdspunten en patiënten per tijdspunt moeten zijn om een significant effect te kunnen aantonen. Er is geen gouden standaard voor het minimaal aantal datapunten en het minimaal aantal observaties per datapunt [14,15]. Mogelijk was het aantal patiënten (n = 40) per tijdspunt in onze studie te klein om een significant effect aan te kunnen tonen.
Met de komst van elektronische patiëntendossiers is het mogelijk geworden om voorschrijvers te ondersteunen in de klinische besluitvorming op basis van specifieke patiëntkenmerken die zijn vastgelegd in het patiëntendossier. Om een goed advies te kunnen formuleren voor de individuele patiënt is het noodzakelijk dat data op de juiste manier en op de juiste plek in het dossier van de patiënt worden vastgelegd en bijgehouden. Uit dit onderzoek is gebleken dat specifieke patiënten, in dit geval patiënten met een hoog risico op het ontwikkelen van een VTE, met een CDS-tool goed kunnen worden herkend. Dit biedt mogelijkheden voor de ontwikkeling van CDS-tools om voorschrijvers te ondersteunen in de klinische besluitvorming.
Conclusie
Wij vonden in ons onderzoek dat de implementatie van een CDS-tool voor het voorschrijven van tromboseprofylaxe aan patiënten met een hoog risico op het ontwikkelen van een VTE volgens de PPS niet leidde tot een significante toename in het percentage adequaat voorgeschreven LMWH-tromboseprofylaxe.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Benjamin EJ, Virani SS, Callaway CW, et al. American Heart Association Council on Epidemiology and Prevention Statistics Committee and Stroke Statistics Subcommittee. Heart Disease and Stroke Statistics-2018 Update: A Report From the American Heart Association. Circulation. 2018 Mar 2020;137(12):e67-e492.
2. Heit JA, O'Fallon WM, Petterson TM, et al. Relative impact of risk factors for deep vein thrombosis and pulmonary embolism: a population-based study. Arch Intern Med. 2002 Jun 10;162(11):1245-8.
3. Barbar S, Noventa F, Rossetto V, et al. A risk assessment model for the identification of hospitalized medical patients at risk for venous thromboembolism: the Padua Prediction Score. J Thromb Haemost. 2010 Nov;8(11):2450-7.
4. Dentali F, Douketis JD, Gianni M, Lim W, Crowther MA. Meta-analysis: anticoagulant prophylaxis to prevent symptomatic venous thromboembolism in hospitalized medical patients. Ann Intern Med. 2007 Feb 20;146(4):278-88.
5. Kahn SR, Lim W, Dunn AS, et al. Prevention of VTE in nonsurgical patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012 Feb;141(2 Suppl):e195S-e226S.
6. Richtlijn Antitrombotisch beleid [internet]. Utrecht: Nederlandse Internisten Vereniging; 2015 [geraadpleegd 2023 Sep 20]. https://www.nvvc.nl/Richtlijnen/Richtlijn%20Antitrombotisch%20beleid_def.pdf
7. Goldhaber SZ, Dunn K, MacDougall RC. New onset of venous thromboembolism among hospitalized patients at Brigham and Women's Hospital is caused more often by prophylaxis failure than by withholding treatment. Chest. 2000 Dec;118(6):1680-4.
8. Cohen AT, Tapson VF, Bergmann JF, et al. Venous thromboembolism risk and prophylaxis in the acute hospital care setting (ENDORSE study): a multinational cross-sectional study. Lancet. 2008 Feb 2;371(9610):387-94.
9. Tapson VF, Decousus H, Pini M, et al. Venous thromboembolism prophylaxis in acutely ill hospitalized medical patients: findings from the International Medical Prevention Registry on Venous Thromboembolism. Chest. 2007 Sep;132(3):936-45.
10. Kucher N, Spirk D, Baumgartner I, et al. Lack of prophylaxis before the onset of acute venous thromboembolism among hospitalized cancer patients: the SWIss Venous ThromboEmbolism Registry (SWIVTER). Ann Oncol. 2010 May;21(5):931-5.
11. Chopard P, Dörffler-Melly J, Hess U, et al. Venous thromboembolism prophylaxis in acutely ill medical patients: definite need for improvement. J Intern Med. 2005 Apr;257(4):352-7.
12. Moesker MJ, Damen NL, de Groot JF, de Bruijne MC, Wagner C. Antistollingszorg in Nederlandse ziekenhuizen: evaluatie van tromboseprofylaxe en perioperatief antistollingsbeleid in vergelijking met geldende richtlijnen [internet]. Utrecht: Nivel; 2017 Jul 24 [geraadpleegd 2023 Sep 20].
https://www.nivel.nl/nl/publicatie/antistollingszorg-nederlandse-ziekenhuizen-evaluatie-van-tromboseprofylaxe-en
13. Jaspers T, Duisenberg-van Essenberg M, Maat B, Durian M, van den Berg R, van den Bemt P. A multifaceted clinical decision support intervention to improve adherence to thromboprophylaxis guidelines. Int J Clin Pharm. 2021 Oct;43(5):1327-1336.
14. Zhang F, Wagner AK, Ross-Degnan D. Simulation-based power calculation for designing interrupted time series analyses of health policy interventions. J Clin Epidemiol. 2011 Nov;64(11):1252-61.
15. Ramsay CR, Matowe L, Grilli R, Grimshaw JM, Thomas RE. Interrupted time series designs in health technology assessment: lessons from two systematic reviews of behavior change strategies. Int J Technol Assess Health Care. 2003 Fall;19(4):613-23.
16. Morbide obesitas: nadroparine [internet]. Den Haag: KNMP Kennisbank; 2019 Okt 14 [geraadpleegd 2023 Sep 20].
https://kennisbank.knmp.nl/article/contra-indicaties_aandoeningen/7002.html
17. Dewan M, Vidrine R, Zackoff M, et al. Design, Implementation, and Validation of a Pediatric ICU Sepsis Prediction Tool as Clinical Decision Support. Appl Clin Inform. 2020 Mar;11(2):218-225.
18. Vande Casteele N, Jairath V, Jeyarajah J, et al. Development and Validation of a Clinical Decision Support Tool That Incorporates Pharmacokinetic Data to Predict Endoscopic Healing in Patients Treated With Infliximab. Clin Gastroenterol Hepatol. 2021 Jun;19(6):1209-1217.e2.
Referentie
Citeer als: Van Gosliga FT, Pals D, van Ojik AL, van Roon EN. Het effect van de introductie van een clinical decision support tool op het percentage adequaat voorgeschreven LMWH-tromboseprofylaxe. Nederlands Platform voor Farmaceutisch Onderzoek. 2024;9:a1778.
DOI
https://www.knmp.nl/resolveuid/c61e6d74d45d42fda322b267f5afbe3dOpen access

Reactie toevoegen