De PIM POM studie: prevalentie van Potentieel Inadequate Medicatie en Potentieel Ontbrekende Medicatie in oudere oncologiepatiënten
- Rubriek: Korte bijdrage
- Identificatie: 2022;7:a1747
Kernpunten
- De prevalentie van Potentieel Inadequate Medicatie (PIM’s) en Potentieel Ontbrekende Medicatie (POM’s) in oudere oncologiepatiënten is hoog.
- Uitgebreide medicatiebeoordelingen door apothekers zijn een goede manier om deze PIM’s en POM’s te identificeren en medicatiegebruik te optimaliseren.
- Het gebruik van de expert opinion van apothekers bij deze medicatiebeoordelingen is, naast het gebruik van enkel gestandaardiseerde criteria, van toegevoegde waarde en wordt sterk aanbevolen.
Abstract
Prevalence of Potentially Inappropriate Medication and Potentially Omitted Medication in older cancer patients - the PIM POM study
Background
Older cancer patients are at high risk for drug-related problems. Pharmacist-led comprehensive medication reviews may optimize treatment and thereby reduce the risk of harmful effects from medication use.
Objective
To determine the prevalence of Potentially Inappropriate Medication (PIMs) and Potentially Omitted Medication (POMs) in older cancer patients.
Design
Prospective observational study.
Methods
(Hospital) pharmacists conducted comprehensive medication reviews in older cancer patients (aged ≥ 65 years) receiving parenteral chemo and/or immunotherapy at the Deventer Hospital. PIMs and POMs were identified using the Screening Tool of Older Persons’ potentially inappropriate Prescriptions (STOPP), the Screening Tool to Alert doctors to the Right Treatment (START) and pharmacists’ expert opinion. Recommendations regarding PIMs and POMs were communicated to the patient’s oncologist/haematologist and follow-up was measured. Associations between covariates and the prevalence of PIMs and POMs were statistically analysed.
Results
For the 150 patients included, 180 PIMs and 86 POMs were identified with a combined prevalence of 78%. Using pharmacists’ expert opinion in addition to only STOPP/START criteria contributed to 49% of the PIMs and 23% of the POMs. A follow-up action was required in 73% of the 266 PIMs and POMs. Number of medicines and Charlson Comorbidity Index score were both independently associated with having at least one PIM and/or POM (P = 0.031 and P = 0.002, respectively).
Conclusion
The prevalence of PIMs and POMs in older cancer patients is high. A pharmacist-led comprehensive medication review is a good instrument to identify these PIMs and POMs and to optimize patients’ treatment. A complete approach, including pharmacists’ expert opinion, is recommended to identify all PIMs and POMs in clinical practice.
Inleiding
Fysiologische veranderingen, multimorbiditeit en frequent geneesmiddelgebruik maken ouderen een hoogrisicogroep voor geneesmiddelgerelateerde problemen (drug-related problems [DRP’s]). De diagnose kanker vergroot dit risico. Behandeling leidt namelijk tot meer geneesmiddelen, meer zorgverleners en grotere ziektelast. Vele ziekenhuisbezoeken en bijbehorende informatieoverdracht zijn extra risico’s voor DRP’s, wat kan leiden tot suboptimale behandeling. Door vergrijzing neemt deze populatie toe en wordt optimalisatie van medicatiegebruik steeds belangrijker [1-5].
Apothekers kunnen in een multidisciplinair team een belangrijke rol spelen in het reduceren van DRP’s door medicatiebeoordelingen uit te voeren [6-9]. Er zijn meerdere criteria beschikbaar om Potentieel Inadequate Medicatie (PIM’s) en Potentieel Ontbrekende Medicatie (POM’s) te identificeren, zoals de STOPP/START-criteria (Screening Tool of Older Persons’ potentially inappropriate Prescriptions / Screening Tool to Alert doctors to the Right Treatment) [10]. Met deze criteria worden echter niet alle relevante DRP’s geïdentificeerd, waardoor een uitgebreidere medicatiebeoordeling nodig is [2,11].
De multidisciplinaire richtlijn ‘Polyfarmacie bij ouderen’ beveelt medicatiebeoordelingen aan bij polyfarmaciepatiënten ≥ 65 jaar met minimaal 1 risicofactor [12]. Oncologie is hierin geen risicofactor en er is geen Nederlandse studie gevonden naar PIM’s/POM’s en uitgebreide medicatiebeoordelingen in deze populatie. Studies naar de prevalentie van PIM’s en POM’s in oudere oncologiepatiënten hebben diverse beperkingen en de resultaten verschillen sterk [3-5,13-17].
Deze studie heeft als doel om de prevalentie PIM’s en POM’s in oudere oncologiepatiënten te bepalen. Secundaire doelen zijn subtypes PIM’s/POM’s vaststellen, vervolgacties op PIM’s/POM’s bepalen en risicofactoren voor PIM’s/POM’s onderzoeken.
Methoden
In deze prospectieve observationele studie zijn medicatiebeoordelingen uitgevoerd met patiënten ≥ 65 jaar, behandeld door een oncoloog/hematoloog met parenterale chemo- en/of immunotherapie. Patiënten zijn willekeurig benaderd op basis van geplande afspraken op de dagbehandeling.
Medicatieverificatie door een apotheker (i.o.) vond plaats tijdens een gesprek op de dagbehandeling, waarbij ook een vragenlijst voor onder andere gebruiksproblemen is doorlopen. Gebaseerd op het gesprek en het medisch dossier zijn PIM’s en POM’s geïdentificeerd met behulp van STOPP/START-criteria (2e herziene versie [18]) en expert opinion van de apotheker (onder andere interpretatie medicatiebewakingssignalen, praktische adviezen, naleving richtlijnen). Alle PIM’s/POM’s en bijbehorend advies zijn gecontroleerd door een ziekenhuisapotheker en na eventuele aanpassing (op basis van consensus) gecommuniceerd naar de oncoloog/hematoloog. Die besloot of een vervolgactie nodig was, met keuze uit vervolgactie door oncoloog/hematoloog zelf of het doorsturen van de PIM/POM en bijbehorend advies aan de huisarts.
De prevalentie PIM’s en POM’s (percentage patiënten met tenminste één PIM en/of POM) is gecombineerd en separaat bepaald. PIM’s/POM’s zijn nader geclassificeerd aan de hand van de Anatomische Therapeutische Chemische (ATC) code, de indeling uit de STOPP/START-criteria en de indeling uit de Systematic Tool to Reduce Inappropriate Prescribing (STRIP)-methode [12,18,19].
De volgende covariabelen zijn meegenomen: leeftijd, geslacht, aantal geneesmiddelen (thuis-, zelfzorg-, kuuren ondersteunende medicatie), polyfarmacie, wel/geen medicatierol, type kanker, behandeling wel/niet curatief in opzet en Charlson Comorbidity Index (CCI)-score [20]. Polyfarmacie is gedefinieerd als chronisch gebruik (≥ 3 maanden) van ≥ 5 verschillende geneesmiddelen, exclusief dermatica [12].
Mogelijke verschillen in covariabelen tussen patiënten met en zonder PIM’s/POM’s zijn getoetst (continue variabelen: Student-t-toets/Mann-Whitneytoets; categorische variabelen: chi-kwadraattoets/Fisher-exacttoets). Vervolgens is logistische regressie gebruikt om de mate van associatie (Odds Ratios [OR’s] en 95%-betrouwbaarheidsintervallen [95%-BI’s]) tussen de significant verschillende covariabelen en de prevalentie PIM’s/POM’s vast te stellen.
Deze studie is door de Medisch Ethische Toetsingscommissie beoordeeld als niet-WMO-plichtig. Patiënten gaven schriftelijke toestemming voor deelname.
Resultaten
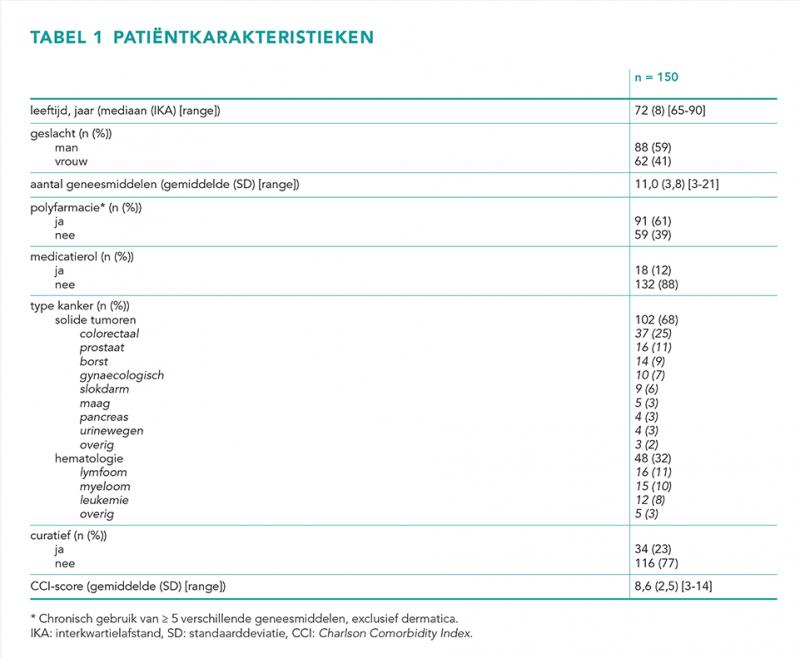
Er zijn 159 patiënten benaderd, waarvan 150 zijn geïncludeerd (4x geen deelname, 5x afspraak niet doorgegaan binnen onderzoeksperiode). Tabel 1 bevat de patiëntkarakteristieken.
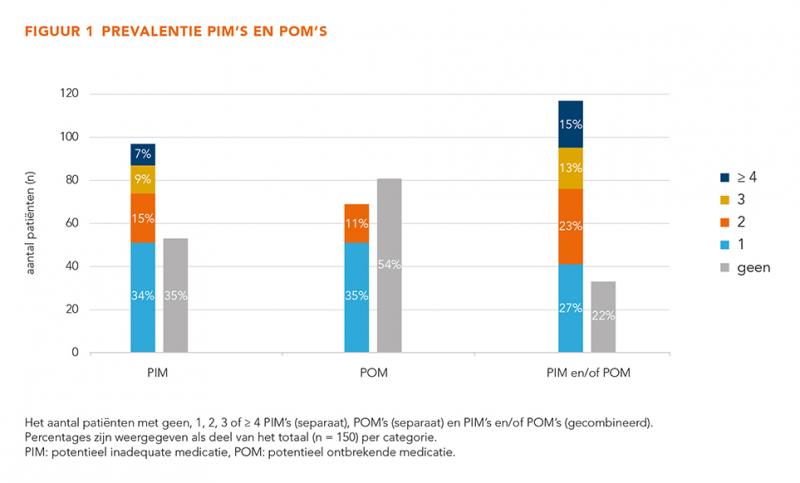
In totaal zijn 180 PIM’s en 86 POM’s geïdentificeerd met gemiddeld 1,8 PIM en/of POM per patiënt (range 0-8). De prevalentie PIM’s/POM’s gecombineerd was 78%, separaat was de prevalentie PIM’s 65% en POM’s 46% (figuur 1).
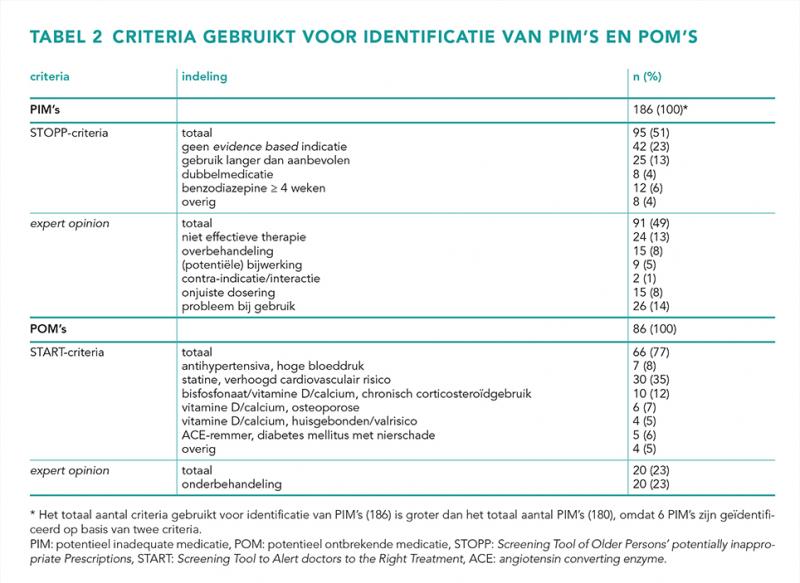
Van de 180 PIM’s betrof 19% protonpompremmers (PPI’s), 11% antihypertensiva, 9% benzodiazepine-agonisten en 8% analgetica. 4 PIM’s (2%) betroffen oncolytica. Van de 86 POM’s betrof 40% statines, 19% antihypertensiva en 15% vitamine D. Tabel 2 toont de criteria gebruikt voor identificatie van de PIM’s/POM’s.
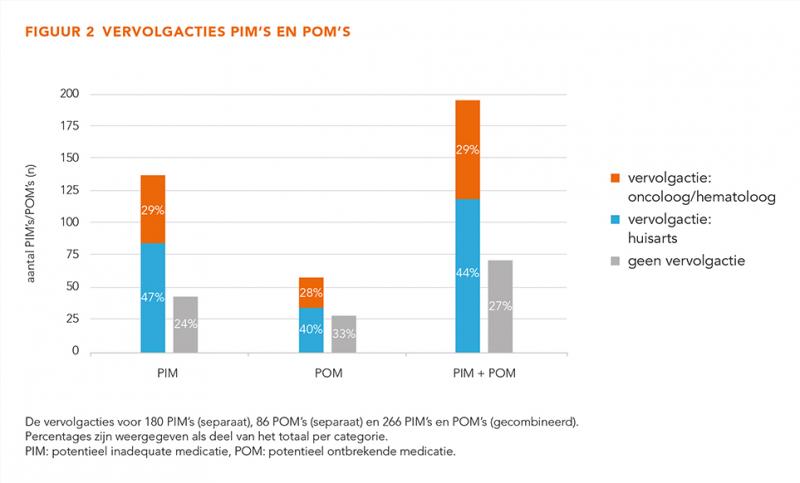
Voor 73% van de PIM’s en POM’s was een vervolgactie nodig (figuur 2). PIM’s kregen vaker een vervolgactie dan POM’s: 76% versus 67%. Van de vervolgacties is 39% door de oncoloog/hematoloog zelf uitgevoerd.
Vervolgacties door de oncoloog/hematoloog betroffen het vaakst PPI’s (PIM’s), antimicrobiële middelen (PIM’s), oncolytica (PIM’s), medicatie voor het bewegingsapparaat (PIM’s/POM’s) en vitamine D (POM’s).
Het doorsturen van de PIM/POM aan de huisarts betrof vaker alfa-adrenoreceptorantagonisten (PIM’s), respiratoire medicatie (PIM’s), antihypertensiva (PIM’s/POM’s) en statines (POM’s). Het percentage vervolgacties was hoog bij gebruik van STOPP-criterium ‘dubbelmedicatie’ en expert opinion ‘contra-indicatie/interactie’, ‘onjuiste dosering’ en ‘probleem bij gebruik’, respectievelijk 100%, 100%, 87% en 86%. Het percentage vervolgacties was het laagst bij START-criterium ‘statine bij verhoogd cardiovasculair risico’: geen vervolgactie bij 43% van de POM’s.
Meer geneesmiddelen (11,4 versus 9,8; P = 0,031) en een hogere CCI-score (8,9 versus 7,4; P = 0,002) zijn geassocieerd met het hebben van tenminste één PIM en/of POM. OR’s (95%-BI’s) voor het aantal geneesmiddelen en de CCI-score waren respectievelijk 1,125 (1,003-1,262) en 1,305 (1,094-1,556) (onafhankelijke associatie). Per toename van één geneesmiddel of één punt voor de CCI-score nam de kans op het hebben van tenminste één PIM en/of POM dus met respectievelijk 1,125 en 1,305 toe. De andere covariabelen zijn niet geassocieerd met de prevalentie PIM’s/POM’s.
Beschouwing
Een hoge prevalentie PIM’s en POM’s (gecombineerd 78%) is gevonden in oudere oncologiepatiënten door medicatiebeoordelingen uit te voeren op basis van STOPP/START-criteria en expert opinion van apothekers.
De gevonden prevalentie PIM’s is hoger dan in eerdere studies. Dit kan komen door een grondigere en completere aanpak voor de medicatiebeoordelingen. Allereerst is een uitgebreide medicatiebeoordeling met de patiënt uitgevoerd in plaats van het baseren van PIM’s op een medicatielijst uit het dossier. Daarnaast is de expert opinion van apothekers gebruikt als toevoeging op gestandaardiseerde criteria.
Studies zonder patiëntgesprek met enkel gestandaardiseerde criteria (Beers of STOPP) vonden een prevalentie PIM’s van 16-57% [5,13-16]. Van alle PIM’s in de huidige studie betreft 14% gebruiksproblemen, die vaak zijn geïdentificeerd op basis van het patiëntgesprek. Die PIM’s zijn gemist in de eerdere studies. Tevens draagt medicatieverificatie met de patiënt bij aan een completer medicatieoverzicht en zo mogelijk aan meer PIM’s. Reis et al. [17], Nightingale et al. [3] en Deliens et al. [4]vonden een prevalentie van respectievelijk 48%, 51% en 52% met wel een patiëntgesprek of uitgebreide medicatiebeoordeling. Niet alle PIM’s/POM’s zijn echter te identificeren met gestandaardiseerde criteria. Dit is duidelijk te zien in deze studie, waar de helft van de PIM’s en een kwart van de POM’s is geïdentificeerd op basis van expert opinion van apothekers. Dit leidt tot de hoge prevalentie PIM’s in deze studie.
Voor volledige optimalisatie moet naast inadequate medicatie ook ontbrekende medicatie worden aangepakt. Slechts 2 studies zijn gevonden waarin POM’s in oudere oncologiepatiënten zijn geïdentificeerd, met een prevalentie van 34% en 98% [4,5]. De hoge prevalentie gerapporteerd door Paksoy et al. [5] wordt bepaald door ontbrekende vaccinaties. Dit is niet van toepassing in Nederland: ouderen worden jaarlijks een influenzavaccin aangeboden en een pneumokokkenvaccin staat niet in de Nederlandse START-criteria [18].
De hoge prevalentie PIM’s op PPI’s en benzodiazepine-agonisten en POM’s op statines, antihypertensiva en vitamine D zijn in lijn met studies in oncologiepatiënten en niet-oncologiepatiënten [4,6,16,17,21,22]. Slechts 4 PIM’s betreffen oncolytica. De populatie in deze studie is dus niet heel afwijkend van andere oudere populaties en STOPP/START-criteria zijn goed toepasbaar.
Het meten van vervolgacties onderscheidt deze studie verder van eerdere studies. Daadwerkelijke medicatiewijzigingen, extra labaanvragen of acties door de huisarts zijn niet gemeten, wat kan leiden tot overschatting. Het percentage vervolgacties in deze studie (73%) komt echter overeen met eerdere studies, met vervolgacties bij 69-82% van de adviezen door apothekers [6,23,24]. Mogelijk kan dit in vervolgonderzoek verder in kaart worden gebracht. Voor alle STOPP/START-criteria geldt dat bij het grootste deel van de PIM’s/POM’s een vervolgactie nodig was. Hieruit blijkt dat de gehanteerde criteria relevant zijn voor deze patiëntenpopulatie.
Het aantal geneesmiddelen en de CCI-score zijn geassocieerd met de prevalentie PIM’s/POM’s, in lijn met een aantal eerdere studies [3,5,13]. OR’s zijn echter klein en er is geen specifieke (sub)groep patiënten aan te wijzen met de meeste baat bij een medicatiebeoordeling. Aangezien implementatie in de praktijk lastig kan zijn door de benodigde tijdsinvestering, kan vervolgonderzoek mogelijk uitwijzen welke patiënten(sub)groep hier de meeste baat bij heeft.
Sterke punten van deze studie zijn de combinatie van een uitgebreide medicatiebeoordeling en medicatieverificatie met de patiënt, de expert opinion van apothekers, identificatie van zowel PIM’s als POM’s en het meten van vervolgacties. Beperkingen zijn dat de studie één instelling betreft en dat enkel patiënten met parenterale oncologische therapie zijn geïncludeerd. Daarnaast is de prevalentie PIM’s/POM’s gemeten met directe vervolgacties, maar kan dit niet worden gerelateerd aan langetermijnuitkomsten voor patiënten en gezondheidszorg.
Conclusie
De prevalentie PIM’s en POM’s in oudere oncologiepatiënten is hoog. Uitgebreide medicatiebeoordelingen inclusief expert opinion van apothekers worden aanbevolen om PIM’s/POM’s te identificeren.
Verantwoording
De auteurs bedanken apothekers in opleiding Carlijn van der Velde en Marjolein Niewenhuijse voor hun bijdrage aan de medicatiebeoordelingen en dataverzameling.
Geen belangenverstrengeling gemeld.
Gebaseerd op het registratieonderzoek van F.M.A.M. van Loveren.
Dit artikel is ook gepubliceerd in Journal of Geriatric Oncology: van Loveren FMAM, van Berlo-van de Laar IRF, Imholz ALT, van ’t Riet E, Taxis K, Jansman FGA. Prevalence and follow-up of potentially inappropriate medication and potentially omitted medication in older patients with cancer - The PIM POM study. J Geriatr Oncol. 2021 Jan;12(1):80-84.
Informatie uit dit artikel is tevens gepubliceerd als: abstract 1825P, ESMO Congress 2019.
Literatuur
1. Hamaker ME, Jonker JM, de Rooij SE, Vos AG, Smorenburg CH, van Munster BC. Frailty screening methods for predicting outcome of a comprehensive geriatric assessment in elderly patients with cancer: a systematic review. Lancet Oncol. 2012 Oct;13(10):e437-44.
2. Sharma M, Loh KP, Nightingale G, Mohile SG, Holmes HM. Polypharmacy and potentially inappropriate medication use in geriatric oncology. J Geriatr Oncol. 2016 Sep;7(5):346-53.
3. Nightingale G, Hajjar E, Swartz K, Andrel-Sendecki J, Chapman A. Evaluation of a pharmacist-led medication assessment used to identify prevalence of and associations with polypharmacy and potentially inappropriate medication use among ambulatory senior adults with cancer. J Clin Oncol. 2015 May 1;33(13):1453-9.
4. Deliens C, Deliens G, Filleul O, et al. Drugs prescribed for patients hospitalized in a geriatric oncology unit: Potentially inappropriate medications and impact of a clinical pharmacist. J Geriatr Oncol. 2016 Nov;7(6):463-70.
5. Paksoy C, Özkan Ö, Ustaalioğlu BB, et al. Evaluation of potentially inappropriate medication utilization in elderly patients with cancer at outpatient oncology unit. J Oncol Pharm Pract. 2019 Sep;25(6):1321-1327.
6. Chau SH, Jansen AP, van de Ven PM, Hoogland P, Elders PJ, Hugtenburg JG. Clinical medication reviews in elderly patients with polypharmacy: a cross-sectional study on drug-related problems in the Netherlands. Int J Clin Pharm. 2016 Feb;38(1):46-53.
7. Tjia J, Velten SJ, Parsons C, Valluri S, Briesacher BA. Studies to reduce unnecessary medication use in frail older adults: a systematic review. Drugs Aging. 2013 May;30(5):285-307.
8. Patterson SM, Cadogan CA, Kerse N, et al. Interventions to improve the appropriate use of polypharmacy for older people. Cochrane Database Syst Rev. 2014 Oct 7;(10):CD008165.
9. Onder G, van der Cammen TJ, Petrovic M, Somers A, Rajkumar C. Strategies to reduce the risk of iatrogenic illness in complex older adults. Age Ageing. 2013 May;42(3):284-91.
10. Hill-Taylor B, Sketris I, Hayden J, Byrne S, O'Sullivan D, Christie R. Application of the STOPP/START criteria: a systematic review of the prevalence of potentially inappropriate prescribing in older adults, and evidence of clinical, humanistic and economic impact. J Clin Pharm Ther. 2013 Oct;38(5):360-72.
11. Verdoorn S, Kwint HF, Faber A, Gussekloo J, Bouvy ML. Majority of drug-related problems identified during medication review are not associated with STOPP/START criteria. Eur J Clin Pharmacol. 2015 Oct;71(10):1255-62.
12. Nederlands Huisartsen Genootschap. Multidisciplinaire richtlijn ‘Polyfarmacie bij ouderen’ 2012. Utrecht, 2012. 13. Prithviraj GK, Koroukian S, Margevicius S, Berger NA, Bagai R, Owusu C. Patient Characteristics Associated with Polypharmacy and Inappropriate Prescribing of Medications among Older Adults with Cancer. J Geriatr Oncol. 2012 Jul 1;3(3):228-237.
14. Feng X, Higa GM, Safarudin F, Sambamoorthi U, Tan X. Potentially inappropriate medication use and associated healthcare utilization and costs among older adults with colorectal, breast, and prostate cancers. J Geriatr Oncol. 2019 Sep;10(5):698-704.
15. Karuturi MS, Holmes HM, Lei X, et al. Potentially inappropriate medications defined by STOPP criteria in older patients with breast and colorectal cancer. J Geriatr Oncol. 2019 Sep;10(5):705-708.
16. Saarelainen LK, Turner JP, Shakib S, et al. Potentially inappropriate medication use in older people with cancer: prevalence and correlates. J Geriatr Oncol. 2014 Oct 1;5(4):439-46.
17. Reis CM, Dos Santos AG, de Jesus Souza P, Reis AMM. Factors associated with the use of potentially inappropriate medications by older adults with cancer. J Geriatr Oncol. 2017 Jul;8(4):303-307.
18. Knol W, Verduijn MM, Lelie-van der Zande AC, et al. Onjuist geneesmiddelgebruik bij ouderen opsporen: de herziene STOPP- en START-criteria. Ned Tijdschr Geneeskd. 2015;159:A8904.
19. WHO Collaborating Centre for Drug Statistics Methodology. ATC/DDD Index 2019 [internet]. https://www.whocc.no/atc_ddd_index/.
20. Charlson ME, Pompei P, Ales KL, MacKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chronic Dis. 1987;40(5):373-83.
21. Bo M, Gibello M, Brunetti E, et al. Prevalence and predictors of inappropriate prescribing according to the Screening Tool of Older People's Prescriptions and Screening Tool to Alert to Right Treatment version 2 criteria in older patients discharged from geriatric and internal medicine wards: A prospective observational multicenter study. Geriatr Gerontol Int. 2019 Jan;19(1):5-11.
22. Dalleur O, Spinewine A, Henrard S, Losseau C, Speybroeck N, Boland B. Inappropriate prescribing and related hospital admissions in frail older persons according to the STOPP and START criteria. Drugs Aging. 2012 Oct;29(10):829-37.
23. Krska J, Cromarty JA, Arris F, et al. Pharmacist-led medication review in patients over 65: a randomized, controlled trial in primary care. Age Ageing. 2001 May;30(3):205-11.
24. Gillespie U, Alassaad A, Henrohn D, et al. A comprehensive pharmacist intervention to reduce morbidity in patients 80 years or older: a randomized controlled trial. Arch Intern Med. 2009 May 11;169(9):894-900.
Referentie
Citeer als: van Loveren FMAM, van Berlo-van de Laar IRF, Imholz ALT, van ’t Riet E, Taxis K, Jansman FGA. De PIM POM studie: prevalentie van Potentieel Inadequate Medicatie en Potentieel Ontbrekende Medicatie in oudere oncologiepatiënten. Nederlands Platform voor Farmaceutisch Onderzoek. 2022;7:a1747.
DOI
https://www.knmp.nl/resolveuid/73302614d9fd4bb2a608421555fa3385Open access

Reactie toevoegen