Identificeren van micro-organismen bij aseptische handelingen
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2018;3:a1680
Kernpunten
- De toegevoegde waarde van routinematig identificeren van alle bij environmental monitoring (EM) gevonden micro-organismen bij aseptische handelingen is beperkt. Dit geldt ook voor het identificeren bij het overschrijden van alert- en actielimieten.
- Bij bouwactiviteiten in de nabijheid van een cleanroom is het belangrijk om op basis van prospectieve risico-inventarisatie gedurende een bepaalde periode de bij EM gevonden micro-organismen in de achtergrondruimte te identificeren en speciaal aandacht te schenken aan de aanwezigheid van schimmels.
Abstract
Identification of microorganisms in aseptic handling
OBJECTIVE
Determination of the relevance of identification of microorganisms found by microbiological Environmental Monitoring (isolates from EM) during aseptic handling.
METHODS
Identification of isolates from EM by microscopical examination, gram and spore staining and/or by MALDI-TOF. Isolates from EM in five hospital pharmacies were collected during one year and subdivided in 7 groups: Gram-positive and Gram-negative cocci, Gram-positive non-spore forming rods, Gram-positive spore forming rods, Gram-negative rods, fungi and yeast.
RESULTS
Gram-positive cocci were found in most cases (70-80 %), followed by Gram-positive rods (non-spore forming and spore forming; around 20%). Our results are comparable with the cleanroom microflora found in the pharmaceutical industry. The two cases described in this article, show that auditing gives more information about possible sources and causes of contamination than identification of micro-organisms.
CONCLUSION
The aim of identification is finding sources of contamination, resulting in corrective actions if EM results exceed the alert or action levels. We believe that the added value of identification, as a routine activity during aseptic handling is doubtful. However, knowing it is important to check if the cleanroom microflora is comparable to the expected microflora, we advise to do this once by using around 100 isolates from EM out of the LAF or biosafety cabinet and to repeat this every 3 years.
Identification is also valuable while building activities are taking place in the neighborhood of the cleanroom. Deviations from the expected cleanroom microflora will be indicative for inadequate preventive measures against contamination resulting from the building activities.
Inleiding
Om de kans op microbiologische contaminatie bij aseptische handelingen zo laag mogelijk te houden, worden een groot aantal voorzorgsmaatregelen getroffen [1]. Zo vinden deze handelingen plaats in een laminar air flow-kast (LAF-kast), veiligheidswerkbank (vwb) of isolator die in een cleanroom klasse D staat, gelden er kleding- en hygiënevoorschriften en wordt het personeel getraind in aseptisch werken. Om de effectiviteit hiervan te controleren wordt op regelmatige basis onderzocht hoeveel micro-organismen in de omgevingslucht, op oppervlakken en op de handschoenen (vingers) van de bereider voorkomen. Dit wordt microbiologische monitoring genoemd (environmental monitoring, EM).
Bij aseptische handelingen onder maximale productbescherming vindt EM in de LAF-kast of vwb dagelijks plaats [2]. De frequentie in de achtergrondruimte is lager en varieert van ziekenhuis tot ziekenhuis van eens per week tot eens per maand. Pas na geruime tijd wordt duidelijk wat het werkelijke contaminatieniveau is en kunnen alert- en actielimieten worden vastgesteld (alert: er is mogelijk wat aan de hand; actie: er is werkelijk wat aan de hand) [3].
Naast het bewaken van het aantal micro-organismen wordt ook geadviseerd om de bij EM geïsoleerde micro-organismen (isolaten) te identificeren. Hierdoor krijgt men een beeld van de verschillende soorten micro-organismen die in de productieomgeving voorkomen. Dit noemt men de huisflora. Identificeren is vooral van belang, zo wordt gesteld, om gericht te kunnen zoeken naar de bron in geval van overschrijding van alert- en/of actielimieten [4].
Identificatie van isolaten wordt niet genoemd in het hoofdstuk Aseptische Handelingen van de GMP-Z [1]. Richtlijnen elders lopen uiteen van alle isolaten identificeren [5], alleen isolaten van kritische plaatsen identificeren [6], tot alleen identificeren bij overschrijding van de actielimiet [7].
In dit artikel bespreken wij de rol van identificatie van de bij EM geïsoleerde micro-organismen bij het borgen van de kwaliteit van aseptische handelingen. Dit zal worden gedaan aan de hand van twee voorbeelden van ingezette acties naar aanleiding van een afwijkend patroon van de bij EM gevonden micro-organismen en op basis van de uitkomsten van onderzoek naar de huisflora in vijf Nederlandse ziekenhuisapotheken in zowel de werkruimte (LAF-kast of vwb) als in de achtergrondruimte.
Methoden
Identificatie als signaal
In dit artikel worden twee voorbeelden in ziekenhuisapotheken beschreven, waarbij een afwijkend patroon van de bij EM gevonden micro-organismen aanleiding was voor nader onderzoek.
Bepalen van de huisflora
Dit onderzoek is uitgevoerd in vijf ziekenhuisapotheken. EM wordt hier uitgevoerd volgens de LNA-procedures voor microbiologische monitoring [2]. Alle vijf de ziekenhuizen gebruikten trypticase soya agar-platen als groeimedium.
Na incubatie bij 30°C en aflezen na 7 dagen, zijn de gegroeide micro-organismen via microscopisch onderzoek en gramkleuring ingedeeld in grampositieve en gramnegatieve staven en coccen (bacteriën), schimmels en gisten. Bij grampositieve staven is sporenkleuring uitgevoerd of is via een massaspectroscopische identificatiemethode (MALDI-TOF) vastgesteld of er sprake is van een sporenvormer. Voor het bepalen van de huisflora zijn de resultaten van het identificeren over een periode van een jaar gebruikt. Een beschrijving van het bepalen van de huisflora staat op het NVZA-kennisplein en wordt te zijner tijd opgenomen in een LNA procedure [8]. Nota bene: anno 2018 bevat MALDI-TOF bijna altijd een databank met ook gegevens van micro-organismen uit de omgeving. In dat geval is microscopisch onderzoek en gramkleuring niet meer nodig en kan het bepalen van de huisflora volgens bovenstaande indeling volledig via MALDI-TOF worden uitgevoerd.
Resultaten
Identificatie als signaal
In beide ziekenhuisapotheken (casus A en B) worden de isolaten van EM niet routinematig geïdentificeerd. Schimmels vallen echter op bij het tellen van het aantal kolonievormende eenheden (kve) na incubatie.
Casus A: cleanroom radiofarmacie
Alle sedimentatieplaten bij luchtmonitoring van de achtergrondruimte bevatten vanaf een bepaald moment één of meer kve met schimmels, terwijl schimmels in het verleden sporadisch voorkwamen. In de werkruimte (vwb) was geen sprake van een verhoogde schimmelfrequentie op de sedimentatieplaten. De radiofarmacie achtergrondruimte (klasse D) heeft 15 Pa onderdruk ten opzichte van de omgeving.
Nader onderzoek leerde het volgende:
• in de kruipruimtes boven de cleanroom komen veel schimmels voor (Aspergillus). De schone kant van de HEPA-filters, voor de luchtinblaas, bevat geen schimmels. De schimmels komen dus niet via de luchtinblaas in de achtergrondruimte;
• de goederensluizen zijn niet schoon, ook daar zijn schimmels aangetoond;
• de achtergrondruimte vertoont technische gebreken: de muren bevatten meerdere kleine beschadigingen en niet alle kieren en naden zijn na eerder onderhoud goed gekit (onder andere rond de lichtbakken);
Maatregelen: tussendoor desinfecteren met een chloorhoudend desinfectans leverde geen verbetering op. Na herstel van de technische gebreken was het uitgangsniveau van sporadisch een schimmel weer bereikt. Verder onderzoek leerde dat op een behoorlijke afstand van de radiofarmacieruimtes gedurende acht maanden bouwactiviteiten hadden plaatsgevonden. Die activiteiten waren tijdens de zoektocht naar de bron van de schimmels alweer gestopt, maar zijn waarschijnlijk de oorzaak geweest van de verhoogde schimmelfrequentie op de sedimentatieplaten.
Geconcludeerd kan worden dat de combinatie van onderdruk en bouwkundige gebreken leidde tot lekken van lucht vanuit de omgeving naar de achtergrondruimte. Door de bouwactiviteiten was de schimmelconcentratie naar alle waarschijnlijkheid verhoogd en dit leidde weer tot een verhoogde schimmelfrequentie bij EM in de achtergrondruimte.
Casus B: cleanroom ziekenhuisapotheek
Het (platte) dak boven de bereidingsafdeling lekte. Er is direct actie ondernomen om dit te herstellen. EM-kweken uit de werkruimte van de datum van reparatie vertoonden schimmelgroei. Bij nader onderzoek bleek het lek zich te bevinden boven de overjassen in de gang. Deze jassen worden door de medewerkers bij het kortdurend verlaten van de bereidingsafdeling gedragen over de werkkleding. De daardoor besmette werkkleding heeft naar alle waarschijnlijkheid de schimmels in de achtergrondruimte en de werkruimte gebracht. Na reparatie van de lekkage duurde het nog circa vier weken voordat het aantal schimmels was gedaald tot de situatie voorheen (sporadisch schimmels op EM-monsters).
Bepalen van de huisflora
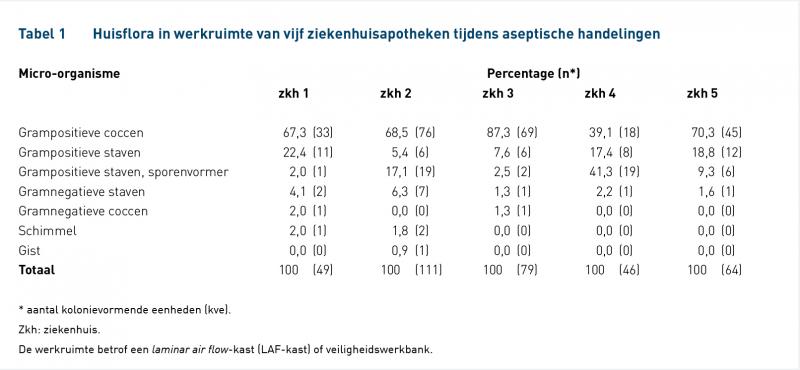
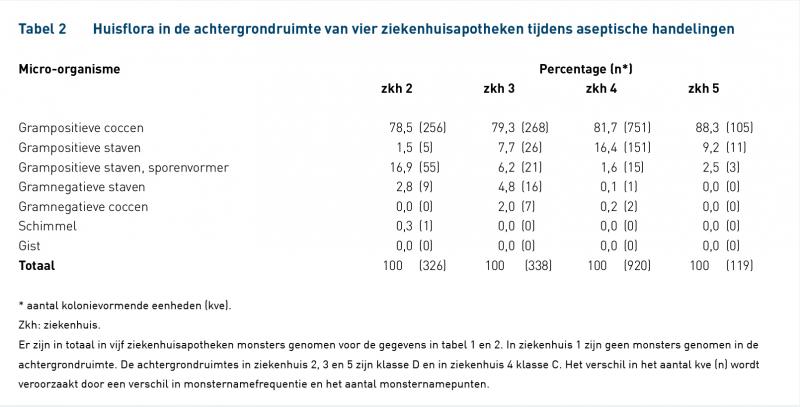
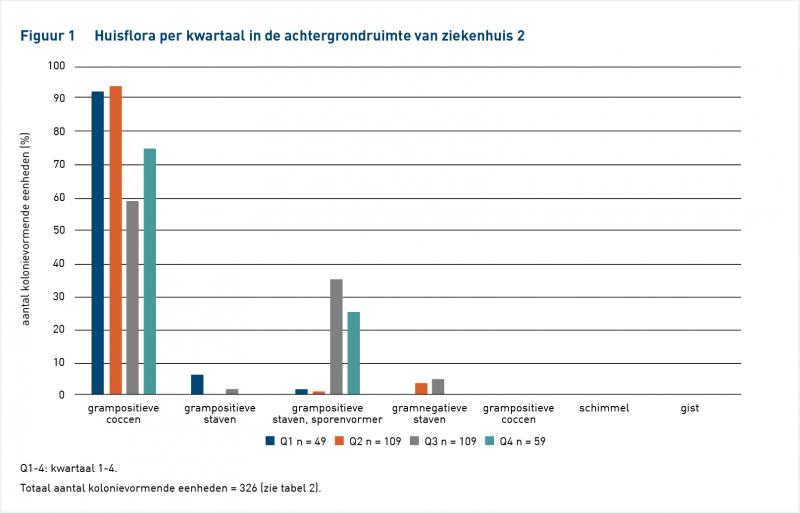
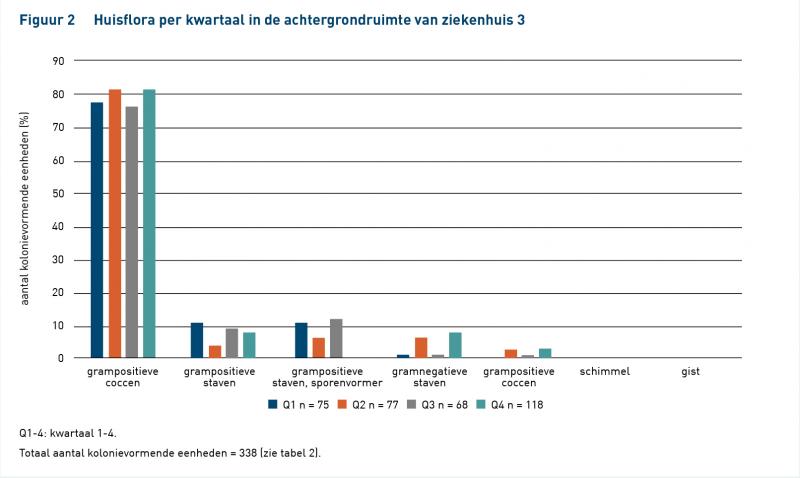
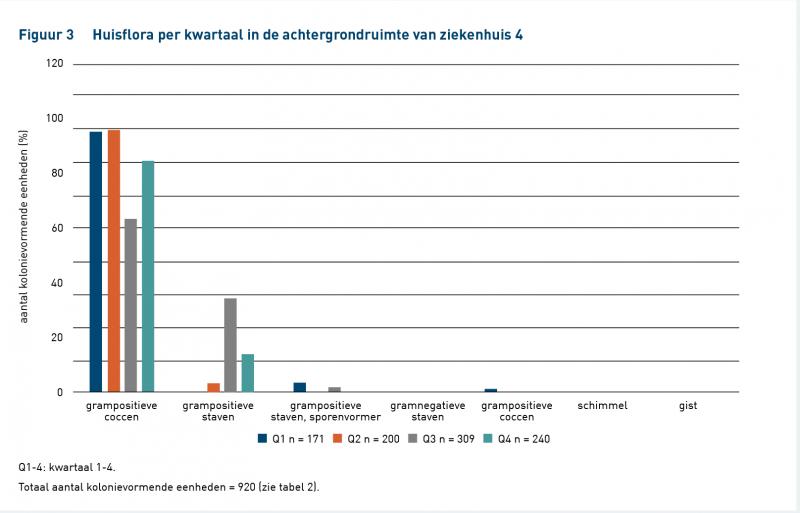
De resultaten van het identificeren van de bij EM gevonden micro-organismen uit de lucht, op de handschoenen en op werkbladen uit de werkruimte (LAF-kast of vwb) over een periode van 1 jaar uit vijf ziekenhuisapotheken staan in tabel 1. De resultaten van ziekenhuis 2 t/m 5 van het identificeren van de bij EM gevonden micro-organismen uit de lucht en op werkbladen in de achtergrondruimte over een periode van 1 jaar staan in tabel 2. Van ziekenhuis 1 zijn geen gegevens beschikbaar van de achtergrondruimte. Van de achtergrondruimten van ziekenhuizen 2, 3 en 4 zijn voldoende gegevens beschikbaar voor een verdere indeling per kwartaal; de resultaten staan in figuur 1, 2 en 3.
Beschouwing
Identificatie als signaal
Door het schimmelprobleem in casus A is men overgegaan tot inspectie van de ruimte en hierdoor zijn de bouwkundige gebreken geconstateerd. Het nut van identificeren lijkt hiermee aangetoond, maar de verhoogde frequentie van schimmels was naar alle waarschijnlijkheid niet voorgekomen als de bouwkundige staat van de achtergrondruimte beter was bewaakt. Bij voorbeelden in de literatuur waarbij sprake is van een afwijkend patroon van de huisflora, gaat het ook vaak om bouwkundige of technische gebreken waarop onvoldoende snel is gereageerd [9].
Bouwactiviteiten in de buurt van de cleanroom kan de huisflora beïnvloeden [10]. Er is sprake van verhoogde stofvorming wat leidt tot verhoogde aantallen micro-organismen in de lucht, met name schimmels. Bouwactiviteiten betekenen dan ook preventieve maatregelen treffen zoals effectieve afscherming (stofschotten), bereidingsactiviteiten en bouwactiviteiten zo nodig op elkaar afstemmen of bereidingsactiviteiten tijdelijk verplaatsen. Daarnaast is het van belang om tijdens bouwactiviteiten de frequentie van EM op te voeren en de bij EM gevonden kve te laten identificeren. Hiermee kan worden bewaakt of de getroffen maatregelen effectief zijn en wordt ook duidelijk wanneer de extra risico’s voorbij zijn.
Casus B is een voorbeeld van extra alert zijn bij een technisch gebrek. De huisflora was niet bekend, maar in verband met de lekkage was er wel verhoogde aandacht voor de resultaten van EM. Daardoor vielen de schimmels direct op. Achteraf bezien was het beter geweest als er na het constateren van de lekkage een prospectieve risico-inventarisatie was uitgevoerd. Het risico van besmetting via de jassen was dan wellicht eerder in beeld gekomen.
Bepalen van de huisflora
Onze bevindingen (tabel 1 en 2) sluiten aan bij elders gepubliceerde resultaten over het identificeren van isolaten uit cleanrooms [11, 12]. Grampositieve coccen en staven (tabel 1 en 2) zijn vooral afkomstig van de mens. Verpakkingsmateriaal (karton) kan relatief veel grampositieve staven bevatten. Gramnegatieve staven wijzen vooral op contaminatie door besmet water (vochtresten). Dit speelt bij aseptische handelingen in het algemeen geen rol. Schimmels (bron buitenomgeving) worden, zo blijkt uit tabel 1 en 2, effectief geweerd in de achtergrond- en werkruimte. Opmerkelijk is het hoge percentage sporenvormende bacteriën in de werkruimtes van ziekenhuis 4 (41,3 %), terwijl in dit ziekenhuis vrijwel geen sporenvormers in de achtergrondruimte zijn aangetroffen (tabel 2). Dit wijst er op dat ze via de materialen die bij de aseptische handelingen worden gebruikt, worden versleept tot in de werkruimte.
Sporenvormende bacteriën produceren zowel onder optimale als onder minder optimale leefomstandigheden sporen. Deze zijn resistent tegen veel desinfectantia, waaronder alcoholen. Toch leveren sporenvormers in de praktijk weinig problemen op bij aseptische handelingen. Dat komt enerzijds omdat ze grotendeels tijdens het schoonmaken en desinfecteren mechanisch worden verwijderd en anderzijds omdat sporenvormers vaak ook in de vegetatieve fase zitten [13]. In die fase worden ze wel gedood door alcoholen.
Uit de figuren 1, 2 en 3 blijkt dat het seizoen geen meetbare invloed heeft op de huisflora in de achtergrondruimte. Dat sluit aan bij bevindingen in de literatuur [11]. Voor het bepalen van de huisflora in de achtergrondruimte hoeft men dus geen rekening te houden met de tijd van het jaar.
Het aantal kve dat beschikbaar is voor het vaststellen van de huisflora hangt af van de frequentie van monitoren, het bemonsteringsschema en het aantal kve dat wordt gevonden. Bij dagelijkse EM van lucht, vingers en werkblad in de werkruimte (LAF-kast en vwb) worden circa 100 kve per jaar gevonden [14]. Deze 100 heeft men nodig om ook minder frequent voorkomende micro-organismen (< 10%) te kunnen opsporen.
Omdat in de werkruimte alles dat invloed kan hebben op het product samenkomt (denk ook aan de materialen: ampullen, injectie- en infusieflacons), is onderzoek naar de huisflora in deze ruimte het meest zinvol. Geadviseerd wordt dit onderzoek initieel, na ingebruikname van een nieuwe werkruimte (LAF-kast en vwb), uit te voeren en dit onderzoek periodiek te herhalen (bijvoorbeeld eens in de 3 jaar). Dit laatste omdat de huisflora geen statisch geheel is.
Mocht de gevonden huisflora duidelijk afwijken van het gebruikelijke patroon dan komt op basis van risico-inventarisatie nader onderzoek van het oppervlak van materialen eerder in aanmerking voor het opsporen van de bron, dan identificeren van isolaten van EM van de achtergrondruimte [15]. Als dit opnieuw onvoldoende informatie oplevert is nader onderzoek van andere omgevingsfactoren nodig. Naast oppervlakken en lucht (ook in de sluizen) moet dan ook gedacht worden aan kleding, schoeisel en persoonlijke hygiëne.
De toegevoegde waarde van routinematig identificeren, om daarmee eerder de bron van een eventuele besmetting te kunnen opsporen, lijkt bij aseptische handelingen beperkt. Er worden tientallen verschillende materialen in de werkruimte gebracht, allen met een andere herkomst. Ook werken er vaak 10 of meer verschillende personen, die allen een eigen microbiële flora meebrengen. Ook als men uitgebreider gaat identificeren, bijvoorbeeld tot op geslachts- of soortniveau, is bij dit brede aanbod van potentiële contaminatiebronnen de kans op het vinden van de juiste bron vrijwel uitgesloten. Zelfs in geval van het overschrijden van een actielimiet lijkt het nut van identificeren beperkt. Goed observeren van de werkwijze, waarbij de opslag en logistiek van de materialen niet mag worden vergeten, levert in het algemeen meer informatie op [16].
Bij groei in de bouillon bij validatie van de aseptische werkwijze wordt ook identificatie geadviseerd [17]. Ook hier moet de waarde van identificatie niet worden overschat en behoort dit een onderdeel te zijn van meer maatregelen [18].
Als alleen MALDI-TOF wordt toegepast bij het identificeren, wordt de uitslag weergegeven in geslachts- en soortnaam. Voor de evaluatie van de resultaten leidt deze gedetailleerde informatie niet direct tot meer inzicht in de huisflora. Geadviseerd wordt daarom om de uitslag van MALDI-TOF ook vast te leggen in de in dit artikel genoemde indeling.
Ten slotte dient men zich te realiseren dat identificeren geld kost (ca. € 5,00 per bepaling). Gezien de beperkte toegevoegde waarde van het identificeren is ook dit een reden voor terughoudendheid.
Conclusie
Het bewaken van de invloed van omgevingsfactoren door het bepalen van het aantal micro-organismen is het primaire doel van EM. Om te weten of de huisflora niet afwijkt van het patroon dat over het algemeen gevonden wordt in cleanrooms, verdient het aanbeveling deze initieel in de werkruimte (LAF-kast en vwb) te bepalen en dit onderzoek periodiek te herhalen (bijvoorbeeld eens per 3 jaar). De toegevoegde waarde van routinematig identificeren van alle bij EM gevonden micro-organismen bij aseptische handelingen is beperkt. Dit geldt ook voor identificeren bij het overschrijden van alert- en actielimieten.
Bij activiteiten of calamiteiten in de nabijheid van een cleanroom die invloed kunnen hebben op de huisflora, zoals bouwactiviteiten, is het belangrijk om een prospectieve risico-inventarisatie uit te voeren. Hiermee kan worden beoordeeld of gedurende een bepaalde periode de bij EM in de achtergrondruimte gevonden micro-organismen geïdentificeerd moeten worden.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Aseptische handelingen, Z3 versie 2013 GMP-ziekenhuisfarmacie [internet]. Nederlandse Vereniging van Ziekenhuisapothekers. Beschikbaar op: https://nvza-connect.nl/umbraco/bibliotheek/gmp-z/ [geraadpleegd oktober 2018].
2. Microbiologische monitoring bij aseptische handelingen [internet]. KNMP kennisbank. Beschikbaar op: https://kennisbank.knmp.nl/article/LNA-procedures_bereiding/intro.html [geraadpleegd oktober 2017].
3. Keijer WJ, van Doorne H, Boom FA. De handhaving van een ongewoon evenwicht. Pharm Weekbl. 2002;137:726-31.
4. Sandle T, Vijayakumar R. Cleanroom Microflora. In: Cleanroom microbiology. Parenteral Drug Association, Bethesda USA 2014.
5. The United States Pharmacopeia USP 35 (2012). The United States Pharmacopeial Convention. Rockville. <1116> Microbiological control and monitoring of aseptic processing environments: 697-707.
6. Pharmaceutical Inspection Convention. GMP Annex 1 revision 2008, interpretation of most important changes for the manufacture of sterile medicinal products. PI 032-2, Januari 2010.
7. Beaney AM. Quality assurance of aseptic preparation services: Standards. On behalf of the Royal Pharmaceutical Society and the NHS Pharmaceutical Quality Assurance Committee, 5th ed. Royal Pharmaceutical Society, UK 2016.
8. Boom FA, Veenbaas T. Onderzoek naar de huisflora bij aseptische handelingen [internet]. Beschikbaar op: https://nvza-connect.nl/umbraco/nieuws/onderzoek-huisflora-bij-aseptische-handelingen/ [geraadpleegd oktober 2018].
9. Van Antwerpen K. Presenting environmental monitoring data to internal and external stakeholders. In: Environmental monitoring, volume 5. Moldenhauder J ed. Parenteral Drug Association, Bethesda USA 2011.
10. Friedman RL. Aseptic processing contamination case studies and the pharmaceutical quality system. PDA J Pharm Sci Tech. 2005;59:118-126.
11. Pacheco FLC, Pinto TdJA. The bacterial diversity of pharmaceutical clean rooms analysed by fatty acid methyl ester technique. PDA J Pharm Sci Tech. 2010;64:156-166.
12. Sandle T. A review of cleanroom microflora: types, trends and patterns. PDA J Pharm Sci Tech. 2011;65:392-403.
13. Mehmi M, Marschall LJ, Lambert PA, Smith JC. Evaluation of disinfecting procedures for aseptic transfer in hospital pharmacy departments. J Pharm Sci Tech. 2009;63:12-138.
14. Nieuwsbrief Microbio [internet]. NVZA en KNMP; november 2016. Beschikbaar op: https://nvza-connect.nl/umbraco/media/2029/nieuwsbrief_microbio_november_2016.pdf [geraadpleegd oktober 2018].
15. Boom FA. Materialen in de LAF-kast en veiligheidswerkbank: welke risicoreductie is zinvol [internet]. Beschikbaar op: https://nvza-connect.nl/umbraco/media/2027/materialen_in_de_laf_kast_en_veiligheidswerkbank__welke_risicoreductie_is_zinvol__frits_boom.pdf [geraadpleegd oktober 2018].
16. Boom FA. Microbiologische monitoring bij aseptische handelingen: grenswaarden, alert en action levels [internet]. Beschikbaar op: https://nvza-connect.nl/umbraco/media/2028/microbiologische_monitoring_bij_aseptische_handelingen__grenswaarden__alert_en_action_levels__f_boom.pdf [geraadpleegd oktober 2018].
17. Technical report no. 13 (revised): fundamentals of an environmental monitoring program [internet]. Parenteral Drug Association; 2014. Beschikbaar op: https://store.pda.org/TableOfContents/TR13_TOC.pdf [geraadpleegd oktober 2017].
18. Boom FA, van Doorne H, Moes-ten Hove JE. Microbiologische validatie van aseptische handelingen: wat zijn de criteria. Pharm Weekbl. 2012;6(6):90-94.
Referentie
Citeer als: Boom FA, Veenbaas T, Crul M, Pavičić MJAMP, Ris JM. Identificeren van micro-organismen bij aseptische handelingen. Nederlands Platform voor Farmaceutisch Onderzoek. 2018;3:a1680.
DOI
https://www.knmp.nl/resolveuid/53eba7ca126744e28cd36c7f2ddb2c53Open access

Reactie toevoegen