Hogere dosis aminoglycosiden nodig in morbide obese patiënten: nieuwe doseeradviezen onderbouwd
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2023;8:a1763
Kernpunten
- In dit onderzoek bij zowel obese als niet-obese individuen mét en zonder nierfunctiestoornissen bleken gedeïndexeerde Modification of Diet in Renal Disease (MDRD) en Chronic Kidney Disease Epidemiology (CKD-EPI, in mL/min) de meest geschikte voorspellers voor respectievelijk de tobramycine- en gentamicineklaring.
- De bij obese patiënten veel toegepaste dosering op basis van adjusted body weight leidt met name bij een verminderde nierfunctie tot mogelijk toxische blootstellingen.
- Nieuwe doseeradviezen gebaseerd op lichaamsgewicht en nierfunctie resulteren in een vergelijkbare blootstelling in obese en niet-obese patiënten en mogelijk verminderde noodzaak voor aanpassing van de dosering via therapeutic drug monitoring.
Abstract
Higher aminoglycoside dosages needed in morbidly obese patients: novel evidence-based dose regimens
Background and objective
Gentamicin and tobramycin are renally cleared antibiotics of which the 24-hour exposure and trough concentration are known to correlate with efficacy and toxicity, respectively. Since there is no consensus on how to adjust the dose in obese individuals, we aimed to develop a dosing algorithm by investigating the pharmacokinetics of these drugs in obese and non-obese individuals with varying renal function.
Design and methods
In a prospective pharmacokinetic study, morbidly obese individuals undergoing bariatric surgery (n = 40) and nonobese healthy volunteers (n = 16), all with normal renal function, received an IV dose of gentamicin or tobramycin with subsequent 24-hour sampling. The influence of renal function was additionally investigated for gentamicin by addition of a retrospective therapeutic drug monitoring dataset from obese patients treated in two hospitals (n = 750). Modelling and simulations were performed using nonlinear mixed effects modelling.
Results
Prospectively included individuals had body weights up to 221 kg. The retrospective dataset contained patients with Chronic Kidney Disease Epidemiology (CKD-EPI) down to 5.1 mL/min/1.73 m2. In a two-compartment model, clearance of both drugs was larger in obese individuals, with de-indexed renal function estimates (in mL/ min) being most predictive for tobramycin (Modification of Diet in Renal Disease [MDRD]) and gentamicin (CKD-EPI) (p < 0.001 for both). Central volume of distribution increased with body weight (p < 0.001 for both). To ensure similar exposure in obese patients, dosing nomograms are proposed based on bodyweight and renal function, as dosing based on total (TBW) or adjusted body weight (ABW) alone might result in overexposure.
Conclusion
Current dosing practices using TBW or ABW may not be appropriate for obese individuals. In this pharmacokinetic study we provide novel evidence-based dosing nomograms for gentamicin and tobramycin for obese patients. The proposed nomograms may potentially reduce the need for dose adjustments after therapeutic drug monitoring, thereby improving the efficacy and safety of these drugs.
Registered in the Dutch Trial Registry (NTR6058).
Inleiding
De wereldwijde prevalentie van obesitas en morbide obesitas, gedefinieerd als een body mass index (BMI) boven 30 en 40 kg/m2 respectievelijk, neemt zeer snel toe [1]. Ook in Nederland is sprake van een hoge prevalentie, nu meer dan de helft van de volwassen Nederlandse bevolking een BMI heeft boven 25 kg/m2, waarbij in bijna 15% sprake is van ernstig overgewicht (BMI ≥ 30 kg/m2) [2].
Door fysiologische veranderingen ten gevolge van overgewicht kan de farmacokinetiek van geneesmiddelen veranderen [3,4], waardoor in veel gevallen de standaarddosering dient te worden aangepast. Intraveneuze antibiotica zoals gentamicine en tobramycine worden frequent toegepast bij ernstige infecties. In Nederland wordt traditioneel voor het effect veelal naar de piekspiegel (Cmax) ten opzichte van de minimale inhibitoire concentratie (MIC) van het micro-organisme gekeken [5,6], terwijl te hoge dalspiegels (Cmin) een verhoogd risico op ernstige (nier)toxiciteit geven [7-9]. Welke farmacodynamische target voor aminoglycosiden echter het beste correleert met het effect, is onderwerp van discussie waarbij steeds vaker de blootstelling aan aminoglycoside (gemeten als de 24-uurs oppervlakte onder de concentratie-tijdcurve [AUC0-24]) wordt genoemd als beste voorspeller [7,8,10,11].
Aminoglycosiden worden in de klinische praktijk gedoseerd op totaal lichaamsgewicht (TBW) met standaarddoseringen in mg/kg. Voor obese patiënten zijn de afgelopen decennia verschillende alternatieve doseerstrategieën voorgesteld, zoals het gebruik van adjusted body weight (ABW) of lean body weight (LBW) [12-17]. De meeste van deze onderzoeken hebben slechts een beperkte bewijskracht, onder meer vanwege het gebruik van verouderde definities van obesitas, het gebruik van (te) beperkte datasets, achterhaalde analysemethodes voor het meten van gentamicineconcentraties (via agar-diffusie methodes in plaats van immunoassays) of het ontbreken van relevante uitkomstmaten.
In dit onderzoek bestuderen we de farmacokinetiek van gentamicine en tobramycine in morbide obese en niet-obese individuen om vast te stellen hoe de klaring en verdeling veranderen bij obese individuen met en zonder nierfunctiestoornissen. Met de ontwikkelde farmacokinetische modellen worden doseeralgoritmes opgesteld met als doel om een voldoende hoge, maar niet toxische, blootstelling voor de gehele populatie van (morbide) obese patiënten te waarborgen.
Methoden
Studieopzet
Dit onderzoek bestond uit een prospectief en retrospectief deel. In de prospectieve farmacokinetische studies werden zowel morbide obese patiënten die een bariatrische operatie ondergingen (BMI > 35 kg/m2, n = 20 per geneesmiddel) als niet-obese gezonde vrijwilligers (BMI 18-25 kg/m2, n = 8 per geneesmiddel) geïncludeerd. Morbide obese patiënten kregen een enkele infusie gentamicine of tobramycine (beide 5 mg/kg LBW [18]) op de ochtend van de operatie, waarna tot 24 uur na het infuus serumconcentraties werden bepaald (11 metingen per individu). De niet-obese gezonde vrijwilligers ontvingen tevens een eenmalige infusie (5 mg/kg TBW) met hetzelfde bloedafnameschema. Exclusiecriteria waren onder andere een geschatte nierfunctie onder 60 mL/min/1,73 m2, bij niet-obesen berekend op basis van de Modification of Diet in Renal Disease (MDRD)-formule, bij obese patiënten op basis van de Cockcroft-Gault (CG)-formule met LBW als gewichtsmaat [19].
Naast de standaard demografische kenmerken werd vooraf aan de toediening van studiemedicatie het serumcreatinine gemeten. De glomerulaire filtratiesnelheid (GFR) werd gemeten op basis van een 24-uurs urineverzameling en tevens geschat op basis van het serumcreatinine met behulp van de CG (in mL/min, met LBW als gewichtsmaat voor obese individuen [19]), MDRD [20] en Chronic Kidney Disease Epidemiology (CKD-EPI) [21] (in mL/min/1,73 m2). Gedeïndexeerde MDRD en CKD-EPI (in mL/min) werden berekend door vermenigvuldiging met het lichaamsoppervlak (body surface area [BSA])/1,73.
Dit door ZonMw gesubsidieerde onderzoek werd goedgekeurd bij de lokale Medisch Ethische Toetsingscommissie (Medical Research Ethics Committees United, MEC-U, Nieuwegein) en staat geregistreerd in het Nederlands Trial Register (NTR6058). Alle deelnemers tekenden vooraf aan deelname informed consent.
Om de invloed van ziekte en nierfunctie in obese patiënten te kunnen karakteriseren, is voor gentamicine de prospectief verzamelde data gecombineerd met patiëntdata op basis van therapeutic drug monitoring (TDM) afkomstig uit twee grote Nederlandse ziekenhuizen (het St. Antonius Ziekenhuis [SAZ] in Nieuwegein/Utrecht en het Spaarne Gasthuis [SG] in Haarlem). Een dergelijke retrospectieve dataset was voor tobramycine helaas niet beschikbaar. In beide ziekenhuizen werd TDM in de vorm van piek-, dal- en/of halverwege spiegels als standaardzorg uitgevoerd bij iedere behandeling met gentamicine [5]. Alle patiënten met een BMI ≥ 25 mg/m2 die in de periode oktober 2017-april 2019 (SAZ) of januari 2013-december 2018 (SG) ten minste één gift gentamicine hadden gekregen, en waarbij tenminste één gentamicinespiegel en één serumcreatinine was bepaald, kwamen in aanmerking voor inclusie. Patiënten werden geëxcludeerd wanneer er geen lichaamsgewicht van maximaal 6 maanden oud bekend was, of wanneer sprake was van nierfunctievervangende therapie.
Spiegelbepalingen
Gentamicine- en tobramycineconcentraties van de prospectieve studie en het SAZ werden bepaald middels commercieel verkrijgbare, gevalideerde immunoassay methodes (Roche Diagnostics GmbH). De kwantificatielimieten (lower limit of quantification, LLOQ) waren 0,4 mg/L (gentamicine) en 0,3 mg/L (tobramycine). TDM gentamicinespiegels uit het SG werden gemeten met een commercieel verkrijgbare, gevalideerde immunoassay (Abbott Laboratories Ltd), met een LLOQ van 0,5 mg/L.
Farmacokinetische analyse
Concentratie-tijddata werden geanalyseerd met behulp van nonlinear mixed effects modelling-software ([NON-MEM], ICON Development Solutions, Hanover, USA). In het geval van gentamicine werd de populatiefarmacokinetiek geanalyseerd met behulp van de prospectieve data in combinatie met de retrospectieve TDM-data uit het SAZ (de trainingsdataset). Voor tobramycine was alleen prospectieve data in gezonde non-obese en obese vrijwilligers beschikbaar.
In de covariaatanalyse werd de invloed van verschillende patiëntkarakteristieken (TBW, LBW, ABW, GFR, [gedeïndexeerde] MDRD en [gedeïndexeerde] CKD-EPI, CG, leeftijd, geslacht en, in het geval van gentamicine, verblijf op een intensive care [IC]) op farmacokinetische parameters onderzocht. Onderscheid tussen modellen werd gemaakt op basis van de objective function value (OFV), waarbij een verschil van 3,84 punten (overeenkomend met een p-waarde van < 0,05) als statistisch significant werd beschouwd. Daarnaast werden modellen geëvalueerd op basis van goodness-of-fit plots (GOF). De farmacokinetische modellen werden intern gevalideerd middels bootstrap resampling en de visual predictive check (VPC).
Voor gentamicine werd een externe validatie uitgevoerd met behulp van de TDM-data uit het SG (validatiedataset). Validaties vonden plaats met behulp van VPC, beoordeling van de GOF en door berekening van de mediane voorspellingsfout (median prediction error [MPE]) en de relatieve kwadratische gemiddelde fout (relative root mean square error [rRMSE]).
Analyse van verschillende doseerregimes
Voor het ontwikkelen van een doseeradvies werden op basis van het finale geneesmiddelspecifieke model simulaties uitgevoerd van een eenmalige gift gentamicine of tobramycine in 30 minuten volgens verschillende doseerstrategieën op basis van gewichtsmaten (TBW, ABW) en/of nierfunctie. Simulatiedatasets bestonden uit 10.000 virtuele individuen per doseerregime, met gewicht uniform verdeeld tussen 55-200 kg. Elke patiënt werd een willekeurig geschatte nierfunctie (op basis van CKD-EPI of MDRD) toegewezen, met als uiterste waardes 5-140 en 50-125 mL/min/1,73 m2 voor respectievelijk gentamicine en tobramycine, in lijn met de originele datasets. Om voor het lichaamsgewicht realistische waarden voor ABW of LBW te verkrijgen, werd een naar lichaamsgewicht gestratificeerde extractie uit de National Health and Nutrition Examination Survey (NHANES)-database uitgevoerd [22]. Deze database bevat demografische data uit een groot retrospectief cohort uit de Verenigde Staten (1999-2016). Voor iedere patiënt werd de blootstelling bepaald op basis van de AUC in de eerste 24 uur (AUC0-24), waarbij voor de obese individuen werd gestreefd naar een AUC0-24 vergelijkbaar met niet-obesen, niet opgenomen op een IC, die een standaarddosis van 6 mg/kg TBW kregen. Hiervoor werd een 80-125% marge gehanteerd, zoals gebruikelijk is voor bio-equivalentie studies. Als secundaire eindpunten werden de Cmax en Cmin geanalyseerd, waarbij Cmin werd gedefinieerd als de concentratie vlak voor de tweede gift. Voor de Cmax, gedefinieerd als de aminoglycoside concentratie 60 minuten na start van het infuus. werd als doelconcentratie 15-20 mg genomen in lijn met de Nederlandse TDM-monografie [5].
Resultaten
Deelnemers
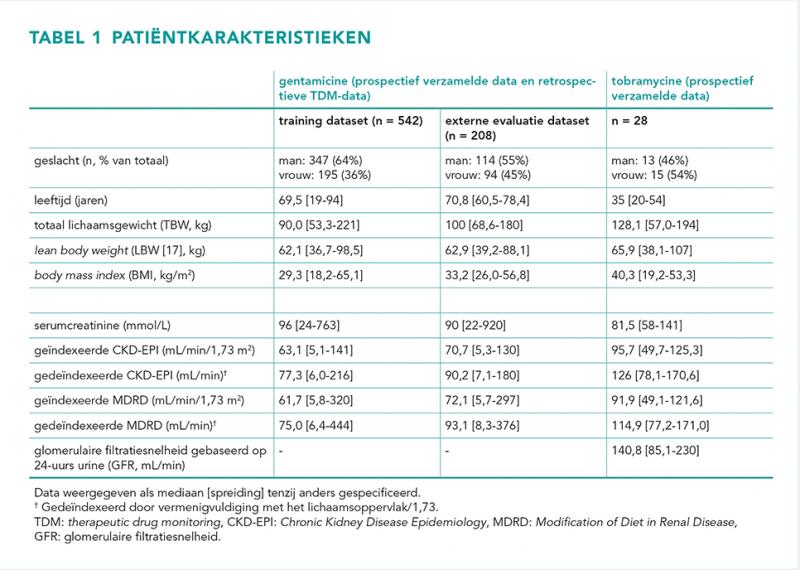
In totaal werden 40 morbide obese en 16 niet-obese individuen geïncludeerd in de prospectieve studie. De gentamicine trainingsdataset, bestaande uit de deelnemers aan de prospectieve studie aangevuld met TDM-data van patiënten uit het SAZ, bestond uit 1187 gentamicinebepalingen bij 542 individuen met mediaan lichaamsgewicht 90,0 kg (spreiding 53,3-221 kg). De gentamicine validatiedataset met TDM-data uit het SG bestond uit een vergelijkbare populatie van 208 patiënten (321 gentamicinebepalingen) met een mediaan lichaamsgewicht van 100 kg (spreiding 68,6-180 kg). De tobramycine dataset bestond uit 280 geneesmiddelspiegels van individuen met een mediaan lichaamsgewicht van 128 kg (spreiding 57,0-194 kg). Een overzicht van de belangrijkste karakteristieken zijn weergegeven in tabel 1.
Populatiefarmacokinetiek
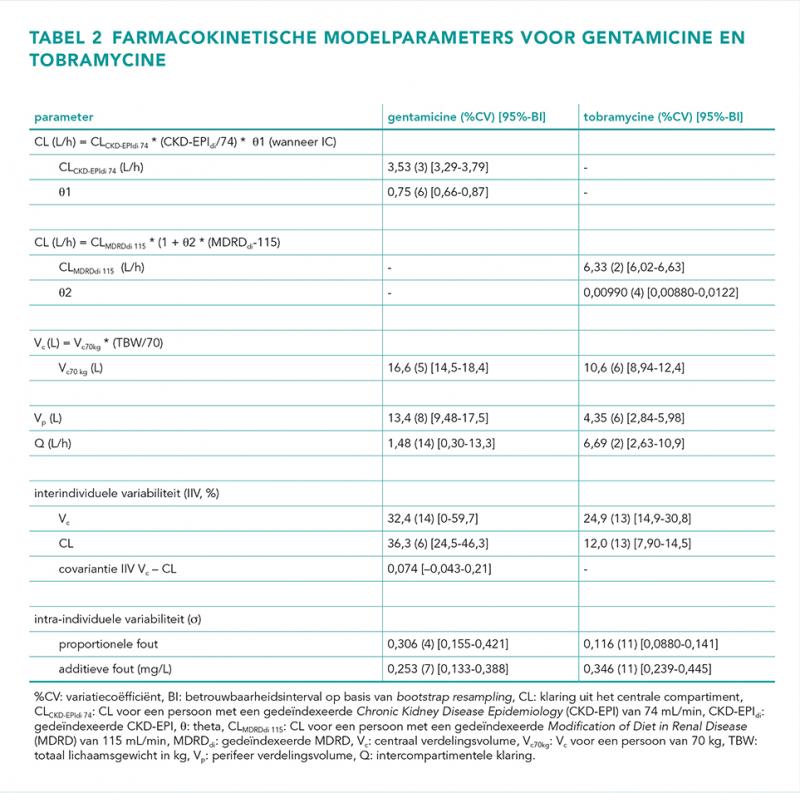
Voor beide aminoglycosiden werd de data het beste beschreven met een tweecompartimentenmodel met interindividuele variabiliteit op centraal distributievolume en klaring. Bij beide aminoglycosiden bleek centraal verdelingsvolume (Vc) goed te worden voorspeld met TBW (p < 0,001) volgens een lineaire vergelijking: Vc (L) = TVVc * (TBW/70), waarbij TVVc de typische Vc is voor een individu van 70 kg, namelijk 16,6 L (gentamicine) en 10,6 L (tobramycine). Gentamicineklaring kon het beste worden voorspeld middels gedeïndexeerde CKD-EPI (OFV daling van –807 punten, p < 0,001) met ook goede resultaten voor gedeïndexeerde MDRD (OFV daling van –723 punten, p < 0,001). Na inclusie van gedeïndexeerde CKD-EPI bleken patiënten die zijn opgenomen op de IC een 25% lagere klaring te hebben (95%-betrouwbaarheidsinterval 13-34%) (OFV daling –20,7 punten, p < 0,001) ten opzichte van patiënten die niet op een IC lagen. De tobramycineklaring bleek het sterkste te correleren met gedeïndexeerde MDRD, gedeïndexeerde CKD-EPI of GFR, met OFV-dalingen van –36,3, –32,8 en –32,3 punten (allen p < 0,001) respectievelijk. Omdat MDRD een betere visuele diagnostiek (GOF) had, kozen we voor gedeïndexeerde MDRD als covariaat op tobramycineklaring in het uiteindelijke model. De VPC’s bevestigden de accuraatheid van beide modellen (niet getoond). De bootstrap analyse bevestigde de robuustheid en stabiliteit van de farmacokinetische modellen (tabel 1). De externe validatie van gentamicine op basis van de TDM-dataset uit het SG liet op basis van GOF en VPC (niet getoond) een goede beschrijving zien van de externe data, zonder bias (MPE –0,39 mg/L), maar met enige precisie (rRMSE 76,6%). Deze imprecisie werd voornamelijk gedreven door hoge (top) gentamicinespiegels, aangezien de rRMSE reduceerde naar 46,3% wanneer deze werd berekend met concentraties < 5 mg/L. De parameters van de gentamicine- en tobramycinemodellen zijn weergegeven in tabel 2.
Analyse van verschillende doseerregimes
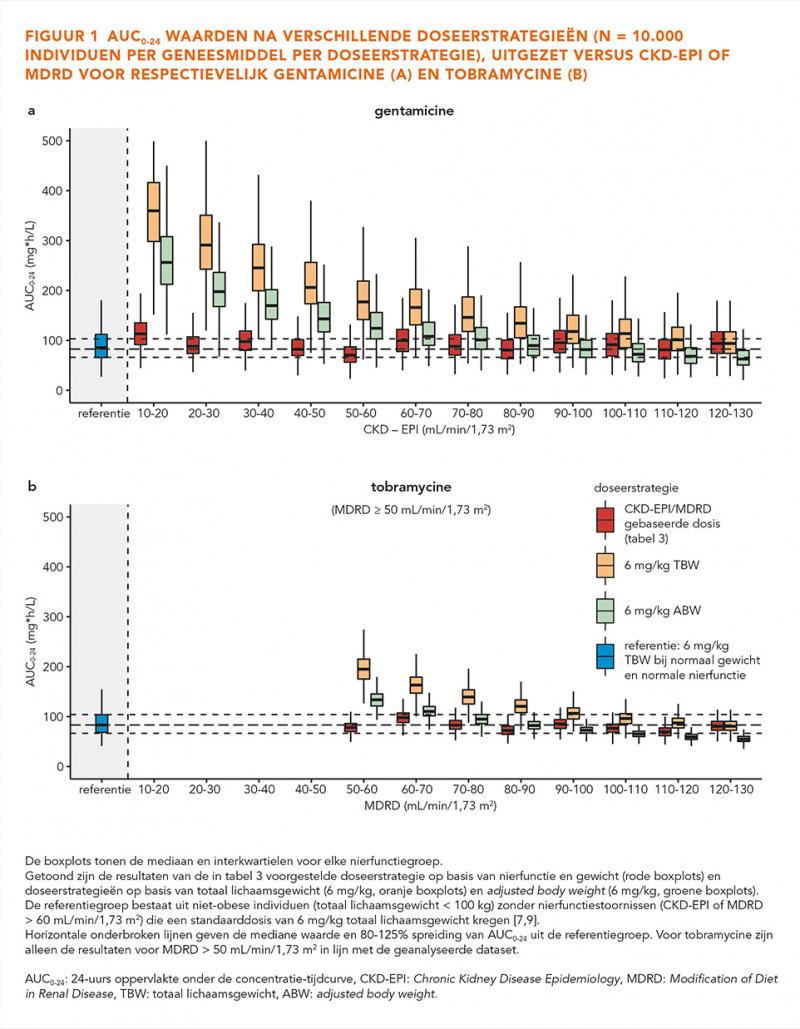
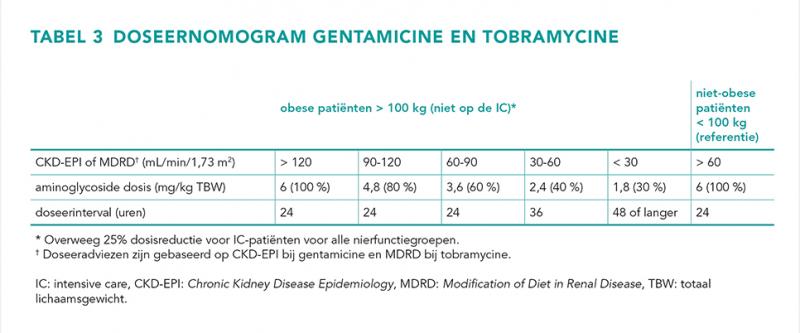
Figuur 1 laat boxplots met medianen en interkwartielen voor de AUC0-24 zien in individuen met lichaamsgewicht tussen 55,0-200 kg voor gentamicine en tobramycine na verschillende doseerstrategieën (n = 10.000 per geneesmiddel per dosering). Naast de gangbare doseerstrategieën op TBW of ABW is tevens een nieuw doseeralgoritme zoals getoond in tabel 3 onderzocht. Dit algoritme is gebaseerd op lichaamsgewicht (mg/kg) met een reductie bij een verlaagde nierfunctie (rode boxplots), waarbij de dosis varieert van 6 mg/kg voor obese patiënten met een MDRD of CKD-EPI > 120 mL/min/1,73 m2 tot 1,8 mg/kg voor patiënten met een MDRD of CKD-EPI < 30 mL/min/1,73 m2.
In figuur 1a is zichtbaar dat met variërende nierfuncties (CKD-EPI tussen 10 en 130 mL/ min) deze doseerstrategie leidt tot een vergelijkbare blootstelling in de eerste 24 uur in obese individuen in vergelijking met de referentiegroep van niet-obesen met een normale nierfunctie die 6 mg/kg TBW krijgen. Tegelijkertijd leiden de TBW- en ABW-gebaseerde doseerstrategieën tot een toename in blootstelling bij afnemende nierfunctie. Figuur 1b toont vergelijkbare resultaten voor tobramycine. Hoewel voor tobramycine alleen simulaties zijn uitgevoerd voor obese individuen met een goede nierfunctie op basis van de oorspronkelijke inclusiecriteria van deze studie, is ook hier reeds bij een MDRD tussen 50-80 mL/min/1,73 m2 zichtbaar dat een afnemende nierfunctie bij TBW- en ABW-gebaseerde doseerstrategieën leidt tot een toename in blootstelling.
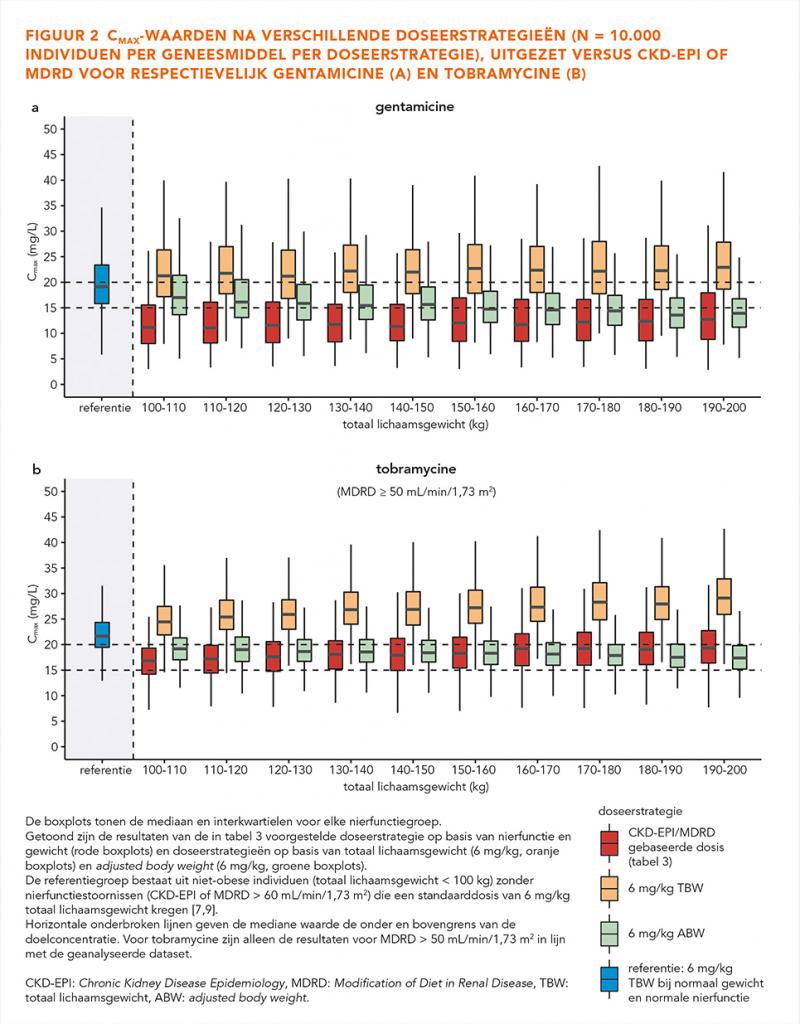
Figuur 2 toont de topspiegels of Cmax-waarden bij de verschillende doseerstrategieën. Hier is te zien dat de voorgestelde doseerstrategie uit tabel 3 bij verminderde nierfuncties < 60 mL/min/1,73 m2 leidt tot verlaagde Cmax bij deze patiënten, ondanks vergelijkbare totale blootstelling (AUC0-24, figuur 1).
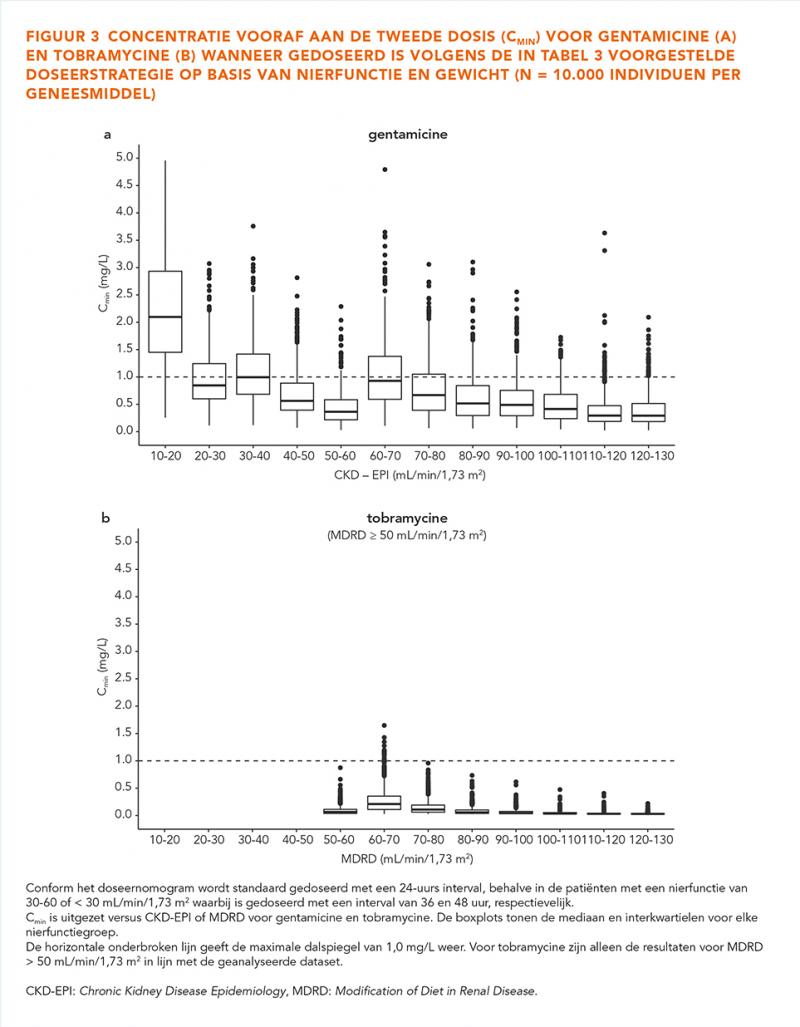
Figuur 3 toont voor dezelfde patiënten als getoond in figuren 1 en 2 de Cmin, vlak voor de vervolggift op basis van de voorgestelde doseerstrategie (tabel 3). Het overgrote deel van de patiënten heeft een gentamicine Cmin onder de streefwaarde van 1 mg/L (figuur 3a). Uitzondering hierop is de groep patiënten met ernstige nierfunctiestoornissen (10-20 mL/min/1,73 m2), waarbij het overgrote deel een Cmin boven de 1 mg/L heeft 48 uur na de gift gentamicine. Voor tobramycine geldt dat alle patiënten een Cmin < 1 mg/L, waarbij een belangrijke kanttekening is dat in deze groep alleen patiënten met een MDRD > 50 mL/min/1,73 m2 zijn gesimuleerd in lijn met de originele dataset.
Beschouwing
In dit onderzoek hebben we de invloed van obesitas op de farmacokinetiek van gentamicine en tobramycine bestudeerd bij obese en niet-obese mensen met lichaamsgewichten tot 221 kg. Hieruit blijkt dat de klaring van deze middelen in obese individuen het beste kan worden voorspeld door gebruik te maken van de geschatte nierfunctie op basis van CKD-EPI of MDRD, uitgedrukt in mL/min na vermenigvuldiging met de individuele BSA/1,73.
De op dit moment bij obese patiënten veel toegepaste dosering op basis van ABW leidt met name bij een verminderde nierfunctie tot zeer hoge, mogelijk toxische blootstellingen. Bovendien wordt ABW verschillend berekend voor mannen en vrouwen, waardoor een ongewenst verschil in dosering tussen mannen en vrouwen wordt geïntroduceerd.
Op basis van deze resultaten laten we zien dat voor een vergelijkbare blootstelling bij obese patiënten de standaarddosering op een andere manier moet worden aangepast. Hiertoe hebben we een doseernomogram opgesteld dat rekening houdt met het lichaamsgewicht en de geschatte nierfunctie (tabel 3). Dit nomogram is in eerste instantie opgesteld en geëvalueerd voor gentamicine (figuur 1a), maar geeft ook goede resultaten voor tobramycine bij patiënten met een goede nierfunctie (figuur 1b). Mogelijk kan dit nomogram ook bij tobramycine gebruikt worden in de populatie van obese patiënten met nierfunctiestoornissen. Dit is vooralsnog echter niet met zekerheid vast te stellen aangezien in onze studie patiënten met nierfunctiestoornissen ontbraken in de tobramycine-groep.
Het voorgestelde doseernomogram streeft zoveel mogelijk een vergelijkbare blootstelling (AUC0-24) tussen de obese en niet-obese individuen na. Hoewel traditioneel een adequate piekspiegel (Cmax) wordt gezien als belangrijkste voorspeller van het antibiotische effect van aminoglycosiden [5,6], is er veel discussie of de AUC0-24 niet beter zou correleren met het effect [10,11]. In preklinische modellen lijkt de AUC0-24 namelijk vaak een sterkere voorspeller voor antibiotisch effect [8]. In latere klinische humane studies zijn de resultaten minder eenduidig [23-26]. Een veel aangehaalde studie die concludeerde dat de piekspiegel voorspellend is voor het effect van aminoglycosiden, rapporteerde echter geen resultaten voor de AUC0-24 [24]. Inmiddels lijken experts en wetenschappelijke organisaties wereldwijd steeds vaker de AUC0-24 als drijvende indicator voor het effect te adviseren [7,8,10]. Om deze reden hebben we in de huidige studie een doseernomogram opgesteld dat zoveel mogelijk in een vergelijkbare AUC0-24 resulteert in de verschillende groepen. Wel wijzen we erop dat door de dosisreductie bij verminderde nierfunctie het nomogram wel tot lagere piekspiegels leidt bij obese patiënten (figuur 2). Indien een vergelijkbare piekspiegel in obese en non-obese patiënten gewenst is, kan worden gekozen voor dosering gebaseerd op TBW of ABW, hoewel dit zal leiden tot een hogere AUC (figuur 1) met naar verwachting ook hogere, toxische dalspiegels (niet getoond). Een kanttekening bij het voorgestelde nomogram is dat, hoewel het leidt tot een effectieve en niet-toxische bloostelling in alle obese patiënten, we in sommige individuen nog wel dalspiegels > 1 mg/L vonden, met name bij ernstige nierfunctiestoornissen. Dit onderstreept het belang van TDM al na de eerste gift, in het bijzonder bij deze patiëntengroep zodat in die gevallen het doseerinterval kan worden verlengd.
Sterke punten van ons onderzoek zijn de grote spreiding in lichaamsgewichten in de dataset, inclusief niet-obese en obese deelnemers tot 221 kg en de rijke dataset door de prospectieve onderzoeksopzet met frequente bloedafnames tot 24 uur na infusie. Wel dient te worden opgemerkt dat de obese patiënten in de prospectieve studie een bariatrische operatie ondergingen tegelijk met de studie, wat in theorie de farmacokinetiek kan beïnvloeden. Omdat deze laparoscopische operaties van zeer korte duur zijn, met daarbij een minimaal bloedverlies en nauwkeurige controle van de hemodynamiek, is deze mogelijke invloed waarschijnlijk verwaarloosbaar. Wel is terughoudendheid belangrijk bij het extrapoleren van onze resultaten naar niet onderzochte populaties, zoals obese patiënten met een lichaamsgewicht van meer 221 kg of in het geval van tobramycine naar patiënten met nierfunctiestoornissen. Ook is niet bekend in hoeverre het doseernomogram kan worden toegepast bij endocarditis, waar gentamicine in een lagere dosering wordt gegeven in synergie met β-lactam antibiotica. Een ander sterk punt van onze studie is het gebruik van een modeleer- en simulatie methode, inclusief een externe validatie in het geval van gentamicine, die tegenwoordig wordt gezien als de gouden standaard door veel geneesmiddelautoriteiten voor de goedkeuring van nieuwe geneesmiddeldoseringen [27]. Ook hebben we voor gentamicine de invloed van zowel lichaamsgewicht als de nierfunctie in de obese populatie tegelijkertijd kunnen onderzoeken door de prospectieve dataset te combineren met retrospectieve data op basis van TDM-data uit verschillende ziekenhuizen.
De invloed van obesitas op de farmacokinetiek van aminoglycosiden is onderzocht in diverse onderzoeken gedurende de afgelopen decennia [12-17]. Hoewel deze onderzoeken over het algemeen een toename in klaring met toenemend lichaamsgewicht rapporteerden, ontbrak adequate kwantificatie van de invloed van gewicht en nierfunctie die noodzakelijk zijn voor het ontwikkelen voor concrete doseeradviezen. Bovendien zijn veel van de resultaten tegenstrijdig, waarbij sommige onderzoeken (een biomarker voor) de nierfunctie als beste voorspeller voor de geneesmiddelklaring vonden [16], terwijl andere juist gewichtsmaten zoals TBW of ABW als covariaat vinden [13,14]. Daarnaast is bij de interpretatie van deze historische onderzoeken enige reserve op zijn plaats. Bij veel (relatief oude) onderzoeken hadden veel deelnemers door het gebruik van een verouderde definitie van obesitas slechts matig overgewicht [13,14,17] of werden aminoglycosideconcentraties gemeten met inmiddels verouderde analysemethodes, namelijk via agar-diffusie methodes in plaats van immunoassays. Tot slot werden analyses in de meeste studies gedaan op basis van schaarse data, veelal verzameld op basis van alleen TDM-data [12-14,16,17]. Hoewel in essentie met een dergelijke onderzoeksopzet waardevolle informatie kan worden verkregen, beperkt dit wel de mogelijkheid om de geneesmiddelklaring precies te schatten [28].
Uit onze analyse blijkt dat het verdelingsvolume correleert met lichaamsgewicht. Een interessant gegeven hierbij is dat aminoglycosiden worden beschouwd als hydrofiel (gentamicine log P –3,1, tobramycine log P –5,8 [29]). Deze resultaten bestrijden dus de veel herhaalde aanname dat bij obese patiënten slechts beperkte veranderingen in distributievolume kunnen worden verwacht bij hydrofiele geneesmiddelen. We kunnen concluderen dat vetoplosbaarheid alleen geen goede voorspeller is van veranderingen in distributievolume bij toenemend lichaamsgewicht, zoals tevens in enkele recente overzichtsartikelen reeds is beschreven [3,30]. In de praktijk wordt voor gentamicine en tobramycine de dosering geïndividualiseerd door het uitvoeren van TDM [5,6]. Ons onderzoek ondersteunt deze praktijk op verschillende niveaus. Allereerst kan door gebruik te maken van het doseernomogram potentieel de noodzaak voor een dosisaanpassing na TDM worden verminderd en zodoende de effectiviteit en veiligheid van aminoglycosiden in de eerste 24 uur van de behandeling worden verbeterd. Na het meten van één of twee spiegels wordt in de praktijk een individuele concentratie-tijdcurve voorspeld met behulp van Bayesiaanse farmacokinetische software. Betere farmacokinetische modellen in deze softwarepakketten zullen de kwaliteit van deze voorspellingen en daaruit volgende doseeradviezen verbeteren. Voor dit doel zijn de hier gepresenteerde farmacokinetische populatiemodellen inmiddels beschikbaar gemaakt via veel gebruikte TDM-softwareplatformen.
Conclusie
In dit onderzoek bij niet-obese en (morbide) obese patiënten tot 221 kg hebben we de toegenomen klaring en verdelingsvolume met gewicht voor gentamicine en tobramycine gekwantificeerd. De hierop gebaseerde doseerstrategie, om te komen tot vergelijkbare blootstelling in vergelijking met niet-obese patiënten die de standaarddosis krijgen, kan potentieel de noodzaak voor dosisaanpassingen na TDM verminderen en tevens de effectiviteit en veiligheid in de eerste 24 uur verbeteren.
Verantwoording
Geen belangenverstrengeling gemeld.
De auteurs danken wijlen prof. dr. Johan Mouton voor zijn bijdrage aan dit onderzoek. Tevens danken de auteurs dr. Matthijs Becker en Anne van Schip voor hun bijdrage in het verzamelen van data. Dit onderzoek is gefinancierd door ZonMW (projectnummer 836041004).
Informatie uit dit artikel is ook gepubliceerd in:
- Smit C, van Schip AM, van Dongen EPA, Brüggemann RJM, Becker ML, Knibbe CAJ. Dose recommendations for gentamicin in the real-world obese population with varying body weight and renal (dys) function. J Antimicrob Chemother. 2020 Nov 1;75(11):3286-3292.
- Smit C, Wasmann RE, Wiezer MJ, van Dongen HPA, et al. Tobramycin Clearance Is Best Described by Renal Function Estimates in Obese and Non-obese Individuals: Results of a Prospective Rich Sampling Pharmacokinetic Study. Pharm Res. 2019 May 30;36(8):112.
- Smit C, Wasmann RE, Goulooze SC, Hazebroek EJ, Van Dongen EPA, Burgers DMT, Mouton JW, Brüggemann RJM, Knibbe CAJ. A Prospective Clinical Study Characterizing the Influence of Morbid Obesity on the Pharmacokinetics of Gentamicin: Towards Individualized Dosing in Obese Patients. Clin Pharmacokinet. 2019 Oct;58(10): 1333-1343.
Literatuur
1. GBD 2015 Obesity Collaborators. Health Effects of Overweight and Obesity in 195 Countries over 25 Years. N Engl J Med. 2017 Jul 6;377(1):13–27.
2. VZinfo.nl: Grafiek volwassenen met overgewicht en obesitas [Internet]. RIVM: Bilthoven; 2019 [geraadpleegd 2020 Jan 20]. https://www.volksgezondheidenzorg.info/onderwerp/overgewicht/cijfers-context/huidige-situatie
3. Smit C, De Hoogd S, Brüggemann RJM, Knibbe CAJ. Obesity and drug pharmacology: a review of the influence of obesity on pharmacokinetic and pharmacodynamic parameters. Expert Opin Drug Metab Toxicol. 2018 Mar;14(3):275–85.
4. Knibbe CAJ, Brill MJE, Van Rongen A, Diepstraten J, van der Graaf PH, Danhof M. Drug disposition in obesity: Toward evidence-based dosing. Annu Rev Pharmacol Toxicol. 2015;55(1):149–67.
5. Coenradie S, Touw D. TDM-monografie Gentamicine [Internet]. Commissie Analyse en Toxicologie van de Nederlandse Vereniging voor Ziekenhuisapothekers. 2018.
https://tdm-monografie.org/gentamicine/
6. Hunfeld NGM, Touw DJ. TDM-monografie Tobramycine [Internet]. Commissie Analyse en Toxicologie van de Nederlandse Vereniging voor Ziekenhuisapothekers (NVZA). 2016.
https://tdm-monografie.org/tobramycine/
7. European Committee on Antimicrobial Susceptibility Testing (EUCAST). Gentamicin: Rationale for the EUCAST clinical breakpoints (version 2.0). 2020.
8. The United States Committee on Antimicrobial Susceptibility Testing (USCAST). Aminoglycoside In Vitro Susceptibility Test Interpretive Criteria Evaluations, version 1.3 [Internet]. 2019 [geraadpleegd 2020 Jun 16].
http://www.uscast.org/documents.html
9. European Committee on Antimicrobial Susceptibility Testing (EUCAST). Tobramycin: Rationale for the EUCAST clinical breakpoints (version 2.0). 2020.
10. Abdul-Aziz MH, Alffenaar JWC, Bassetti M, et al. Antimicrobial therapeutic drug monitoring in critically ill adult patients: a Position Paper. Intensive Care Med. 2020 Jun;46(6):1127–53.
11. Hodiamont CJ, van den Broek AK, de Vroom SL, Prins JM, Mathôt RAA, van Hest RM. Clinical Pharmacokinetics of Gentamicin in Various Patient Populations and Consequences for Optimal Dosing for Gram-Negative Infections: An Updated Review. Clin Pharmacokinet. 2022 Aug;61(8):1075–94.
12. Bauer LA, Edwards WA, Dellinger EP, Simonowitz DA. Influence of weight on aminoglycoside pharmacokinetics in normal weight and morbidly obese patients. Eur J Clin Pharmacol. 1983;24:643–7.
13. Leader WG, Tsubaki T, Chandler MH. Creatinine-clearance estimates for predicting gentamicin pharmacokinetic values in obese patients. Am J Hosp Pharm. 1994 Sep 1;51:2125–30.
14. Schwartz SN, Pazin GJ, Lyon JA, Ho M, Pasculle AW. A controlled investigation of the pharmacokinetics of gentamicin and tobramycin in obese subjects. J Infect Dis. 1978 Oct;138:499–505.
15. Korsager S. Administration of gentamicin to obese patients. Int J Clin Pharmacol Ther Toxicol. 1980 Dec;18(12):549–53.
16. Pai MP, Nafziger AN, Bertino JS Jr. Simplified estimation of aminoglycoside pharmacokinetics in underweight and obese adult patients. Antimicrob Agents Chemother. 2011 Sep;55(9):4006–11.
17. Sketris I, Lesar T, Zaske DE, Cipolle RJ. Effect of obesity on gentamicin pharmacokinetics. J Clin Pharmacol. 1981 Jul;21(7):288–93.
18. Janmahasatian S, Duffull SB, Ash S, Ward LC, Byrne NM, Green B. Quantification of lean bodyweight. Clin Pharmacokinet. 2005;44(10):1051–65.
19. Demirovic JA, Pai AB, Pai MP. Estimation of creatinine clearance in morbidly obese patients. Am J Heal Syst Pharm. 2009 Apr 1;66(7):642–8.
20. Levey AS, Coresh J, Greene T, et al. Using standardized serum creatinine values in the modification of diet in renal disease study equation for estimating glomerular filtration rate. Ann Intern Med. 2006 Aug 15;145(4):247–54.
21. Levey AS, Stevens LA, Schmid CH, et al. A new equation to estimate glomerular filtration rate. Ann Intern Med. 2009 May 5;150(9):604–12.
22. Centers for Disease Control and Prevention (CDC). National Health and Nutrition Examination Survey (NHANES): Questionnaires, Datasets, and Related Documentation 1999-2016 [Internet].
https://wwwn.cdc.gov/nchs/nhanes/Default.aspx
23. Mouton JW, Jacobs N, Tiddens H, Horrevorts AM. Pharmacodynamics of tobramycin in patients with cystic fibrosis. Diagn Microbiol Infect Dis. 2005 Jun;52(2):123–7.
24. Moore RD, Lietman PS, Smith CR. Clinical Response to Aminoglycoside Therapy: Importance of the Ratio of Peak Concentration to Minimal Inhibitory Concentration. J Infect Dis. 1987 Jan;155(1):93–9.
25. Moore RD, Smith CR, Lietman PS. Association of aminoglycoside plasma levels with therapeutic outcome in gram-negative pneumonia. Am J Med. 1984 Oct;77(4):657–62.
26. Smith PF, Ballow CH, Booker BM, Forrest A, Schentag JJ. Pharmacokinetics and pharmacodynamics of aztreonam and tobramycin in hospitalized patients. Clin Ther. 2001 Aug;23(8):1231–44.
27. European Medicines Agency (EMA). Guideline on the use of pharmacokinetics and pharmacodynamics in the development of antimicrobial medicinal products. 2016.
28. Lee PI. Design and power of a population pharmacokinetic study. Pharm Res. 2001 Jan;18(1):75–82.
29. Wishart DS, Feunang YD, Guo AC, et al. DrugBank 5.0: a major update to the DrugBank database for 2018. Nucleic Acids Res. 2018 Jan 4;46(D1):D1074–82.
30. Jain R, Chung SM, Jain L, et al. Implications of obesity for drug therapy: limitations and challenges. Clin Pharmacol Ther. 2011 Jul;90(1):77–89.
Referentie
Citeer als: Smit C, Wasmann RE, Wiezer MJ, van Dongen EPA, Brüggemann RJM, Knibbe CAJ. Hogere dosis aminoglycosiden nodig in morbide obese patiënten: nieuwe doseeradviezen onderbouwd. Nederlands Platform voor Farmaceutisch Onderzoek. 2023;8:a1763.
DOI
https://www.knmp.nl/resolveuid/1b280a4c85da4fa7b913523c06ff8420Open access

Reactie toevoegen