Het effect van medicatieverificatie bij poliklinische internegeneeskundepatiënten
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2019;4:a1709
Kernpunten
- Verschillende internationale richtlijnen bevelen de implementatie van medicatieverificatie aan.
- Medicatieverificatie wordt vooral toegepast bij klinische patiënten.
- Deze studie laat een significante halvering van het aantal patiënten met een discrepantie op de internegeneeskundepolikliniek zien. Dit is vergelijkbaar met eerdere studies bij klinische patiënten.
Abstract
An evaluation of medication reconciliation at an outpatient internal medicines clinic
BACKGROUND
Several international guidelines recommend the implementation of medication reconciliation.
OBJECTIVE
To evaluate the impact of medication reconciliation at an outpatient internal medicines clinic.
DESIGN
A prospective before-and-after study was conducted in the OLVG hospital, Amsterdam.
METHODS
At the internal medicines clinic, all adults (≥ 18 years of age) with a written informed consent and using more than one drug chronically (≥ 3 months) were included. In the usual care group no structural medication reconciliation was performed. In the intervention group, one week before the visit, the patient’s actual medication use (name, dosage, frequency) was assessed by phone by a pharmacy technician.
The primary outcome was the proportion of patients with unintentional discrepancies between documented and actual medication use. Secondary outcomes were the time needed by the physician to discuss medication-related topics during the outpatient visit, patient knowledge of medication changes, and patient satisfaction. Descriptive analysis and logistic regression was used to analyze the outcomes.
RESULTS
A total of 308 patients were included: 157 usual care, 151 intervention. The proportion of patients with an unintentional discrepancy decreased significantly by medication reconciliation: usual care 83%, intervention 39% (adjusted OR = 0.14, CI = 0.08-0.25). The physician used similar amounts of time to discuss drug-related topics in both groups (P = 0.316). Patients’ knowledge regarding medication changes increased non-significantly from 71% to 84% after medication reconciliation in the intervention group (P =0.058, adjusted OR = 1.35, CI = 0.64-3.64). Patients in both groups were equally satisfied with the physicians’ communication.
CONCLUSION
Similar to previous studies, medication reconciliation significantly decreased discrepancies with 50%. Further research is needed to assess the impact of medication reconciliation on clinical outcomes (e.g. adverse drug events).
Inleiding
Incomplete medicatieoverdracht kan resulteren in discontinuïteit in de gezondheidszorg. Discrepanties tussen het actuele medicatiegebruik van de patiënt en het gedocumenteerde medicatiegebruik door de zorgverlener zijn hier een belangrijk voorbeeld van [1-7]. Ashjian et al. tonen aan dat 88% van de poliklinische patiënten één of meerdere discrepanties heeft [8]. Deze discrepanties kunnen leiden tot voorkombare risico’s in ernstige gevallen leidend tot ziekenhuisopnames [6].
Verschillende internationale richtlijnen bevelen de implementatie van medicatieverificatie aan [9]. Medicatieverificatie wordt gedefinieerd als: het proces van het opstellen van het meest accurate medicatieoverzicht van de patiënt en het gebruik van dit overzicht voor een correcte medicatieverstrekking in de gehele gezondheidszorg [10]. Medicatieverificatie is in Nederland beperkt geïmplementeerd in de poliklinische setting.
In de literatuur is er veel onderzoek gedaan naar medicatieverificatie in het ziekenhuis. Ook in de poliklinische setting kan medicatieverificatie onbedoelde discrepanties reduceren bij 14-98% van de patiënten [11]. Bij poliklinische patiënten kunnen wellicht meer onbedoelde discrepanties optreden, omdat er minder tijd beschikbaar is om de medicatie te verifiëren met de patiënt [13]. In theorie zou medicatieverificatie door de apotheek, de arts tijd kunnen besparen tijdens het consult. Deze tijd zou de arts kunnen besteden aan informatie over wijzigingen in de medicatie en over goed geneesmiddelengebruik.
Het doel van deze studie is het effect van medicatieverificatie op het aantal onbedoelde discrepanties tussen actueel en gedocumenteerd medicatiegebruik te bepalen bij poliklinische patiënten op de polikliniek interne geneeskunde. Daarnaast wordt gekeken naar de tijdsinvestering van de arts om medicatiegerelateerde onderwerpen te bespreken tijdens het consult. Tot slot wordt de kennis van medicatiewijzigingen door de patiënt en de patiënttevredenheid geëvalueerd.
Methoden
Setting en studiepopulatie
Een prospectieve voor-na-studie werd uitgevoerd in het OLVG locatie West te Amsterdam. De controlegroep werd geïncludeerd in de periode februari tot en met april 2015 en – na een implementatieperiode – de interventiegroep in de periode juni tot en met juli 2015. Volwassenen (18 jaar en ouder) die een bezoek brachten aan de polikliniek interne geneeskunde werden geïncludeerd wanneer zij meer dan 1 geneesmiddel chronisch – langer dan drie maanden – gebruikten. Patiënten werden geëxcludeerd wanneer ze niet telefonisch bereikbaar waren na drie pogingen, wanneer ze geen informed consent gaven of wanneer er taal- en/of cognitieve barrières waren.
Controlegroep
In de controlegroep werd geen structurele medicatieverificatie uitgevoerd. De behandelend arts verifieerde het medicatiegebruik bij de patiënt wanneer dit noodzakelijk werd geacht. Sommige patiënten hadden een medicatieoverzicht of hun geneesmiddelen bij zich tijdens het bezoek aan de polikliniek. Naar het inzicht van de arts werd indien nodig de medicatie bijgewerkt in het ziekenhuisinformatiesysteem (ZIS).
Interventiegroep
De implementatieperiode bedroeg twee maanden, waarbij een farmaceutisch consulent de patiënten twee weken voor het polikliniekbezoek telefonisch heeft benaderd. Hierbij werd toestemming gevraagd voor het onderzoek en voor het opvragen van de medicatiehistorie bij de openbare apotheek. Na de beoordeling van de medicatiehistorie werden de patiënten één week voor het polikliniekbezoek opnieuw gebeld door een farmaceutisch consulent. Hierbij werden de patiënten via een standaard protocol geïnterviewd over hun actuele medicatiegebruik (naam, dosering en frequentie), inclusief het gebruik van zelfzorgmedicatie en eventuele bestaande allergieën.
De informatie verkregen uit de medicatiehistorie van de openbare apotheek en het interview met de patiënt (gouden standaard) werd vergeleken met de medicatie in het ZIS. Redenen voor discrepanties tussen het gedocumenteerde en actuele medicatiegebruik werden nagevraagd bij de patiënt. Vervolgens heeft de farmaceutisch consulent de geneesmiddelen in het ZIS geüpdatet, waarna de arts het voorstel tot medicatiewijziging(en) kon overnemen in het dossier.
Dataverzameling en classificatie
Het gesprek tussen patiënt en arts tijdens de polikliniekbezoeken werd in beide groepen opgenomen om de tijd die de arts besteedde aan medicatiegerelateerde onderwerpen vast te stellen. Daarnaast werd geëxtraheerd welke medicatiewijzigingen de arts doorvoerde tijdens het bezoek.
De medicatiegerelateerde onderwerpen werden onderverdeeld in de volgende categorieën: inventarisatie van het actuele medicatiegebruik, effectiviteit van geneesmiddelen, bijwerkingen, interacties, gebruik van (nieuwe) geneesmiddelen, gebruik van zelfzorgmedicatie, benodigde herhaalrecepten en overige onderwerpen.
De medicatiewijzigingen werden onderverdeeld in vier categorieën: start van nieuwe geneesmiddelen, stoppen van geneesmiddelen, wijzigingen in dosis of frequentie en omzetting binnen dezelfde geneesmiddelklasse.
Om het aantal onbedoelde discrepanties te kunnen bepalen, werden patiënten uit beide groepen gebeld binnen één week na het polikliniekbezoek (maximaal drie belpogingen). De patiënten werd gevraagd om hun medicatiedoosjes bij de hand te hebben, waarna medicatieverificatie werd uitgevoerd in beide groepen door dezelfde onderzoeker (SvdG). Het actuele medicatiegebruik zoals verkregen tijdens dit telefoongesprek werd vergeleken met het gedocumenteerde medicatiegebruik in het ZIS. Discrepanties werden geclassificeerd in vier categorieën: omissie (wanneer een patiënt een geneesmiddel gebruikt dat niet in het ZIS gedocumenteerd was), commissie (wanneer een patiënt een geneesmiddel niet gebruikt dat wel in het ZIS gedocumenteerd was), dosis/schema (verschillen in dosering of frequentie) en switch (verschillen binnen dezelfde geneesmiddelklasse).
Tijdens het telefonisch interview werden de patiënten ook gevraagd om te benoemen welke medicatiewijzigingen doorgevoerd waren tijdens het polikliniekbezoek. De informatie van de patiënt werd vergeleken met de informatie uit het ZIS en de geluidsopname van het polikliniekbezoek. De kennis over medicatiewijzigingen van de patiënt werd als correct geclassificeerd als de patiënt de juiste naam, dosering en frequentie kon noemen van elk gewijzigd geneesmiddel.
Om de patiënttevredenheid te bepalen met betrekking tot de communicatie over geneesmiddelen en – voor de interventiegroep – de medicatieverificatieservice, werd aan de patiënten gevraagd een vragenlijst in te vullen na het polikliniekbezoek. De tevredenheid met betrekking tot de communicatie van de arts werd gescoord op een vijfpuntsschaal, waarbij 1 zeer ontevreden is en 5 zeer tevreden. Als aanvulling werden vragen gesteld om te bepalen of patiënten genoeg tijd hadden om alle medicatiegerelateerde onderwerpen te bespreken en of alle vragen gesteld konden worden. De interventiegroep kon daarnaast opmerkingen plaatsen over de medicatieverificatieservice en voorstellen doen voor verbetering.
Eindpunten
Het primaire eindpunt was het aantal patiënten met een onbedoelde discrepantie in beide groepen. Secundaire eindpunten waren het aantal onbedoelde discrepanties per patiënt, de mediane tijd die de arts nodig had voor medicatiegerelateerde onderwerpen, het aantal patiënten met een correcte kennis van medicatiewijzigingen en patiënttevredenheid met betrekking tot de communicatie over geneesmiddelen en de medicatieverificatieservice.
Analyse
Alle kwantitatieve data werden verzameld in Microsoft Excel 2010 en geanalyseerd met SPSS (versie 21.0.0 SPSS, Inc., Chicago, IL). Voor continue variabelen werden de groepen vergeleken via een ongepaarde Student-t-toets voor normaal verdeelde data en de Mann-Whitneytoets voor niet-normaal verdeelde data. Voor categorische variabelen werd gebruik gemaakt van een Pearson’s chi-kwadraattoets of een Fisher’s exacttoets. Een P-waarde van < 0,05 werd gezien als statistisch significant.
Multivariabele logistische regressie werd gebruikt om te corrigeren voor verschillen in basiskarakteristieken. Mogelijke confounders werden achtereenvolgens in een handmatige logistische regressie ingevoerd. Wanneer de ß-coëfficiënt meer dan 10% wijzigde werd de confounder in het model gelaten. Ruwe en aangepaste odds ratio’s (OR’s) met 95%-betrouwbaarheidsintervallen (95%-BI’s) en P-waarden werden berekend.
Resultaten
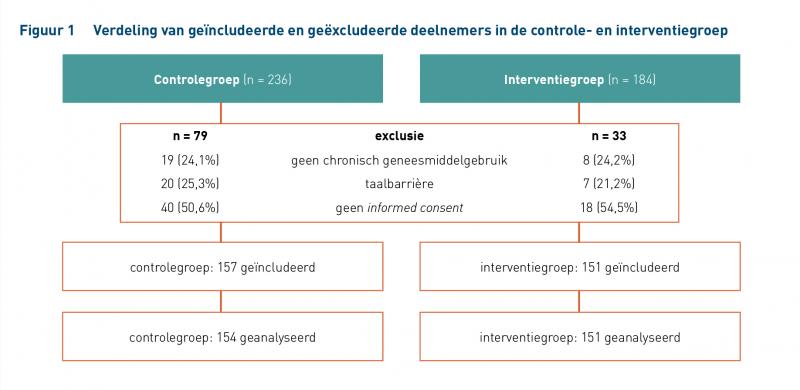
In totaal zijn 420 patiënten gescreend, waarvan 308 geïncludeerd: 157 in de controlegroep en 151 in de interventiegroep (figuur 1). De voornaamste reden van exclusie was het ontbreken van een informed consent of van chronisch geneesmiddelengebruik. In de controlegroep vielen drie patiënten uit na drie belpogingen.
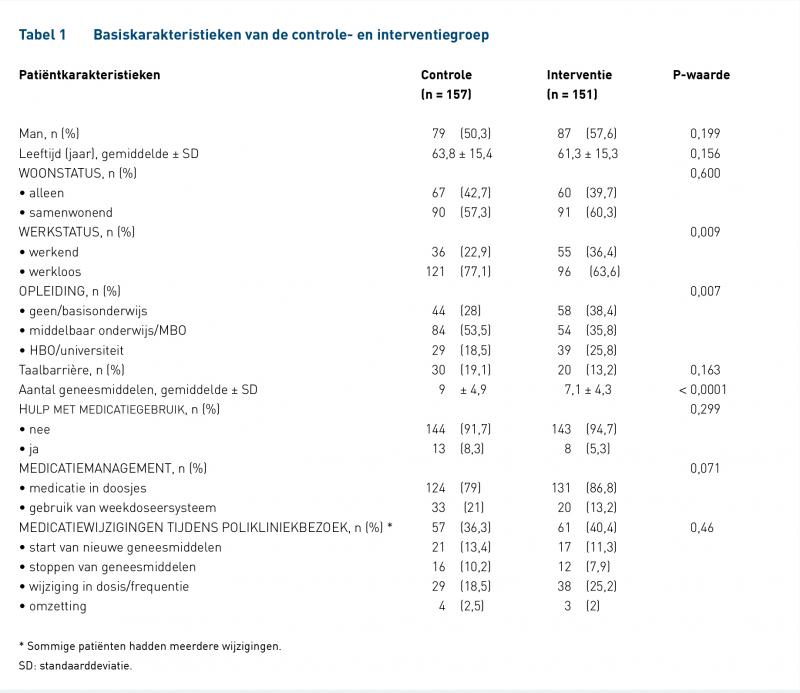
De gemiddelde leeftijd van de patiënten was 63 jaar en verschilde niet tussen beide groepen (P = 0,156; tabel 1). Ook het geslacht en het aantal patiënten met een medicatiewijziging verschilde niet. Er waren significant meer werkenden (P = 0,009) en hogeropgeleiden (P = 0,007) in de interventiegroep. Daarnaast gebruikte de controlegroep significant meer geneesmiddelen dan de interventiegroep (9 ten opzichte van 7 middelen, P < 0,0001).
Onbedoelde discrepanties
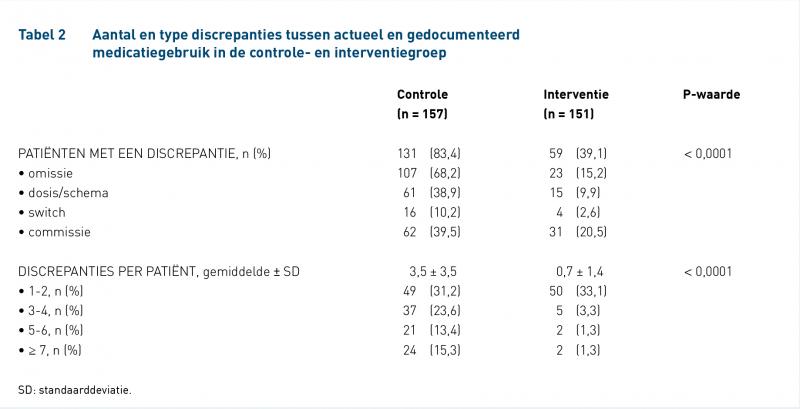
Het aantal patiënten met een onbedoelde discrepantie daalde van 83% in de controlegroep naar 39% in de interventiegroep (P <0,001; tabel 2). De aangepaste OR was 0,14 (95%-BI = 0,08-0,25) na aanpassen voor verschillen in de basiskarakteristieken werkstatus, opleidingsniveau en aantal gebruikte geneesmiddelen.
De afname in het aantal discrepanties was het grootst bij omissies en dosis/frequentie-discrepanties met een afname van respectievelijk 53% en 29%. Omissies kwamen het meest voor bij vitaminepreparaten (16,6%), gevolgd door cardiovasculaire geneesmiddelen (14%). Dosis/frequentie-discrepanties kwamen daarentegen het meest voor bij antidiabetica, voornamelijk insulinepreparaten (39%), gevolgd door cardiovasculaire geneesmiddelen (20,3%).
Het aantal discrepanties per patiënt nam significant af met een gemiddelde van 3,5 (standaarddeviatie [SD] = 3,5) discrepanties per patiënt in de controlegroep naar 0,7 (SD = 1,4) in de interventiegroep (P < 0,0001; tabel 2). Met name het aantal patiënten met multipele discrepanties nam af.
Tijd voor medicatiegerelateerde onderwerpen
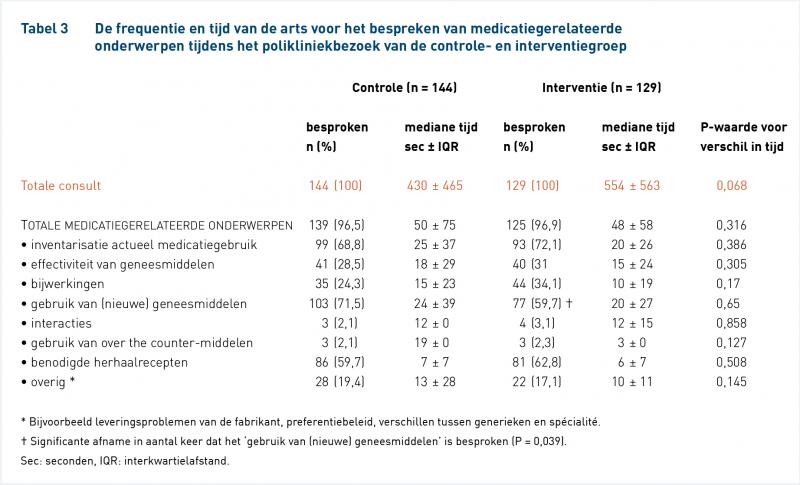
In de controle- en interventiegroep zijn bij respectievelijk 144 (93,5%) en 129 (85,4%) van de polikliniekbezoeken geluidsopnamen gemaakt (tabel 3). De arts besprak medicatiegerelateerde onderwerpen gedurende een mediane tijdsduur van 49 seconden, oftewel 11,6% en 8,7% van de totale consulttijd voor de controle- en interventiegroep, respectievelijk (P = 0,316). Er was een grote tijdsvariatie tussen de verschillende medicatiegerelateerde onderwerpen (tabel 3). De tijdsduur voor de onderwerpen verschilde niet significant, behalve voor het ‘gebruik van (nieuwe) geneesmiddelen’. Dit onderwerp werd significant vaker besproken in de controlegroep dan in de interventiegroep, 71,5% en 59,7% respectievelijk (P = 0,039). In de interventiegroep werd alsnog een inventarisatie van het actuele medicatiegebruik gedaan door de arts, waarbij voornamelijk werd gevraagd of er wijzigingen waren ten opzichte van het vorige bezoek.
Medicatiewijzigingen
In totaal werden in beide groepen 79 medicatiewijzigingen doorgevoerd tijdens het polikliniekbezoek, waarbij wijzigingen in dosis/frequentie het meest voorkwamen (tabel 4). Het aantal patiënten dat de medicatiewijziging correct kon benoemen steeg van 70,9% in de controlegroep naar 83,5% in de interventiegroep (P = 0,058, aangepaste OR = 1,35, 95%-BI = 0,55-3,28).
Patiënttevredenheid
De gemiddelde tevredenheidsscore met betrekking tot communicatie over geneesmiddelen verschilde niet tussen beide groepen (P = 0,687; tabel 4). Significant meer patiënten hebben aangegeven dat al hun medicatiegerelateerde vragen zijn beantwoord in de interventiegroep en dat er voldoende tijd was om alle medicatiegerelateerde onderwerpen te bespreken.
Van alle patiënten uit de interventiegroep reageerde 87,4% positief op de medicatieverificatieservice. Hierbij werd genoemd dat ze het belang van deze service inzagen. Daarnaast waardeerden patiënten de monitoring van hun medicatiegebruik. De overige 12,6% van de patiënten vond medicatieverificatie onnodig, waarbij ze aannamen dat de arts al op de hoogte was van het actuele medicatiegebruik.
Beschouwing
Deze studie laat zien dat medicatieverificatie leidt tot een significante afname van het aantal patiënten met onbedoelde discrepanties tussen actueel en gedocumenteerd medicatiegebruik van 83% naar 39% (aangepaste OR = 0,14, 95%-BI = 0,08-0,25). Het aantal discrepanties per patiënt nam aanzienlijk af van 3,5 naar 0,7 per patiënt. De correcte benoeming van medicatiewijzigingen door de patiënt vertoonde een niet-significante toename in de interventiegroep. Tot slot werd er in deze studie geen significant verschil gezien in de tijd die de arts besteedt aan medicatiegerelateerde onderwerpen tijdens het polikliniekbezoek. Ruim 80% van de patiënten is tevreden met de medicatieverificatieservice.
Medicatieverificatie is met enige regelmaat bestudeerd. Slechts enkele studies hebben medicatieverificatie uitgevoerd in de poliklinische setting [1,2,14,17]. Een systematische review van Bayoumi et al. laat een grote variatie zien in de verschillende studies, waarbij de ene geen voordeel van medicatieverificatie aangeeft en de andere een afname in het aantal discrepanties liet zien van 88,5% naar 49,1% [14,20,21]. De afname van 50% in de laatste studie komt overeen met de resultaten van deze studie. Vergelijkbare afnames in het aantal discrepanties zijn aangetoond door Nassarella et al. die een afname van 90% naar 29% lieten zien [15]. Verschillen in het effect van medicatieverificatie kunnen verklaard worden door de verschillen in patiëntengroepen. De invloed van medicatieverificatie op klinische uitkomsten, waaronder daadwerkelijke medicatiegerelateerde schade, blijft nog onduidelijk [11]. In de interventiegroep bleven discrepanties aanwezig, omdat patiënten bepaalde geneesmiddelen vergaten te benoemen, zoals crèmes, zalven en vitaminepreparaten. Mogelijk zorgde de tweede medicatieverificatie voor een trigger om deze geneesmiddelen alsnog te benoemen.
Deze studie is de eerste die kijkt naar de tijd die de arts heeft besteed aan het bespreken van medicatiegerelateerde onderwerpen tijdens het polikliniekbezoek. We hadden een afname verwacht in de tijd die de arts nodig had voor het verifiëren van de medicatie en een toename in de overige onderwerpen. Dit werd niet vastgesteld in deze studie, wellicht door de korte implementatieperiode. Een gelijkwaardige meting na 1 tot 2 jaar zal mogelijk andere resultaten geven. Artsen gebruikten slechts 10% van de totale tijd van het polikliniekbezoek, wat overeenkomt met 49 seconden per patiënt. Hiervan werden 23 seconden gebruikt voor inventarisatie van het huidige medicatiegebruik van de patiënt. Hierbij lijkt weinig ruimte voor verdere afname van de tijd die de arts besteedt aan medicatiegerelateerde onderwerpen.
Opvallend was dat er een verschuiving in onderwerpen optrad, waarbij er een significante afname was in het aantal keer dat ‘gebruik van (nieuwe) geneesmiddelen’ is besproken in de interventiegroep (P = 0,042). Dit kan wellicht verklaard worden doordat patiënten hun vragen over het gebruik konden stellen aan de farmaceutisch consulent op het moment van telefonische verificatie. Voorbeelden hiervan waren ‘moet ik deze geneesmiddelen mijn hele leven blijven gebruiken?’ of ‘wat is het beste tijdstip om mijn geneesmiddelen in te nemen (voor/tijdens/na de maaltijd)?’
In tegenstelling tot het bovenstaande, hebben we een niet-significante toename gezien in het correct benoemen van medicatiewijzigingen door de patiënt. Dit kan toeval zijn, maar patiënten konden ook meer getriggerd zijn met betrekking tot medicatie vanwege de medicatieverificatieservice. Ook omdat ze significant vaker benoemden dat al hun vragen waren beantwoord en er genoeg tijd was voor medicatie.
Sterktes en beperkingen
Een sterk punt van deze studie was de structurele basis waarop alle interviews met de patiënten over het actuele medicatiegebruik zijn afgenomen.
Er waren ook beperkingen aan deze studie. Als eerste beperking is de studie niet gerandomiseerd en niet geblindeerd. Hier is bewust voor gekozen, aangezien het proces significant veranderde met de interventie, wat voor contaminatiebias kan zorgen.
Ten tweede waren veel patiënten niet of laagopgeleid en deze studie is uitgevoerd in één ziekenhuis, waardoor de generaliseerbaarheid beperkt is.
Ten derde is enkel het aantal discrepanties bepaald en niet de klinische impact van deze discrepanties. Hierbij is het logisch dat een omissie van vitaminepreparaten of paracetamol een kleinere klinische impact heeft dan een omissie van cardiovasculaire geneesmiddelen die interacties kunnen geven met nieuwe medicatie die gestart wordt tijdens het consult.
Verder zijn er bij 11,4% van de polikliniekbezoeken geen geluidsopnamen gemaakt. Dit kan leiden tot een onderschatting van de medicatiewijzigingen. De patiënten rapporteerden echter geen additionele medicatiewijzigingen tijdens het telefonisch interview.
Tot slot kunnen patiënten inzake patiënttevredenheid in de interventiegroep sociaal wenselijke antwoorden hebben gegeven.
Voor toekomstig onderzoek kunnen een aantal aanbevelingen worden gedaan. Andere efficiënte mogelijkheden voor medicatieverificatie zouden verder onderzocht moeten worden, bijvoorbeeld het gebruik van patiëntportalen. Vervolgstudies zullen de klinische impact van discrepanties moeten onderzoeken op daadwerkelijke medicatiegerelateerde schade. Via de Centrale Medicatie-incidenten Registratie zijn reeds enkele casussen gepubliceerd waar schade opgetreden is door onvoldoende implementatie van medicatieverificatie [27].
Conclusie
Medicatieverificatie op een polikliniek interne geneeskunde zorgt voor een afname van het aantal onbedoelde discrepanties tussen het actuele en gedocumenteerde medicatiegebruik. Daarnaast was er een niet-significante toename van de kennis van patiënten met betrekking tot medicatiewijzigingen. In deze studie werd geen verschil gemeten in de tijd die de arts besteedt aan medicatiegerelateerde onderwerpen tijdens het polikliniekbezoek. Patiënten waren tevreden met de medicatieverificatieservice.
Verantwoording
We willen graag onze dank uiten aan alle farmaceutisch consulenten, patiënten en openbare apotheken die meegewerkt hebben aan deze studie en aan de internisten voor hun inzet en medewerking om deze studie tot een goed einde te brengen.
Geen belangenverstrengeling gemeld.
Een verkorte versie van het artikel is verschenen als: Van der Gaag S, Janssen MJA, Wessemius H, Siegert CEH, Karapinar-Çarkit F. An evaluation of medication reconciliation at an outpatient internal medicines clinic. Eur J Intern Med. 2017 Oct;44:e32-e34. doi: 10.1016/j.ejim.2017.07.015.
Literatuur
- Neufeld NJ, Gonzalez Fernandez M, Christo PJ, et al. Positive recognition program increases compliance with medication reconciliation by resident physicians in an outpatient clinic. Am J Med Qual. 2013;28(1):40-5.
- Peyton L, Ramser K, Hamann G, et al. Evaluation of medication reconciliation in an ambulatory setting before and after pharmacist intervention. J Am Pharm Assoc. 2010;50:490-5
- Cornish PL, Knowles SR, Marchesano R, et al. Unintended medication discrepancies at the time of hospital admission. Arch Intern Med. 2005;164:424-9.
- Moore C, Wisnivesky J, Williams S, et al. Medical errors related to discontinuity of care from an inpatient to an outpatient setting. J Gen Intern Med. 2003;18(8):646-51.
- Joint Commission. Approved: will not score medication reconciliation in 2009. Plans to review, refine NPSG 8 for 2010. Jt Comm Perspect. 2009;29:1, 3.
- Kohn LT, Corrigan JM, Donaldson MS, eds. To err is human: building a safer health system. Washington, DC: National Academy Press; 1999.
- Taché SV, Sönnichsen A, Ashcroft DM. Prevalence of adverse drug events in ambulatory care: a systematic review. Ann Pharmacother. 2011;45:977-89.
- Ashjian E, Salamin LB, Eschenburg K, et al. Evaluation of outpatient medication reconciliation involving student pharmacists at a comprehensive cancer centre. J Am Pharm Assoc. 2015;55 (5):540-5.
- The Joint Commission. National Patient Safety Goals Effective January 1, 2015. Accessed at http://www.jointcommission.org/assets/1/6/2015_NPSG_AHC1.PDF, March 18, 2015.
- Pevnick JM, Shane R, Schnipper JL. The problem with medication reconciliation. BMJ Qual Saf. 2016;0:1-5.
- Lehnbom EC, Stewart MJ, Manias E, et al. Impact of medication reconciliation and review on clinical outcomes. Ann Pharmacother. 2014;48(10):1298-312.
- Weingart SN, Cleary A, Seger A, et al. Medication reconciliation in ambulatory oncology. Jt Comm J Qual Improv. 2007;33(12):750-7.
- Ho L, Akada K, Messner H, et al. Pharmacist’s role in improving medication safety for patients in an allogeneic hematopoietic cell transplant ambulatory clinic. Can J Hosp Pharm. 2013;66(2):110-7.
- Varkey P, Cunningham J, Bisping S. Improving medication reconciliation in the outpatient setting. Jt Comm J Qual Improv. 2007;33(5):286-92.
- Nassaralla CL, Naessens JM, Chaudhry R, et al. Implementation of a medication reconciliation process in an ambulatory internal medicine clinic. Qual Saf Health Care. 2007;16:90-94.
- Nassaralla CL, Naessens JM, Hunt VL, et al. Medication reconciliation in ambulatory care: attempts at improvement. Qual Saf Health Care. 2009;18:402-7.
- Andrus MR. Student pharmacist initiated medication reconciliation in the outpatient setting. Pharmacy Practice. 2012;10(2):78-82.
- Steward AL, Snodgrass J, Schontz M, et al. A student pharmacist-led medication reconciliation service and its impact on the identification of drug-related problems in an ambulatory clinic. Curr Pharm Teach Learn. 2015;7(5):575-83.
- Milone AS, Philbrick AM, Harris IM, et al. Medication reconciliation by clinical pharmacists in an outpatient family medicine clinic. J Am Pharm Assoc. 2014;54(2):181-7.
- Bayoumi I, Howard M, Holbrook AM, et al. Interventions to improve medication reconciliation in primary care. Ann Pharmacother. 2009;43:1667-75.
- Vira T, Colquhoun M, Etchells E. Reconcilable differences: correcting medication errors at hospital admission and discharge. Qual Saf Health Care. 2006;15:122-6.
- Osorio SN, Abramson E, Pfoh ER, et al. Risk factors for unexplained medication discrepancies during transitions in care. Fam Med. 2014;46(8):587-96.
- Andreoli L, Alexandra J-F, Tesmoingt C, et al. Medication reconciliation: a prospective study in an internal medicine unit. Drugs Aging. 2014;31:387-93.
- Vasileff HM, Whitten LE, Pink JA, et al. The effect on medication errors of pharmacist charting medication in an emergency department. Pharm World Sci. 2009;31:373-9.
- Schnipper JL, Kirwin JL, Cotugno MC, et al. Role of pharmacist counseling in preventing adverse drug events after hospitalization. Ann Intern Med. 2006;166:565-71.
- Ziaeian B, Araujo KLB, Van Ness PH, et al. Medication reconciliation accuracy and patient understanding of intended medication changes on hospital discharge. J Gen Intern Med. 2012;27(11):1513-20.
- Stichting Portaal voor Patiëntveiligheid. EVS meldingen en onderwijs EVS aan artsen. CMR Nieuwsbrief 2013: Nummer 4.
Referentie
Citeer als: Van der Gaag S, Janssen MJA, Wessemius H, Siegert CEH, Karapinar-Çarkit F. Het effect van medicatieverificatie bij poliklinische internegeneeskundepatiënten. Nederlands Platform voor Farmaceutisch Onderzoek. 2019;4:a1709.
DOI
https://www.knmp.nl/resolveuid/e08e7da852cb4b708100f9d3b5bc464aOpen access


Reactie toevoegen