Een praktische gids voor probiotica ter preventie van antibiotica-gerelateerde diarree in Nederland
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2019;4:a1689
Kernpunten
- Een meta-analyse laat zien dat zeven enkel of meerstammige probiotische formuleringen in staat zijn het risico op antibiotica-gerelateerde diarree (AGD) te verkleinen.
- De effectiviteit van probiotische formuleringen is afhankelijk van de dosering en de probiotische stam.
- Op basis van klinische studies kan als vuistregel worden aanhouden dat probiotica gedurende de hele periode van de antibioticakuur – twee uur na inname – en tot 1 à 2 weken na de kuur moeten worden ingenomen.
Abstract
A practical guide for probiotics applied to the case of antibiotic-associated diarrhea in The Netherlands
BACKGROUND
Antibiotic-associated diarrhea (AAD) is a side-effect frequently associated with the use of broad spectrum antibiotics. Although a number of clinical studies show that co-administration of specific probiotics reduces the risk for AAD, there is still unclarity among healthcare professionals on the recommendation of probiotic products.
OBJECTIVE
This paper aims to provide a practical guide to inform healthcare professionals, patients and consumers about the exact product characteristics of available probiotics with a proven efficacy to prevent AAD.
DESIGN and METHODS
The workflow in this paper includes three consecutive steps: a systematic review of relevant clinical studies for effective probiotics by a meta-analysis, compilation of a list of available probiotic products, and recommendation of probiotic products that match effective formulations. Our systematic review on the efficacy of probiotics for the prevention of AAD included only studies with randomized, double blind placebo-controlled trials, a clear definition of antibiotic associated diarrhea, and a probiotic administration regime for at least the duration of the antibiotic therapy.
RESULTS
Using our inclusion criteria, we selected 32 out of 128 identified trials and pooled the results of these studies for each specific dairy product and food supplement. The results indicate a total of seven single or multiple-strain formulations favoring the probiotic treatment group, with the strain Lactobacillus rhamnosus GG being the most effective (relative risk ratio of probiotic versus placebo 0.30 with 95% CI 0.16 - 0.5). We selected products for recommendation from a compiled list of all probiotic dairy products and food supplements available in The Netherlands and categorized them into groups of products showing effects against the incidence of AAD in at least one, two, or three independent clinical studies. We excluded all products which did not unambiguously declare on the label the specific probiotic strain(s) and the number of colony forming units.
CONCLUSION
Here, we present a practical guide that informs healthcare professionals and patients on the availability of probiotic products with a proven efficacy for the prevention of AAD.
Inleiding
Antibiotica-gerelateerde diarree
Antibioticagebruik in Nederland
Nederland is een van de Europese landen met het laagste antibioticagebruik in de eerstelijnsgezondheidszorg [1,2]. Daarnaast is het aantal antibioticavoorschriften in de ambulante zorg in Nederland volgens de European Surveillance of Antimicrobial Consumption over de laatste 20 jaar redelijk stabiel [1]. Desondanks zijn er in het laatste decennium stijgingen waargenomen in de aantallen antibioticavoorschriften in de ambulante zorg, vooral bij oudere patiënten (> 80 jaar) [3]. Deze categorie patiënten zou ook gevoeliger kunnen zijn voor de negatieve bijwerkingen van antibiotica. Meer recentelijk is het aangetoond dat infecties aan de lucht- en urinewegen, twee van de aandoeningen waarvoor de meeste antibiotica worden voorgeschreven [4], op hogere leeftijd vaker voorkomen [5]. Daarbij kwam ook naar voren dat volwassen patiënten in de leeftijd van 31 tot 65 jaar met bovenste luchtweginfecties – in vergelijking met andere leeftijdsgroepen – het grootste risico liepen om onnodig veel medicatie voorgeschreven te krijgen [6,7]. Bij kinderen was de leeftijdsgroep met de hoogste aantallen antibioticavoorschriften die van 0 tot 2 jaar [8].
Diarree is een veelvoorkomende bijwerking van de behandeling met antibiotica en komt het vaakst voor bij breedspectrum antibiotica. [9-11]. Een groeiende tendens in het voorschrijven van breedspectrum antibiotica wordt zelfs in een land als Nederland met een relatief laag aantal antibioticavoorschriften waargenomen [12]. Het breedspectrum antibioticum amoxicilline is bijvoorbeeld een van de 25 geneesmiddelen waarvan het aantal voorschriften in 2015 het meest gestegen is [13]. Amoxicilline is ook het meest voorgeschreven antibioticum in Nederland [1,14], en wordt – in combinatie met clavulaanzuur – vaak voorgeschreven binnen de eerstelijnsgezondheidszorg voor lucht- en urineweginfecties [4]. Interessant daarbij is verder dat amoxicilline/clavulaanzuur bij de antibiotica zitten die in Nederland het vaakst ten onrechte worden voorgeschreven [15]. Het voorschrijven van amoxicilline bij acute ongecompliceerde, onderste luchtweginfecties levert vaak weinig voordeel op dat bovendien niet in verhouding staat tot het risico op bijwerkingen [16].
Bijwerkingen van antibiotica
Antibioticagebruik wordt in verband gebracht met een reeks bijwerkingen. De meest voorkomende zijn bijwerkingen in de maag en darm, zoals misselijkheid en diarree. De bijlage Side-effects of antibiotics in het oorspronkelijke artikel bevat meer informatie over de bijwerkingen van antibiotica. Antibiotica-gerelateerde diarree (AGD) ontstaat wanneer een antibioticum het milieu van de darmmicrobiota verstoort door het diversiteitsprofiel te veranderen en het totale aantal bacteriën te verkleinen. Deze veranderingen kunnen op hun beurt leiden tot aanpassingen in het normale microbiële metabolisme en mogelijkerwijs tot de overgroei van opportunistische ziekteverwekkers die endogeen in de darmmicrobiota aanwezig zijn [17,18]. De meest voorkomende en ernstigste ziekteverwekker bij AGD is Clostridium difficile, waarvan geschat wordt dat deze verantwoordelijk is voor ongeveer 25% van de gevallen [19]. Meestal is diarree het resultaat van verstoring van de stofwisseling van de dikke darm, van de darmmicrobiota of van het slijmvlies van de patiënt [20].
Gemiddeld ontwikkelt 25% van de volwassenen die antibiotica krijgen antibiotica-gerelateerde diarree [21]; dit percentage is lager bij ambulante en hoger bij gehospitaliseerde patiënten [22]. Bij kinderen ligt de gemiddelde incidentie van diarree op 22%, met grote variaties ten aanzien van de leeftijd van het kind en het voorgeschreven antibioticum [23]. AGD kan resulteren in een verlenging van de ziekenhuisopname, hogere zorgkosten en andere complicaties.
Hoewel diarree over het algemeen een kortstondige bijwerking van de antibioticumbehandeling is, kunnen herhaaldelijke of bijkomende infecties tot langdurige gevolgen van antibioticagebruik leiden. Door hun invloed op de diversiteit en het aantal darmbacteriën kunnen antibiotica de capaciteit beïnvloeden van de residente darmmicrobiota om ziekteverwekkende micro-organismen af te weren [24]. Zelfs als het totaal aantal bacteriën weer op hetzelfde niveau terugkomt, kunnen er langdurige gevolgen zijn met betrekking tot het evenwicht van de darmmicrobiota en bijgevolg tot de vatbaarheid van de patiënt voor infecties en andere ziekten [25,26]. Blootstelling aan antibiotica kan vooral zeer risicovol zijn bij jonge kinderen (0 tot 24 maanden) als het microbioom van de gastheer nog in ontwikkeling is en gevoelig voor verstoringen [27,28]. Vroege blootstelling aan breedspectrum antibiotica wordt in verband gebracht met verhoogd risico op obesitas, astma, allergieën en diabetes [29-32].
Probiotica als profylaxe
Definitie en eigenschappen
Probiotica zijn ‘levende micro-organismen die, indien toegediend in toereikende hoeveelheden, de gastheer een gezondheidsvoordeel bieden’ [33]. Het belangrijkste voordeel van probiotica komt voort uit hun bijdrage bij het onderhouden van gezonde darmmicrobiota en derhalve bij het creëren van een gunstig darmmilieu [34]. Wenselijke kenmerken van probiotische producten zijn: een gehalte levensvatbare micro-organismen dat overeenkomt met een dosis waarvan in vivo vastgesteld is dat deze effectief is [35,36], resistentie tegen maagzuur en galzouten om de overgang door de maag en dunne darm te overleven, en hechtingsvermogen om het maagdarmstelsel te koloniseren om zo ziekteverwerkers uit te sluiten en het immuunsysteem te activeren [37].
Werkingsmechanismen
Probiotica kunnen ziekteverwekkende micro-organismen op verschillende wijzen bestrijden. De competitieve exclusie van ziekteverwekkers is een van de meest gebruikte verklaringen voor hun werking, omdat probiotica met ziekteverwekkers strijden om voedingsstoffen en aanhechtingsplaatsen op de slijmvliezen in de darmen [38]. Ook subtielere, remmende mechanismen kunnen een rol spelen, door de verstoring van signalen van ziekteverwekkende bacteriën, waardoor pathogeniteit wordt voorkomen [39]. Directe bestrijding kan daarnaast optreden door de productie van bacteriocines of metabolieten met antimicrobiële activiteit tegen pathogene micro-organismen [40,41]. Tenslotte zijn probiotica in staat om lokale en systemische afweerreacties in de patiënt te stimuleren [42].
Veiligheid
Het gebruik van probiotische producten bij gezonde mensen wordt als veilig beschouwd. Reviews gebaseerd op bewijs uit gerandomiseerde onderzoeken met een controlegroep concluderen dat probioticagebruik niet geassocieerd is met een verhoogd gezondheidsrisico, aangezien het optreden van bijwerkingen niet significant verschilt in vergelijking met de controlegroep [43,44].
Toepassingsgebied
Dit artikel vormt een praktische gids voor het gebruik van probiotica ter voorkoming van antibiotica-gerelateerde diarree. De gids is gebaseerd op beschikbaar wetenschappelijk bewijs en ontwikkeld aan de hand van een drie stappen:
• evaluatie van de effectiviteit van probiotica in de context van de ziekte, en identificatie van effectieve stammen en formuleringen door een systematische review van relevante klinische onderzoeken en een meta-analyse van hun resultaten;
• identificatie van probiotische producten die beschikbaar zijn voor de doelgroep;
• aanbeveling van specifieke probiotische producten met een werkzame productsamenstelling.
Het doel van deze gids is om zorgprofessionals en patiënten te informeren over de beschikbaarheid van probiotische producten die bewezen werkzaam zijn bij het voorkomen van AGD.
Methoden
Zoekstrategie en inclusiecriteria
We hebben in deze review studies opgenomen die de effectiviteit van probiotica beoordelen bij het verminderen van de incidentie van antibiotica-gerelateerde diarree (AGD) bij patiënten die een antibioticabehandeling ondergaan, onafhankelijk van de indicatie waarvoor de antibiotica zijn voorgeschreven. Om deze studies te identificeren zijn we eerst de referenties van eerder gepubliceerde systematische reviews en meta-analyses nagegaan, en hebben we direct daarna naar klinische onderzoeken gezocht in publieke databases. De gebruikte inclusiecriteria kunnen als volgt worden samengevat:
• gerandomiseerd, dubbelblind en placebogecontroleerd onderzoek;
• duidelijke definitie van AGD, en de incidentie van AGD is gemeten als een van de resultaten;
• de probiotica zijn tenminste voor de duur van de antibioticumbehandeling toegediend.
In Nederland beschikbare probiotische producten
In december 2016 hebben we een volledige lijst van in Nederland beschikbare probiotische producten opgesteld door websites van apotheken, vitaminehandels, gezondheidswinkels en webshops die probiotica verkopen af te gaan. Vervolgens heeft de stichting Natuur- en Gezondheidsproducten Nederland (NPN Amersfoort) onze lijst geëvalueerd en aangevuld.
Resultaten
Zoekstrategie en studieselectie
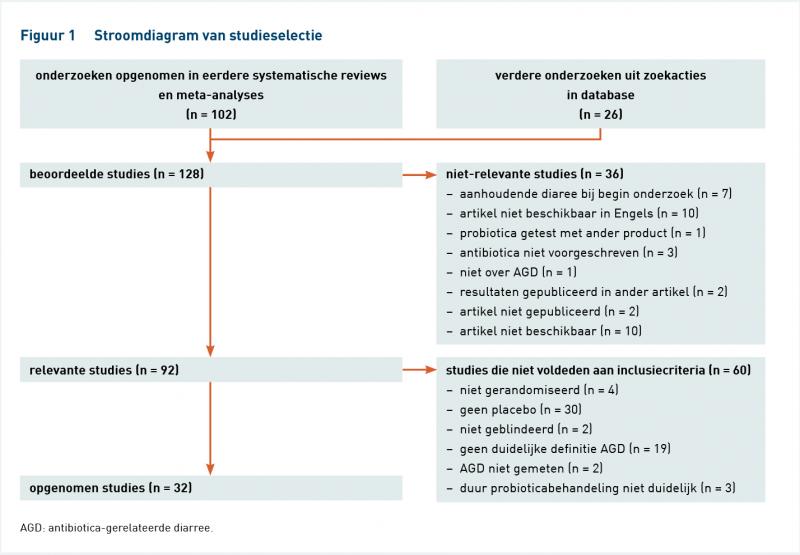
De meta-analyse – van zoekfase tot studieselectie – is afgebeeld in figuur 1. Uit het literatuuronderzoek kwamen 128 relevante studies. Een overzicht van deze studies en de redenen voor uitsluiting van een gedeelte hiervan is te vinden in de List of reviewed studies van het oorspronkelijke artikel. In totaal voldeden 32 studies aan onze inclusiecriteria en deze zijn opgenomen in de meta-analyse, waarvan 26 uit vorige reviews [45-70] en zes door direct in beschikbare databases te zoeken [71-76].
Data-analyse
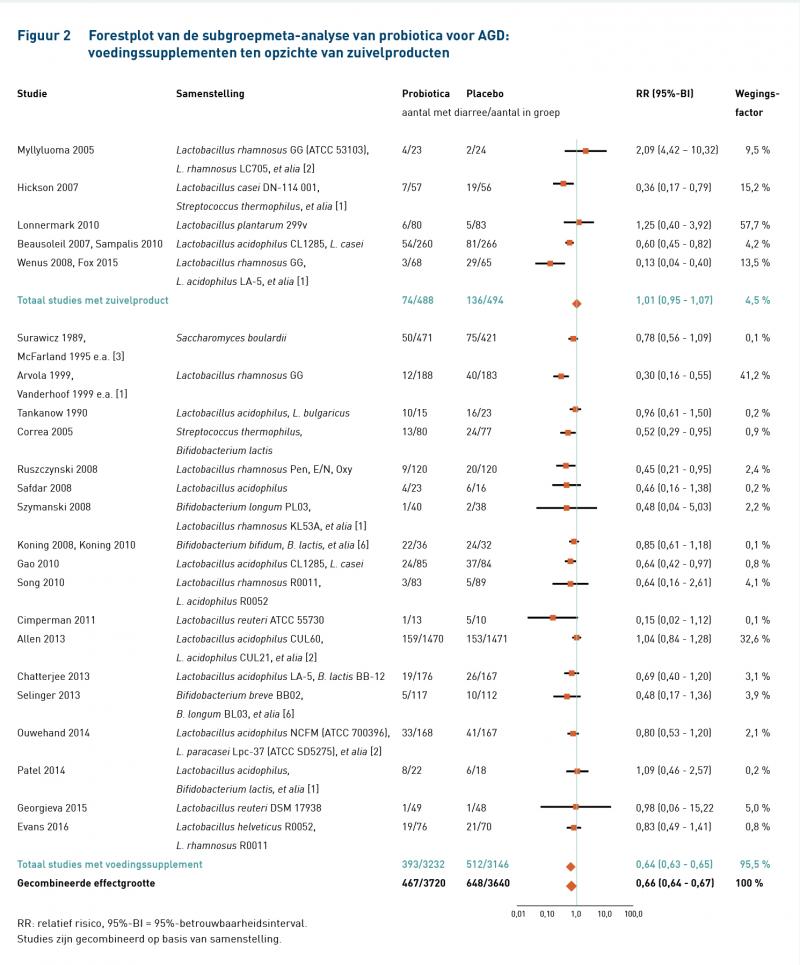
De resultaten van de meta-analyse zijn samengevat in figuur 2. In deze forestplot zijn studies gecombineerd op basis van de probiotische formulering en onderverdeeld in twee categorieën: zuivelproducten (7 studies) en voedingssupplementen (dat wil zeggen niet-zuivelproducten, 25 studies). Over het geheel genomen worden probiotica in verband gebracht met een lagere incidentie van antibiotica-gerelateerde diarree (467/3720 [13%]) in vergelijking met de controlegroep (648/3640 [18%]) (relatief risico [RR] = 0,66 met 95%-betrouwbaarheidsinterval [95%-BI] = 0,64-0,67). Bij studies die gebruik maken van probiotische zuivelproducten was de incidentie van AGD in de probiotische groep gemiddeld 15,2% in vergelijking met 27,5% in de controlegroep (RR = 1,01 met 95%-BI = 0,95-1,07). In geval van studies met voedingssupplementen was de incidentie van diarree in de probiotische groep 12,2% in vergelijking met 16,3% bij de controlegroep (RR = 0,64 met 95%-BI = 0,63-0,65).
Aanbevelingen
We hebben de volgende stammen geïdentificeerd die aan de aanbevelingscriteria voldoen: Lactobacillus rhamnosus GG met een minimale dagelijkse dosis van 2 x miljard kolonievormende eenheden (kve), krijgt een aanbeveling van drie sterren omdat er een effect is in tenminste drie van de geselecteerde studies [45,66,69]. De meerstammige formulering Lactobacillus rhamnosus GG, Lactobacillus acidophilus LA-5, Bifidobacterium lactis BB-12 toont een effect in twee van de geselecteerde studies [49,70], maar we konden geen probiotisch product identificeren met deze formulering. Een aantal meerstammige formuleringen heeft een aanbeveling van één ster gekregen, waaronder die met een effect in slechts één geselecteerde studie: Streptococcus thermophilus en Bifidobacterium lactis (minimale dagelijkse dosis: 5 miljard kve) [48], Lactobacillus rhamnosus strains Pen, E/N, Oxy (minimale dagelijkse dosis: 4 miljard kve) [61] en Lactobacillus acidophilus CL1285, Lactobacillus casei (minimale dagelijkse dosis: 50 miljard kve) [50]. Daarnaast hebben we een aanbeveling van één ster gegeven aan formuleringen die een trend lieten zien in twee of meer studies. Dit zijn Saccharomyces boulardii (minimale dagelijkse dosis: 10 miljard kve) [55,56,58,60,65] en Bifidobacterium bifidum, Bifidobacterium lactis, Enterococcus faecium, Lactobacillus acidophilus, Lactobacillus paracasei, Lactobacillus plantarum, Lactobacillus rhamnosus, Lactobacillus salivarium (minimale dagelijkse dosis: 10 miljard kve) [53,54].
Vervolgens hebben we op basis van bovenstaande categorieën de aanbevolen probiotische producten vastgesteld – zowel voedingssupplementen als zuivelproducten. Als we de in Nederland beschikbare producten in aanmerking nemen, zijn de aanbevolen producten de voedingssupplementen Microbiol Platinum (Vitals) en Culturelle (Allergy Research Group) die het probioticum Lactobacillus rhamnosus GG bevatten in een dagelijkse dosis van respectievelijk 33 en 11 miljard kve (tabel 1). We hebben alleen producten opgenomen en aanbevolen waarvan de probiotische stam(men) en kolonievormende eenheden vermeld worden en corresponderen met de stam en minimale dosis die in studies een positief effect of trend laten zien.
Beschouwing
Studieselectie en inclusiecriteria
In dit onderzoek zijn alleen studies geïncludeerd waarbij een duidelijke definitie van AGD is gebruikt. Studies zonder een duidelijke definitie kunnen nog steeds waardevolle informatie bevatten. Bovendien zouden sommige studies die een zeer strikte definitie van AGD hanteren het effect van probiotica ter preventie van AGD kunnen onderschatten [57]. We hebben systematisch gezocht naar klinische studies waarbij antibiotica zijn toegediend, maar we hebben geen strikte criteria gebruikt voor de klassen antibiotica en de specifieke ziektes waarvoor werd behandeld, omdat diarree een bijwerking kan zijn van verschillende antibiotica. Vijf van de geïncludeerde studies specificeerden niet welke antibiotica er werden toegediend. Van de overgebleven 27 studies waren er 21 waarbij verschillende antibiotica werden toegediend, waaronder breedspectrum penicillines en cefalosporines die worden geassocieerd met een relatief hoog risico op AGD. Onder de studies waarvoor werd gerapporteerd welke breedspectrum antibiotica zijn toegediend, werden geen systematische verschillen gevonden in de effectiviteit van het probioticum ter preventie van AGD en het antibioticum in kwestie [48,55,61]. Onder de geïncludeerde studies bevatten er 22 een poweranalyse, waarvan er 11 een significant verschil vonden tussen behandeling en placebo. Onder de 11 studies waarin geen verschil werd gevonden, waren er vier under powered [62-64,75].
Een belangrijk aspect bij het ontwerp van klinische studies is het gebruik van een geschikt placebo. In geval van studies met een zuivelproduct bestaat het placebo in het ideale geval uit een specifiek ontwikkeld product met organoleptische eigenschappen dat niet te onderscheiden is van het zuivelproduct dat de probiotica bevat. In het geval van de klinische studies die beschreven staan in dit artikel is het placebo vaak een product dat in een groot aantal opzichten afwijkt van het probiotische zuivelproduct. Omdat we op geen enkele manier kunnen nagaan op wat voor manier de productverschillen in kwestie de reactie op de placebo kunnen beïnvloeden, raden we producenten van probiotische zuivelproducten aan om producten te ontwikkelen die beter geschikt zijn om als placebo te dienen in klinische studies.
Criteria voor aanbevelingen
In deze studie hebben we zeer strikte criteria gebruikt om tot aanbevelingen te komen uit de resultaten van onze meta-analyse. We hebben besloten om sterke aanbevelingen – drie sterren – voor commerciële producten te beperken tot producten waarvoor exact dezelfde combinatie van stammen was getest, en niet de enkele stammen in separate studies. Daarnaast moet de effectiviteit van het product positief bevonden zijn in op zijn minst drie onafhankelijke studies. Deze benadering is noodzakelijk voor evidentie-gebaseerde besluitvorming, maar kent zijn beperkingen, omdat er naar alle waarschijnlijkheid vele andere producten, waarvan de compositie niet is getest, effectief zijn in de preventie van AGD. Veruit de meeste studies met meerstammige producten die we geëvalueerd hebben (figuur 2), lieten een significante afname zien van het risico op AGD [53,54,76]. De zuivelproducten die we aanbevelen lieten een positief effect zien in een klinische studie, maar het is zeker niet uitgesloten dat producten van andere merken met vergelijkbare formuleringen net zo effectief zijn. We hebben bijvoorbeeld een studie geëvalueerd die een positief effect liet zien van de probiotische drank Actimel (Danone) bij de preventie van AGD [52], en we hebben dit product dus opgenomen in onze lijst van 1-ster aanbevelingen. Het bedrijf Yakult produceert een zuiveldrank die een stam van Lactobacillus casei bevat die zo goed als identiek is aan de stam die in Actimel wordt gebruikt [77]. Toch achten we het noodzakelijk voor een aanbeveling dat evidentie voor het effect van Yakult ter preventie van AGD in een separate klinische studie wordt verkregen, aangezien de effectiviteit van de probiotische zuivelproducten niet alleen bepaald wordt door de aanwezige probiotische stammen, maar ook door de specifieke condities gedurende het productieproces. Afhankelijk van dit proces varieert de samenstelling van bacteriële metabolieten in het eindproduct die de effectiviteit kunnen beïnvloeden.
Hoewel onze aanbevelingen gebaseerd zijn op andere criteria en we ons niet beperkt hebben tot studies met kinderen, wijzen wij erop dat ze in overeenstemming zijn met de die van The European Society for Pediatric Gastroenterology, Hepatology and Nutrition. Zij maakt sterke aanbevelingen voor gebruik van L. rhamnosus GG (drie sterren in onze studie) en S. boulardii (één ster in onze studie) ter voorkoming van AGD bij kinderen [78]. Uit onze meta-analyse blijkt dat S. boulardii een positief effect laat zien bij kinderen [55], een positieve trend bij volwassenen [58,65], maar geen effect bij ouderen [56,60]. Leeftijd is dus een factor van belang bij de evaluatie van gezondheidseffecten van probiotica. In het algemeen geldt dat verschillen in de criteria om studies te includeren en in de maatstaven om aanbevelingen te formuleren kunnen leiden tot verschillend op evidentie gebaseerd advies.
Factoren voor effectiviteit van probiotica
Er zijn vele factoren die de effectiviteit van probiotische producten kunnen bepalen onder specifieke, klinische condities. Allereerst wordt de effectiviteit bepaald door de specifieke samenstelling van probiotische stammen. Een van de best bestudeerde probiotische stammen is Lactobacillus rhamnosus GG. Deze stam heeft effectiviteit laten zien in de reductie van AGD en andere darmaandoeningen in een groot aantal onafhankelijke studies [79]. Verschillende stammen van de soort Lactobacillus rhamnosus zijn niet even effectief in de preventie van AGD [80], en dit is ook het geval voor andere probiotische soorten. Klinische studies zouden altijd moeten specificeren welke probiotische stam wordt getest. Indien alleen de soortnaam wordt vermeld, kunnen de resultaten ervan niet op waarde worden geschat en kunnen zij niet worden vergeleken met andere studies. Zelfs onder ‘identiek’ veronderstelde stammen, waaronder LGG, is genotypische variabiliteit vastgesteld die resultaten van klinische studies kunnen beïnvloeden [81]. Het is dus zaak na te gaan voor aanvang van de studie of de stam nog beschikt over dezelfde genetische eigenschappen als de referentiestam. Naast de specifieke probiotische stam en soort speelt uiteraard de samenstelling van de stammen in een meerstammige product een rol bij de effectiviteit. In geval van zuivelproducten is ook het moment van toevoegen van de probiotische stammen – voor of na de fermentatie – van belang. Dit aangezien hun betrokkenheid bij de productie van metabolieten van invloed zal zijn op de uiteindelijke samenstelling van het product. In deze studie hebben we zuivelproducten en supplementen apart geanalyseerd, en hebben we alleen producten gecombineerd met exact dezelfde samenstelling om het effect van deze verschillen op de resultaten te minimaliseren.
De effectiviteit van probiotica wordt ook bepaald door verschillen tussen individuele patiënten, waaronder leeftijd, specifieke gezondheidstoestand, genetische factoren, en de samenstelling van de darmmicrobiota, zoals evident in een aantal van de klinische studies die we hebben geëvalueerd. De grootste klinische studie in onze meta-analyse, die is gerapporteerd door Allen et al. met 3000 deelnemers, liet geen significant verschil zien tussen probioticum en placebo [71]. In deze studie werden uitsluitend participanten geïncludeerd die ouder waren dan 65 en dus vatbaarder zouden kunnen zijn voor hardnekkige bijwerkingen van antibiotica. De effectiviteit van probiotica varieert onder verschillende leeftijdscategorieën en wordt beïnvloed door het antibioticaregime gedurende therapie. Hogere incidentie van AGD is waargenomen in patiënten van hoge leeftijd die relatief lang werden behandeld met antibiotica [74]. Deze factoren zouden de observaties van Allen et al. deels kunnen verklaren. Bovendien werden de antibiotica in de studie van Allen et al. toegediend voor een periode van maximaal zeven dagen voor het begin van de probioticabehandeling. Probiotica zijn mogelijk effectiever in preventie van AGD als zij gedurende de gehele periode van blootstelling aan antibiotica worden toegediend. Dit beeld wordt bevestigd in een meta-regressieanalyse van Shen et al. waarin wordt aangetoond dat probiotica effectiever zijn in de preventie van Clostridum difficile infecties als zij kort na de eerste antibioticumdosis worden toegediend [82].
De effectiviteit van probiotica ter preventie van AGD hangt ook af van de dosis. Een dagelijkse inname van minstens 5 miljard kve is geassocieerd met een verlaagd risico op AGD [35,36]. Een hogere dosis correleert met een hogere effectiviteit [50,74]. Slechts een klein aantal dosiseffectstudies zijn uitgevoerd, maar zij laten een duidelijke correlatie zien tussen dosering en een verlaagd risico op AGD [83].
Aangezien vele factoren de effectiviteit van probiotica als profylaxe beïnvloeden, zouden onderzoekers zorgvuldig te werk moeten gaan in het beschrijven van de relevante condities van het klinisch onderzoek waardoor studies beter met elkaar vergeleken kunnen worden. Studies zouden alle kenmerken moeten beschrijven van het gebruikte probioticum (stam, dosering en duur van de therapie), het antibioticum (type, dosering en duur van de therapie), de patiënten (leeftijdsgroep, diagnose) en nauwkeurige definities van de gemeten resultaten en bijwerkingen. Daarnaast kunnen individuele factoren, die niet routinematig worden bepaald in klinische studies, van invloed zijn op de effectiviteit van probiotica. Elk individu beschikt over unieke microbiota die een uniek microbieel ecosysteem vormen in de darmen. De impact van een antibioticum op de samenstelling en stabiliteit van dit ecosysteem zal dus verschillend zijn en een specifieke probiotische stam of combinatie van stammen zullen dus niet dezelfde effectiviteit hebben in elk individu. In het bijzonder voor patiënten die regelmatig met antibiotica worden behandeld – zoals patiënten op hoge leeftijd – kan het waardevol zijn flexibel te zijn en verschillende probiotica te proberen tot een effectieve formulering is gevonden. Meer onderzoek is nodig om aanbevelingen te kunnen formuleren voor op maat gemaakte, oftewel gepersonaliseerde therapie.
Conclusie
We presenteren hier een methodologie voor de beoordeling van effectiviteit van probiotica bij het voorkomen van antibiotica-gerelateerde diarree. Deze methodologie kan breder worden toegepast en bestaat uit drie stappen: meta-analyse van relevante klinische onderzoeken, inventarisatie van beschikbare producten en formulering van op wetenschappelijke feiten gebaseerde aanbevelingen. We concluderen dat er voldoende bewijs is om een aanbeveling te doen voor het gebruik van specifieke probiotische producten ter voorkoming van antibiotica-gerelateerde diarree. In het bijzonder geven we een aanbeveling van drie sterren aan producten met een minimale dosis van 2 miljard kve van de probiotische stam Lactobacillus rhamnosus GG.
Verantwoording
De auteurs danken Prof. Dr. Michiel Kleerebezem (Wageningen University en Research, Host-Microbe Interactomics group) voor het kritisch lezen van het manuscript. We danken Eveline Hensel, Jasper Buikx, Janna Laeven en Haig Balian van ARTIS-Micropia voor hun bijdrage aan deze Nederlandse gids voor probiotica.
Geen belangenverstrengeling gemeld.
Dit artikel is een bewerkte vertaling van: Agamennone V, Krul CAM, Rijkers G, Kort R. A practical guide for probiotics applied to the case of antibiotic-associated diarrhea in The Netherlands. BMC Gastroenterol. 2018 Aug 6;18(1):103. doi: 10.1186/s12876-018-0831-x.
Literatuur
1. Holstiege J, Schink T, Molokhia M, Mazzaglia G, Innocenti F, Oteri A, et al. Systemic antibiotic prescribing to paediatric outpatients in 5 European countries: a population-based cohort study. BMC Pediatr. 2014;14:174.
2. Adriaenssens N, Coenen S, Kroes ACM, Versporten A, Vankerckhoven V, Muller A, et al. European Surveillance of Antimicrobial Consumption (ESAC): outpatient antibiotic use in Europe (1997–2009). J. Antimicrob. Chemother. 2011;66:vi3-vi12.
3. Haeseker MB, Dukers-Muijrers NHTM, Hoebe CJPA, Bruggeman CA, Cals JWL, Verbon A. Trends in Antibiotic Prescribing in Adults in Dutch General Practice. PLoS One. 2012;7.
4. van den Broek d’Obrenan J, Verheij TJM, Numans ME, van der Velden AW. Antibiotic use in Dutch primary care: Relation between diagnosis, consultation and treatment. J. Antimicrob. Chemother. 2014;69:1701–7.
5. Zarb P, Amadeo B, Muller A, Drapier N, Vankerckhoven V, Davey P, et al. Antimicrobial prescribing in hospitalized adults stratified by age. Drugs Aging. 2012;29:53–62.
6. Akkerman AE, van der Wouden JC, Kuyvenhoven MM, Dieleman JP, Verheij TJM. Antibiotic prescribing for respiratory tract infections in Dutch primary care in relation to patient age clinical entities. J. Antimicrob. Chemother. 2004;54:1116–21.
7. Dekker ARJ, Verheij TJM, van der Velden AW. Inappropriate antibiotic prescription for respiratory tract indications: Most prominent in adult patients. Fam. Pract. 2015;32:401–7.
8. Dik J-WH, Sinha B, Friedrich AW, Lo-Ten-Foe JR, Hendrix R, Köck R, et al. Cross-border comparison of antibiotic prescriptions among children and adolescents between the north of the Netherlands and the north-west of Germany. Antimicrob. Resist. Infect. Control. Antimicrobial Resistance & Infection Control; 2016;5:14.
9. Turck D, Bernet J-P, Marx J, Kempf H, Giard P, Walbaum O, et al. Incidence and risk factors of oral antibiotic-associated diarrhea in an outpatient pediatric population. J. Pediatr. Gastroenterol. Nutr. 2003;37:22–6.
10. Wiström J, Norrby SR, Myhre EB, Eriksson S, Granström G, Lagergren L, et al. Frequency of antibiotic-associated diarrhoea in 2462 antibiotic-treated hospitalized patients: a prospective study. J. Antimicrob. Chemother. 2001;47:43–50.
11. Kramer MS, Hutchinson TA, Naimark L, Contardi R, Flegel KM, Leduc DG. Antibiotic-associated gastrointestinal symptoms in general pediatric outpatients. Pediatrics. 1985;76:365–70.
12. Kuyvenhoven MM, van Balen FAM, Verheij TJM. Outpatient antibiotic prescriptions from 1992 to 2001 in The Netherlands. J. Antimicrob. Chemother. 2003;52:675–8.
13. GIP/ZorgInstituut Nederland [Internet]. 2016. Beschikbaar op: https://www.gipdatabank.nl/
14. Griens JM; Kroon JDL; Lukaart JS; van der Vaart RJ; AJ. Data en feiten 2016 – Het jaar 2015 in cijfers. 2016.
15. Akhloufi H, Streefkerk RH, Melles DC, de Steenwinkel JEM, Schurink CAM, Verkooijen RP, et al. Point prevalence of appropriate antimicrobial therapy in a Dutch university hospital. Eur. J. Clin. Microbiol. Infect. Dis. 2015;34:1631–7.
16. Little P, Stuart B, Moore M, Coenen S, Butler CC, Godycki-Cwirko M, et al. Amoxicillin for acute lower-respiratory-tract infection in primary care when pneumonia is not suspected: A 12-country, randomised, placebo-controlled trial. Lancet Infect. Dis. Elsevier Ltd; 2013;13:123–9.
17. Francino MP. Antibiotics and the human gut microbiome: Dysbioses and accumulation of resistances. Front. Microbiol. 2016;6:1–11.
18. Sarker P, Mily A, Mamun A, Jalal S, Bergman P, Raqib R, et al. Ciprofloxacin affects host cells by suppressing expression of the endogenous antimicrobial peptides cathelicidins and beta-defensin-3 in colon epithelia. Antibiotics. 2014;3:353–74.
19. Al-Jashaami LS, DuPont HL. Management of Clostridium difficile infection. Gastroenterol. Hepatol. 2016;12:609–16.
20. Young VB, Schmidt TM. Antibiotic-associated diarrhea accompanied by large-scale alterations in the composition of the fecal microbiota. 2004;42:1203–6.
21. Doron SI, Hibberd PL, Gorbach SL. Probiotics for prevention of antibiotic-associated diarrhea. Prevention. 2008;42:58–63.
22. McFarland L V. Antibiotic-associated diarrhea: epidemiology, trends and treatment. Future Microbiol. 2008;3:563–78.
23. McFarland LV, Ozen M, Dinleyici EC, Goh S. Comparison of pediatric and adult antibiotic-associated diarrhea and Clostridium difficile infections. World J. Gastroenterol. 2016;22:3078–104.
24. Keeney KM, Yurist-Doutsch S, Arrieta M-C, Finlay BB. Effects of antibiotics on human microbiota and subsequent disease. Annu. Rev. Microbiol. 2014;68:217–35.
25. Croswell A, Amir E, Teggatz P, Barman M, Salzman NH. Prolonged impact of antibiotics on intestinal microbial ecology and susceptibility to enteric Salmonella infection. Infect. Immun. 2009;77:2741–53.
26. Jernberg C, Löfmark S, Edlund C, Jansson JK. Long-term ecological impacts of antibiotic administration on the human intestinal microbiota. ISME J. 2007;1:56–66.
27. Bokulich NA, Chung J, Battaglia T, Henderson N, Li H, Lieber A, et al. Antibiotics, birth mode, and diet shape microbiome maturation during early life. Sci. Transl. Med. 2017;8.
28. Schulfer A, Blaser MJ. Risks of antibiotic exposures early in life on the developing microbiome. PLOS Pathog. 2015;11:e1004903.
29. Bailey LC, Forrest CB, Zhang P, Richards TM, Livshits A, DeRusso PA. Association of antibiotics in infancy with early childhood obesity. JAMA Pediatr. 2014;168:1063–9.
30. Love BL, Mann JR, Hardin JW, Lu ZK, Cox C, Amrol DJ. Antibiotic prescription and food allergy in young children. Allergy, asthma, Clin. Immunol. 2016;12:41.
31. Risnes KR, Belanger K, Murk W, Bracken MB. Antibiotic exposure by 6 months and asthma and allergy at 6 years: Findings in a cohort of 1,401 US children. Am. J. Epidemiol. 2011;173:310–8.
32. Clausen TD, Bergholt T, Bouaziz O, Arpi M, Eriksson F, Rasmussen S, et al. Broad-spectrum antibiotic treatment and subsequent childhood type 1 diabetes: A nationwide Danish cohort study. PLoS One. 2016;11:1–15.
33. Joint FAO/WHO expert consultation. Health and nutrition properties of probiotics in food including powder milk with live lactic acid bacteria. 2001.
34. Hill C, Guarner F, Reid G, Gibson GR, Merenstein DJ, Pot B, et al. Expert consensus document: The international scientific association for probiotics and prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nat. Rev. Gastroenterol. Hepatol. 2014;11:506–14.
35. Hayes SR, Vargas AJ. Probiotics for the prevention of pediatric antibiotic-associated diarrhea. Explor. J. Sci. Heal. 2016;12:463–6.
36. McFarland L V. Meta-analysis of probiotics for the prevention of antibiotic associated diarrhea and the treatment of Clostridium difficile disease. Am. J. Gastroenterol. 2006;101:812–22.
37. Sanchez B, Bressollier P, Urdaci MC. Exported proteins in probiotic bacteria: Adhesion to intestinal surfaces, host immunomodulation and molecular cross-talking with the host. FEMS Immunol. Med. Microbiol. 2008;54:1–17.
38. Collado MC, González A, González R, Hernández M, Ferrús MA, Sanz Y. Antimicrobial peptides are among the antagonistic metabolites produced by Bifidobacterium against Helicobacter pylori. Int. J. Antimicrob. Agents. 2005;25:385–91.
39. Chu W, Lu F, Zhu W, Kang C. Isolation and characterization of new potential probiotic bacteria based on quorum-sensing system. J. Appl. Microbiol. 2011;110:202–8.
40. Cotter PD, Hill C, Ross RP. Bacteriocins: developing innate immunity for food. Nat. Rev. Microbiol. 2005;3:777–88.
41. Servin AL. Antagonistic activities of lactobacilli and bifidobacteria against microbial pathogens. FEMS Microbiol. Rev. 2004;28:405–40.
42. Ashraf R, Shah NP. Immune system stimulation by probiotic microorganisms. Crit. Rev. Food Sci. Nutr. 2014;54:938–56.
43. Hempel S, Newberry S, Ruelaz A, Wang Z, Miles JN V, Suttorp MJ, et al. Safety of probiotics used to reduce risk and prevent or treat disease. 2011.
44. van den Nieuwboer M, Brummer RJ, Guarner F, Morelli L, Cabana M, Claassen E. Safety of probiotics and synbiotics in children under 18 years of age. Benef. Microbes. 2015;6:615–30.
45. Arvola T, Laiho K, Torkkeli S, Mykkanen H, Salminen S, Maunula L, et al. Prophylactic Lactobacillus GG reduces antibiotic-associated diarrhea in children with respiratory infections : a randomized study. Pediatrics. 1999;104:e64.
46. Beausoleil M, Fortier N, Guénette S, L’Ecuyer A, Savoie M, Franco M, et al. Effect of a fermented milk combining Lactobacillus acidophilus CL1285 and Lactobacillus casei in the prevention of antibiotic-associated diarrhea: A randomized, double-blind, placebo-controlled trial. Can. J. Gastroenterol. 2007;21:732–6.
47. Cimperman L, Bayless G, Best K, Diligente A, Mordarski B, Oster M, et al. A randomized, double-blind, placebo-controlled pilot study of Lactobacillus reuteri ATCC 55730 for the prevention of antibiotic-associated diarrhea in hospitalized adults. J. Clin. Gastroenterol. 2011;45:785–9.
48. Correa NB, Peret Filho LA, Penna FJ, Lima FM, Nicoli JR. A randomized formula controlled trial of Bifidobacterium lactis and Streptococcus thermophilus for prevention of antibiotic-associated diarrhea in infants. J. Clin. Gastroenterol. 2005;39:385–9.
49. Fox MJ, Ahuja KDK, Robertson IK, Ball MJ, Eri RD. Can probiotic yogurt prevent diarrhoea in children on antibiotics? A double-blind, randomised, placebo-controlled study. BMJ Open. 2015;5:e006474.
50. Gao XW, Mubasher M, Fang CY, Reifer C, Miller LE. Dose-response efficacy of a proprietary probiotic formula of Lactobacillus acidophilus CL1285 and Lactobacillus casei LBC80R for antibiotic-associated diarrhea and Clostridium difficile-associated diarrhea prophylaxis in adult patient. Am. J. Gastroenterol. Nature Publishing Group; 2010;105:1636–41.
51. Georgieva M, Pancheva R, Rasheva N, Usheva N, Ivanova L, Koleva K. Use of the probiotic Lactobacillus reuteri DSM 17938 in the prevention of antibiotic-associated infections in hospitalized Bulgarian children: a randomized, controlled trial. J. IMAB – Annu. Proceeding. 2015;21:895–900.
52. Hickson M, D’Souza AL, Muthu N, Rogers TR, Want S, Rajkumar C, et al. Use of probiotic Lactobacillus preparation to prevent diarrhoea associated with antibiotics: randomised double blind placebo controlled trial. BMJ. 2007;335:80.
53. Koning C, Jonkers D, Smidt H, Rombouts F, Pennings H, Wouters E, et al. The effect of a multispecies probiotic on the composition of the faecal microbiota and bowel habits in chronic obstructive pulmonary disease patients treated with antibiotics. Br J Nutr. 2009;1–9.
54. Koning C, Jonkers D, Stobberingh E, Mulder L, Rombouts F, Stockbrügger R. The effect of a multispecies probiotic on the intestinal microbiota and bowel movements in healthy volunteers taking the antibiotic amoxycillin. Am. J. Gastroenterol. 2008;103:178–89.
55. Kotowska M, Albrecht P, Szajewska H. Saccharomyces boulardii in the prevention of antibiotic-associated diarrhoea in children: A randomized double-blind placebo-controlled trial. Aliment. Pharmacol. Ther. 2005;21:583–90.
56. Lewis SJ, Potts L., Barry RE. The lack of therapeutic effect of Saccharomyces boulardii in the prevention of antibiotic-related diarrhoea in elderly patients. J. Infect. 1998;36:171–4.
57. Lönnermark E, Friman V, Lappas G, Sandberg T, Berggren A, Adlerberth I. Intake of Lactobacillus plantarum reduces certain gastrointestinal symptoms during treatment with antibiotics. J. Clin. Gastroenterol. 2010;44:106–12.
58. McFarland L, Surawicz C, Greenberg R, Elmer GW, Moyer K, Melcher S, et al. Prevention of ß-lactam associated diarrhea by Saccharomyces boulardii compared with placebo. Am. J. Gastroenterol. 1995;90:439–48.
59. Myllyluoma E, Veijola L, Ahlroos T, Tynkkynen S, Kankuri E, Vapaatalo H, et al. Probiotic supplementation improves tolerance to Helicobacter pylori eradication therapy – A placebo-controlled, double-blind randomized pilot study. Aliment. Pharmacol. Ther. 2005;21:1263–72.
60. Pozzoni P, Riva A, Bellatorre A, Amigoni M, Redaelli E, Ronchetti A, et al. Saccharomyces boulardii for the prevention of antibiotic-associated diarrhea in adult hospitalized patients: a single-center, randomized, double-blind, placebo-controlled trial. Am. J. Gastroenterol. 2012;107:922–31.
61. Ruszczyński M, Radzikowski A, Szajewska H. Clinical trial: Effectiveness of Lactobacillus rhamnosus (strains E/N, Oxy and Pen) in the prevention of antibiotic-associated diarrhoea in children. Aliment. Pharmacol. Ther. 2008;28:154–61.
62. Safdar N, Barigala R, Said A, McKinley L. Feasibility and tolerability of probiotics for prevention of antibiotic-associated diarrhoea in hospitalized US military veterans. J. Clin. Pharm. Ther. 2008;33:663–8.
63. Sampalis J, Psaradellis E, Rampakakis E. Efficacy of BIO K+ CL1285® in the reduction of antibiotic-associated diarrhea – A placebo controlled double-blind randomized, multi-center study. Arch. Med. Sci. 2010;6:56–64.
64. Song HJ, Kim J-Y, Jung S-A, Kim S-E, Park H-S, Jeong Y, et al. Effect of probiotic Lactobacillus (Lacidofil® cap) for the prevention of antibiotic-associated diarrhea: a prospective, randomized, double-blind, multicenter study. J. Korean Med. Sci. 2010;25:1784–91.
65. Surawicz CM, Elmer GW, Speelman P, McFarland L V, Chinn J, van Belle G. Prevention of antibiotic-associated diarrhea by Saccharomyces boulardii: a prospective study. Gastroenterology. 1989;96:981–8.
66. Szajewska H, Albrecht P, Topczewska-cabanek A. Randomized, double-blind, placebo-controlled trial: Effect of Lactobacillus GG supplementation on Helicobacter pylori eradication rates and side effects during treatment in children. 2009;431–6.
67. Szymański H, Armańska M, Kowalska-Duplaga K, Szajewska H. Bifidobacterium longum PL03, Lactobacillus rhamnosus KL53A, and Lactobacillus plantarum PL02 in the prevention of antibiotic-associated diarrhea in children: A randomized controlled pilot trial. Digestion. 2008;78:13–7.
68. Tankanow RM, Ross MB, Ertel IJ, Dickinson DG, McCormick LS, Garfinkel JF. A double-blind, placebo-controlled study of the efficacy of Lactinex in the prophylaxis of amoxicillin-induced diarrhea. Dicp. 1990;24:382–4.
69. Vanderhoof J a, Whitney DB, Antonson DL, Hanner TL, Lupo J V, Young RJ. Lactobacillus GG in the prevention of antibiotic-associated diarrhea in children. J. Pediatr. 1999;135:564–8.
70. Wenus C, Goll R, Loken EB, Biong AS, Halvorsen DS, Florholmen J. Prevention of antibiotic-associated diarrhoea by a fermented probiotic milk drink. Eur. J. Clin. Nutr. 2008;62:299–301.
71. Allen SJ, Wareham K, Wang D, Bradley C, Hutchings H, Harris W, et al. Lactobacilli and bifidobacteria in the prevention of antibiotic-associated diarrhoea and Clostridium difficile diarrhoea in older inpatients (PLACIDE): a randomised, double-blind, placebo-controlled, multicentre trial. Lancet. 2013;382:1249–57.
72. Chatterjee S, Kar P, Das T, Ray S, Ganguly S, Rajendiran C, et al. Randomized placebo-controlled double blind multicentric trial on efficacy and safety of Lactobacillus acidophilus LA-5 and Bifidobacterium BB-12 for prevention of antibiotic-associated diarrhea. J. Assoc. Physicians India. 2013;61:708–12.
73. Evans M, Salewski RP, Christman MC, Girard S-A, Tompkins TA. Effectiveness of Lactobacillus helveticus and Lactobacillus rhamnosus for the management of antibiotic-associated diarrhoea in healthy adults: a randomised, double-blind, placebo-controlled trial. Br. J. Nutr. 2016;116:94–103.
74. Ouwehand AC, DongLian C, Weijian X, Stewart M, Ni J, Stewart T, et al. Probiotics reduce symptoms of antibiotic use in a hospital setting: A randomized dose response study. Vaccine. 2014;32:458–63.
75. Patel J, Curry WJ, Graybill MA, Bernard S, Mcdermott AS, Karpa K. Randomized study of probiotics in primary care. J. Pharm. Heal. Serv. Res. 2014;5:187–90.
76. Selinger CP, Bell A, Cairns A, Lockett M, Sebastian S, Haslam N. Probiotic VSL#3 prevents antibiotic-associated diarrhoea in a double-blind, randomized, placebo-controlled clinical trial. J. Hosp. Infect. 2013;84:159–65.
77. Douillard FP, Kant R, Ritari J, Paulin L, Palva A, De Vos WM. Comparative genome analysis of Lactobacillus casei strains isolated from Actimel and Yakult products reveals marked similarities and points to a common origin. Microb. Biotechnol. 2013;6:576–87.
78. Szajewska H, Canani RB, Guarino A, Hojsak I, Indrio F, Kolacek S, et al. Probiotics for the prevention of antibiotic-associated diarrhea in children. J. Pediatr. Gastroenterol. Nutr. 2016;62:495–506.
79. Horvath A, Dziechciarz P, Szajewska H. Meta-analysis: Lactobacillus rhamnosus GG for abdominal pain-related functional gastrointestinal disorders in childhood. Aliment. Pharmacol. Ther. 2011;33:1302–10.
80. Ritchie ML, Romanuk TN. A meta-analysis of probiotic efficacy for gastrointestinal diseases. PLoS One. 2012;7.
81. Sybesma W, Molenaar D, van IJcken W, Venema K, Kort R. Genome instability in Lactobacillus rhamnosus GG. Appl. Environ. Microbiol. 2013;79:2233–9.
82. Shen NT, Maw A, Tmanova LL, Pino A, Ancy K, Crawford C V., et al. Timely use of probiotics in hospitalized adults prevents Clostridium difficile infection: a systematic review with meta-regression analysis. Gastroenterology. Elsevier, Inc; 2017;152:1889–1900.e9.
83. Ouwehand AC. A review of dose-responses of probiotics in human studies. Benef. Microbes. 2016;1–10.
Referentie
Citeer als: Agamennone V, Krul CAM, Rijkers G, Kort R. Een praktische gids voor probiotica ter preventie van antibiotica-gerelateerde diarree in Nederland. Nederlands Platform voor Farmaceutisch Onderzoek. 2019;4:a1689.
DOI
https://www.knmp.nl/resolveuid/12bc89e5ee4d4f70b0d3a898ebe7093fOpen access

Reactie toevoegen