Doseerhomogeniteit van meer dan honderd SyrSpend SF suspensies onderzocht na bewaren
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2022;7:a1757
Kernpunten
- Bij kinderen en ouderen blijft behoefte aan medicatie op maat.
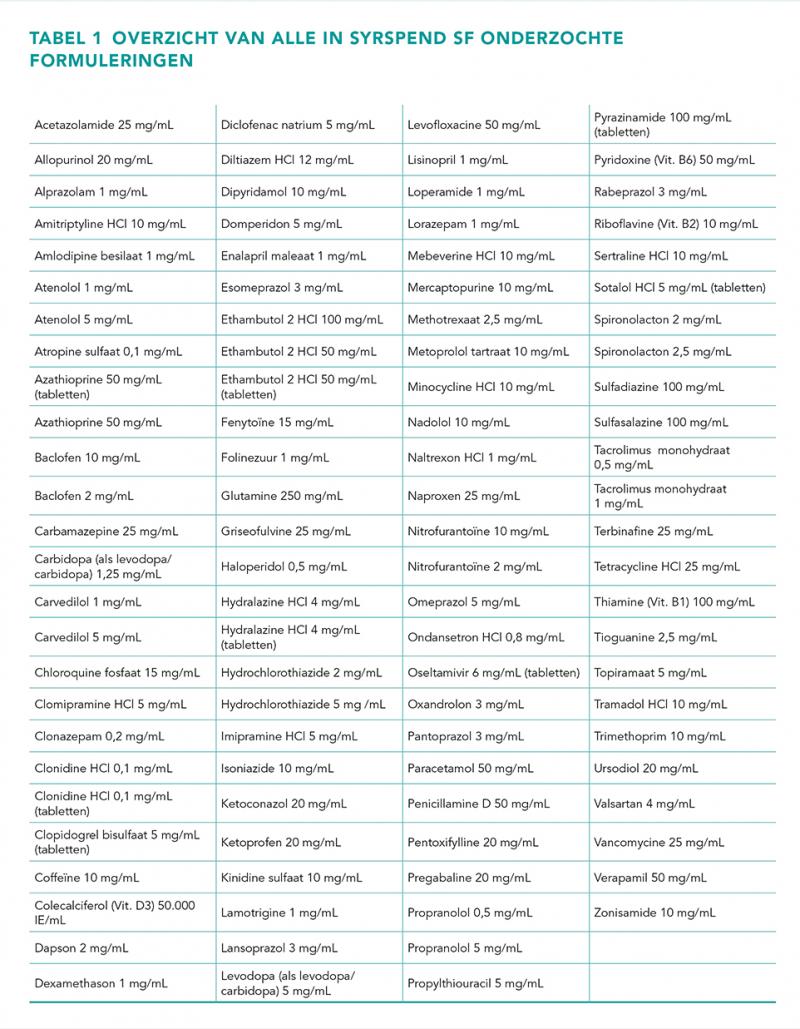
- In deze studie werden 104 verschillende formuleringen in SyrSpend SF onderzocht.
- Alle 104 formuleringen (89 unieke actieve stoffen, 6414 geanalyseerde monsters) voldeden na bewaren ruimschoots aan de eisen zoals gesteld in de monografie Unlicensed Medicines: Oral Suspensions - Homogeneity of Suspension van de Britse Farmacopee.
Abstract
Homogeneity in over 100 different SyrSpend SF suspensions tested after storage
Introduction
There is still an evident need for non-sterile compounded medications for paediatric and elderly patients in cases where patients require dose adjustments or have swallowing difficulties. Pharmacists generally have the choice between compounding capsules or oral liquids. In daily pharmacy practice, extemporaneous capsules are, from time to time, seen as a better alternative to oral liquid medication. However, various published studies also indicate that weight variation and content uniformity can be significantly out of specification for compounded capsules.
Objective
To investigate the homogeneity and resuspendability of SyrSpend SF suspensions.
Methods
HPLC analysis with the ready-to-use oral liquid vehicle SyrSpend SF was performed in 104 different formulations with 89 unique active pharmaceutical ingredients (6,414 individual samples).
Conclusion
All samples in SyrSpend SF were compliant with the specifications set by the British Pharmacopoeia monograph Unlicensed Medicines: Oral Suspensions - Homogeneity of Suspension.
Inleiding
Bij de behandeling van kinderen en ouderen met geneesmiddelen doen zich specifieke farmaceutische problemen voor. Bij geriatrische patiënten moet de dosering vaak worden aangepast vanwege leeftijdsgerelateerde fysiologische veranderingen in farmacokinetiek, waaronder de opname, verspreiding en uitscheiding van geneesmiddelen [1]. Bij kinderen is tijdens de ontwikkeling sprake van grote veranderingen in gewicht en lichaamsgrootte. Wanneer ze eenmaal volgroeid zijn, kunnen ze twintig keer zwaarder zijn dan bij hun geboorte en tot wel een honderdvoudige dosering nodig hebben [2,3]. Bovendien kan bij pediatrische patiënten de biologische beschikbaarheid van een geneesmiddel variëren doordat het absorptieoppervlak tijdens de groei verandert [4]. Dysfagie, moeite met slikken, is een andere reden om medicatie bij kinderen en ouderen aan te passen. Voor kinderen tot zes jaar zijn gangbare toedieningsvormen dikwijls ongeschikt, en 25% tot 45% van de kinderen lijdt aan dysfagie [5,6].
Het aantal toedieningsvormen dat speciaal is bedoeld voor kinderen en ouderen neemt weliswaar toe, maar veel geneesmiddelen moeten nog steeds op kleine schaal of op individuele basis door (ziekenhuis)apothekers worden bereid voor deze doelgroepen. In dergelijke gevallen zullen apothekers doorgaans capsules maken of kiezen voor orale vloeistoffen. Oplossingen en suspensies hebben als voordeel dat ze relatief snel kunnen worden klaargemaakt en de dosering gemakkelijk is aan te passen, maar voor apothekers is het vaak lastiger formuleringen te vinden waarbij de fysische en chemische stabiliteit voldoende is onderbouwd. Veel Active Pharmaceutical Ingredients (API’s) zijn slechts beperkt oplosbaar, waardoor een suspensie wordt gevormd. Het risico van suspensies is het irreversibele uitzakken, het zogenaamde ‘caking’. Daarnaast bestaat voor suspensies de kans dat, wanneer geproduceerd in grotere hoeveelheden en het actieve ingrediënt in kleine hoeveelheden aanwezig is, segregatie optreedt tijdens bereiding [7-9]. Om deze redenen en de langere houdbaarheid, wordt soms de voorkeur gegeven aan handmatig bereide capsules boven orale vloeistoffen.
Om de veilige en nauwkeurige toediening van handmatig bereide geneesmiddelen te garanderen, moet het gehalte van de werkzame stoffen binnen de grenzen blijven, zoals die worden gesteld door de geldende farmacopees. Apothekers beschikken doorgaans over twee testen om te bepalen of de bereide geneesmiddelen aan de vereisten voldoen en dus betrouwbaar zijn: 1) gewichtsvariatie en 2) gelijkmatigheid van gehalte [10,11]. De in de Europese Farmacopee (Ph. Eur.) en Amerikaanse Farmacopee (USP) beschreven monografieën voor gelijkmatigheid van gehalte (Content Uniformity [CU]) zijn uitsluitend van toepassing op toedieningsvormen voor enkelvoudige dosering [10,11]. De Britse Farmacopee (BP) daarentegen, heeft een specifieke monografie om de doseerhomogeniteit na resuspenderen van orale suspensies te beoordelen [12]. De testen op gewichtsvariatie en gelijkmatigheid van gehalte van capsules zijn in de verschillende farmacopees grotendeels geharmoniseerd [10-12].
SyrSpend SF is een kant-en-klare suspensiebasis met specifieke reologische eigenschappen die een constante dosering garanderen. De thixotropische eigenschappen van de basis voorkomen het neerslaan van API’s, door de viscositeit te vergroten wanneer de vloeistof stilstaat. De pseudoplasticiteit van SyrSpend SF vergemakkelijkt homogenisering door verlaging van de viscositeit, wanneer de vloeistof wordt geschud [13].
In dit artikel bespreken we de doseerhomogeniteit na resuspenderen van meer dan honderd verschillende formuleringen in SyrSpend SF, bewaard in de koelkast en bij kamertemperatuur. Deze studie is een vervolg op een eerdere publicatie waarin de CU van een beperkt aantal API’s in SyrSpend SF was beschreven [14].
Methoden
Voor de bereiding van de suspensies met de actieve component is, waar mogelijk, gebruikgemaakt van grondstoffen. De grondstoffen werden geleverd door Fagron (St. Paul, Minnesota, USA). Indien een grondstof niet beschikbaar was, werd gebruikgemaakt van het geregistreerde handelspreparaat. In deze gevallen staat dat duidelijk aangegeven in tabel 1. Ongeacht de herkomst van de actieve stof (grondstof of handelspreparaat) zijn de suspensies op de volgende wijze verkregen [15-36]:
- De benodigde hoeveelheid van alle componenten werd berekend.
- Elk ingrediënt werd nauwkeurig afgewogen.
- De actieve stof werd met behulp van mortier en stamper gemalen tot een fijn poedermengsel.
- Een kleine hoeveelheid SyrSpend SF PH4 (vloeibaar) werd aan het poedermengsel toegevoegd en gemengd tot een uniforme pasta.
- De resterende hoeveelheid SyrSpend SF PH4 (vloeibaar) werd in gelijke delen toegevoegd, waarbij na elke toevoeging het mengsel goed gehomogeniseerd werd.
- Tenslotte werd SyrSpend SF PH4 (vloeibaar) toegevoegd tot een volume van 300 mL.
- Het eindproduct werd vervolgens verpakt in een lichtresistente, zuurarme farmaceutische verpakking en gelabeld.
- De suspensies werden onmiddellijk geanalyseerd (t = 0).
- De monsters werden gesplitst in koelkasttemperatuur (2-8 °C) en kamertemperatuur (15-25 °C).
- Temperatuur en luchtvochtigheid werden gedurende het gehele experiment gemeten.
Alle data zijn verkregen in één enkel ISO (Internationale Organisatie voor Standaardisatie) en GLP (Goede Laboratorium Praktijken) gecertificeerd laboratorium. De stabiliteit van elk afzonderlijke API in SyrSpend SF is bepaald door gedurende negentig dagen op verschillende momenten te meten hoeveel procent van de werkzame stof nog in de vloeistof aanwezig was. De metingen werden uitgevoerd met behulp van hogedrukvloeistofchromatografie (HPLC) met UV-detectie en hielden rekening met mogelijke degradatie van de actieve component. Er werd – waar mogelijk – gebruikgemaakt van de analyseprotocollen zoals beschreven in de USP [11]. Het onderzoek vond plaats volgens, in overeenstemming met de International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use (ICH)-richtlijnen [37]. Tijdens validatie van de HPLC-analyse, werden de monsters op verschillende manieren bewerkt: met zuur, base, ultraviolet licht, verhitting en oxidatie (‘geforceerde degradatie’). Dit om er zeker van te kunnen zijn dat degradatieproducten gescheiden konden worden van de actieve component. Het gehalte van de monsters werd bepaald met behulp van HPLC, op vooraf vastgestelde tijdspunten. De onderzochte formuleringen werden voor analyse één minuut met de hand geschud. De 60 seconden schudden is langer dan de 30 seconden die beschreven staan in de BP [12] of de bereidingsinstructies van de SyrSpend SF kits, maar hiervoor is gekozen om inhomogeniteit zoveel mogelijk uit te sluiten als oorzaak voor een mogelijk lager gehalte.
Voor de metingen werden volumetrisch monsters genomen uit het midden van de fles, zonder het binnenoppervlak van de fles aan te raken. Ze werden verdund om werkoplossingen te verkrijgen zoals eerder beschreven [15-36]. De monsters werden op verschillende momenten genomen: op dag 0 (basislijn), 7, 14, 30, 60 en op dag 90. Bij elf monsters die al eerder bij een andere concentratie waren bestudeerd en die een goede fysisch-chemische compatibiliteit lieten zien, werd het gehalte uitsluitend op dag 0, 30, 60 en 90 bepaald. Alle bepalingen werden per tijdspunt in zesvoud gemeten. Uit deze metingen werd het percentage van de werkzame stof dat nog in de vloeistof aanwezig was ten opzichte van t = 0 (zoals vastgesteld met HPLC) bepaald. Daarnaast werden het gemiddelde en de standaarddeviatie van alle bepalingen berekend [15-36].
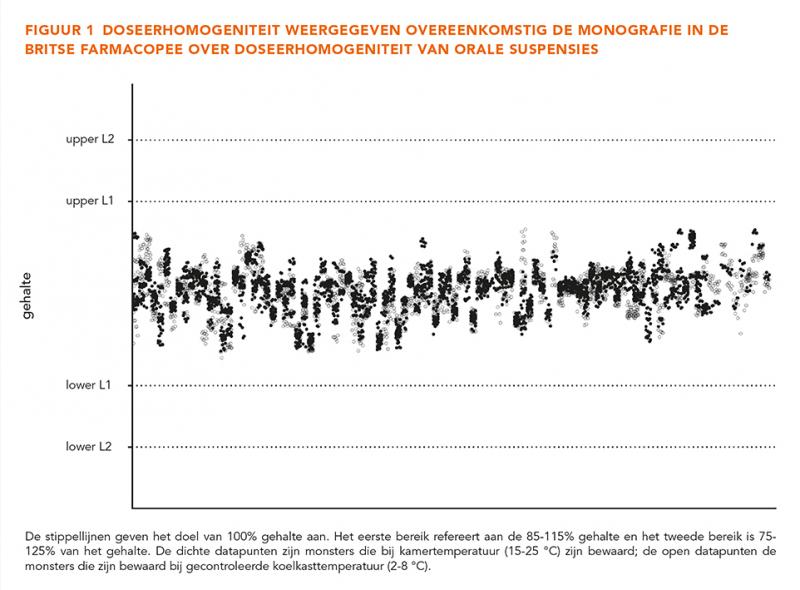
Zoals in de inleiding aangegeven, beschrijft alleen de BP eisen voor de homogeniteit van orale suspensies. De geanalyseerde data zijn dan ook geëvalueerd op basis van deze monografie. De BP-monografie Unlicensed Medicines: Oral Suspensions - Homogeneity of Suspension stelt dat de homogeniteit na resuspenderen van een orale suspensie voldoet, als alle 10 de geanalyseerde monsters zich tussen 85% en 115% van de gemiddelde dosis bevinden. Het preparaat voldoet niet aan de eisen als meer dan één meting buiten deze grenzen valt of als één afzonderlijke dosis buiten de grenzen van 75% tot 125% valt [12].
Resultaten
In deze studie werden 104 verschillende formuleringen bestudeerd met 89 unieke API’s. In totaal werden 6414 verschillende monsters geanalyseerd, waarvan de meeste werden getest bij zowel kamer- (15-25 °C) als koelkasttemperatuur (2-8 °C). Een volledig overzicht van de verschillende geteste formuleringen en bijbehorende concentratie is te vinden in tabel 1. Data-analyse werd uitgevoerd overeenkomstig de BP-monografie Unlicensed Medicines: Oral Suspensions - Homogeneity of Suspension. Alle waarden, van alle API’s, vielen ruim binnen de eis (85-115% van het opgegeven gehalte). De gemiddelde concentratie van alle monsters was 100,30% en 100,34% voor respectievelijk kamer- en koelkasttemperatuur. Alle 6414 afzonderlijke datapunten zijn weergegeven in figuur 1.
Beschouwing
De actieve componenten, onderzocht in SyrSpend SF, laten een goede fysisch-chemische stabiliteit zien. Enerzijds wordt dit verklaard door het feit dat – door keuze van de chemische vorm – een deel van de actieve componenten zeer beperkt oplosbaar is in water en als zodanig beperkt reactief is. Anderzijds is de pH, naast temperatuur, een belangrijke bepalende factor voor de stabiliteit van een geneesmiddel door hydrolytische degradatie. De pH kan een katalyserende werking hebben op de rol die waterstof- en hydroxide-ionen spelen in diverse reacties en daarmee op de snelheid waarmee een geneesmiddel degradeert. De degradatie van actieve componenten door hydrolyse of oxidatie is direct gerelateerd aan de concentratie van waterstof- en hydroxyde-ionen. Over het algemeen vinden deze reacties frequenter plaats in een neutraal of alkalisch milieu. Voor de meeste hydrolyseerbare geneesmiddelen geldt dat ze het meest stabiel zijn in een licht zuur milieu (pH 5-6). Fenolbevattende geneesmiddelen, zoals bepaalde amines, oxideren snel bij een neutrale of licht alkalische pH. Deze reactie vindt echter veel trager plaats bij een pH onder de 4 [38-44].
Binnen de farmacie wordt steeds meer aandacht besteed aan de veiligheid van kindermedicatie [45,46]. Dat is ook terecht, want veel geneesmiddelen hebben een smal therapeutisch venster waardoor kleine afwijkingen van het gehalte verstrekkende gevolgen kunnen hebben voor de patiëntveiligheid. Uit dit onderzoek blijkt dat met SyrSpend SF alle meer dan 6000 onderzochte monsters binnen de specificaties voor doseerhomogeniteit vallen, ongeacht de gebruikte API, de bewaaromstandigheden of het moment van analyse.
Zoals in de inleiding beschreven, wordt in de praktijk vaak voor capsules gekozen vanwege het risico op uitzakken van suspensies. Uit de literatuur blijkt echter dat ook op kleine schaal, handmatig bereide capsules buiten de specificaties voor CU kunnen vallen, zelfs wanneer wordt voldaan aan de eisen voor gewichtsvariatie. De kans hierop lijkt toe te nemen bij laaggedoseerde capsules. Markman et al. beoordeelden bereide simvastatinecapsules 40 mg van 18 verschillende apotheken. In 22% van de gevallen vielen de capsules buiten de specificaties voor gewichtsvariatie, maar een nog groter percentage voldeed niet aan de specificaties voor CU: 72% [47]. In een andere studie met simvastatinecapsules 20 mg voldeed 37% van de capsules niet aan de criteria voor CU [48]. Colucci et al. stelden vast dat captoprilcapsules met een microdosis van 1 mg allemaal binnen de aanvaardbare grenzen voor gewichtsvariatie in de USP vielen, maar dat de aan de patiënten toegediende dosis met maar liefst 25% kon variëren wanneer het gehalte werd geanalyseerd [49]. Raffl publiceerde een studie waarbij capsules van 0,1 mg of 1 mg met natriumchloride als model-API werden beoordeeld. Alle monsters voldeden aan de vereisten in de USP voor gewichtsvariatie, maar 46% van de capsules van 1 mg en 64% van de capsules van 0,1 mg voldeden niet aan de criteria zoals gesteld voor CU [50]. Neumann et al. verzamelde in Duitsland steekproefsgewijs handmatig bereide hydrocortisoncapsules voor kinderen met congenitale bijnierhyperplasie. Na HPLC-analyse van 56 verschillende batches met in totaal 1125 capsules, bleek dat 21,4% niet voldeed aan de specificaties voor gewicht en/of gehalte [51]. In een andere studie werden bij acht apotheken handmatig bereide veterinaire trilostaancapsules gekocht van 15, 45 of 100 mg, waarvan vervolgens het gehalte werd vastgesteld. In totaal viel 38% van de handmatig bereide partijen onder de aanvaardingscriteria voor het gehalte [52]. Morita et al. analyseerden capsules met de schildklierhormonen levothyroxine (T4) en liothyronine (T3) van vijf verschillende apothekers. Daaruit bleek dat 40% tot 100% van de geanalyseerde capsules buiten de specificaties voor CU vielen [53]. Op basis van bovenstaande literatuur zou het daarom interessant zijn om in een vervolgstudie handmatig bereide, laaggedoseerde capsules direct te vergelijken met in SyrSpend SF bereide suspensies met dezelfde API.
Conclusie
Er is nog altijd een duidelijke behoefte aan geneesmiddelen op maat voor kinderen en ouderen bij wie de dosis moet worden aangepast of die moeite hebben met slikken. Gewoonlijk hebben apothekers de keus tussen handmatig bereide capsules en orale vloeistoffen. Uit dit onderzoek blijkt dat alle 104 verschillende onderzochte formuleringen (89 unieke API’s, 6414 analysepunten) ruimschoots voldoen aan de eisen zoals gesteld door de BP-monografie Unlicensed Medicines: Oral Suspensions - Homogeneity of Suspension.
Verantwoording
Het houdbaarheidsonderzoek waaruit de data is gegenereerd, is gefinancierd door Fagron Nederland B.V. De auteurs zijn in functie bij Fagron Nederland B.V.
Dit artikel is een bewerkte vertaling van: Dijkers E, Polonini H, Ferreira AO. Always the Right Dose? Content Uniformity in Over 100 Different Formulations Tested. Int J Pharm Compd. 2020 Sep-Oct;24(5):408-412.
Literatuur
1. Klotz U. Pharmacokinetics and drug metabolism in the elderly. Drug Metab Rev. 2009;41(2):67–76.
2. Ivanovska V, Rademaker CM, van Dijk L, Mantel-Teeuwisse AK. Pediatric drug formulations: a review of challenges and progress. Pediatrics. 2014 Aug;134(2):361–72.
3. European Medicines Agency. Committee for Medicinal Products for Human use (CHMP) 2005. Reflection Paper: Formulations of choice for the paediatric population [Internet]. Document EMEA/CHMP/PEG/194810/2005. [Geraadpleegd 2020 July 17]. Formulations of choice for the paediatric population | European Medicines Agency (europa.eu)
4. Kearns GL, Abdel-Rahman SM, Alander SW, Blowey DL, Leeder JS, Kauffman RE. Developmental pharmacology--drug disposition, action, and therapy in infants and children. N Engl J Med. 2003 Sep;349(12):1157–67.
5. Schirm E, Tobi H, De Vries TW, Choonara I, De Jong-van den Berg LT. Lack of appropriate formulations of medicines for children in the community. Acta Paediatr. 2003 Dec;92(12):1486–9.
6. Gosa M, Schooling T, Coleman J. Thickened liquids as a treatment for children with dysphagia and associated adverse effects: a systematic review. Infant, Child & Adolescent Nutrition. 2011;3(6):344–50.
7. Glass BD, Haywood A. Stability considerations in liquid dosage forms extemporaneously prepared from commercially available products. J Pharm Pharm Sci. 2006;9(3):398–426.
8. Haywood A, Glass BD. Liquid dosage forms extemporaneously prepared from commercially available products – considering new evidence on stability. J Pharm Pharm Sci. 2013;16(3):441–55.
9. Lein A, Ng SW. Oral liquids. In: Bouwman-Boer Y, Fenton-May V, Le Brun P, editors. Practical Pharmaceutics. An international guideline for the preparation, care and use of medicinal products. Switzerland: KNMP and Springer International Publishing; 2015:77–97.
10. Council of Europe. Convention of a European Pharmacopoeia. European Pharmacopoeia. Eighth Edition. Strasbourg, Germany: Druckerei C. H. Beck; 2013.
11. United States Pharmacopeial Convention, Inc. United States Pharmacopeia–National Formulary. Rockville, MD: United States Pharmacopeial Convention, Inc.; Current Edition.
12. British Pharmacopoeia Commission Office. British Pharmacopoeia. Unlicensed Medicines 2015. London, UK: The Stationery Office; 2014.
13. Visser JC, Ten Seldam IE, van der Linden IJ, et al. Comparison of rheological and sedimentation behavior of commercially available suspending vehicles for oral pharmaceutical preparations. Int J Pharm Comp. 2018 May-Jun;22(3):247–251.
14. Dijkers E, Nanhekhan V, Thorissen A, Polonini H. Suspensions as a valuable alternative to extemporaneously compounded capsules. Int J Pharm Comp. 2017 Mar-Apr;21(2):171–175.
15. Geiger CM, Sorenson B, Whaley P. Stability Assessment of 10 active pharmaceutical ingredients compounded in SyrSpend SF. Int J Pharm Comp. 2015 Sep-Oct;19(5):420–427.
16. Ferreira AO, Polonini HC, Silva SL, Patrício FB, Brandão MAF, Raposo NRB. Feasibility of amlodipine besylate, chloroquine phosphate, dapsone, phenytoin, pyridoxine hydrochloride, sulfadiazine, sulfasalazine, tetracycline hydrochloride, trimethoprim and zonisamide in SyrSpend® SF PH4 oral suspensions. J Pharm Biomed Anal. 2016 Jan;118:105–112.
17. Polonini HC, Loures S, Lima LC, Ferreira AO, Brandão MA. Stability of atenolol, clonazepam, dexamethasone, diclofenac sodium, diltiazem, enalapril maleate, ketoprofen, lamotrigine, penicillamine-d, and thiamine in SyrSpend SF PH4 oral suspensions. Int J Pharm Comp. 2016 Mar-Apr;20(2):167–74.
18. Geiger CM, Sorenson B, Whaley PA. Stability of captopril in SyrSpend SF. Int J Pharm Comp. 2013 Jul-Aug;17(4):336–8.
19. Polonini HC, Silva SL, Cunha CN, Brandão MA, Ferreira AO. Compatibility of cholecalciferol, haloperidol, imipramine hydrochloride, levodopa/carbidopa, lorazepam, minocycline hydrochloride, tacrolimus monohydrate, terbinafine, tramadol hydrochloride and valsartan in SyrSpend SF PH4 oral suspensions. Pharmazie. 2016 Apr;71(4):185–91.
20. Sorenson B, Voudrie MA 2nd, Gehrig D. Stability of gabapentin in SyrSpend SF. Int J Pharm Comp. 2012 Jul-Aug;16(4):347–9.
21. Vu NT, Aloumanis V, Ben M, et al. Stability of metronidazole benzoate in SyrSpend SF One-step Suspension System. Int J Pharm Comp. 2008 Nov-Dec;12(6):558–564.
22. Geiger CM, Sorenson B, Whaley PA. Stability of midazolam in SyrSpend SF and SyrSpend SF cherry. Int J Pharm Comp. 2013 Jul-Aug;17(4):344–6.
23. Whaley PA, Voudrie MA 2nd, Sorenson B. Stability of omeprazole in SyrSpend SF Alka (reconstituted). Int J Pharm Comp. 2012 Mar-Apr;16(2):164–6.
24. Voudrie li MA, Allen DB. Stability of oseltamivir phosphate in SyrSpend SF, Cherry Syrup, and SyrSpend SF (For Reconstitution). Int J Pharm Comp. 2010 Jan-Feb;14(1):82–6.
25. Geiger CM, Voudrie MA 2nd, Sorenson B. Stability of propranolol hydrochloride in SyrSpend SF. Int J Pharm Comp. 2012 Nov-Dec;16(6):513–5.
26. Sorenson B, Whaley P. Stability of rifampin in SyrSpend SF. Int J Pharm Comp. 2013 Mar-Apr;17(2):162–4.
27. Geiger CM, Voudrie MA 2nd, Sorenson B. Stability of ursodiol in SyrSpend SF Cherry flavored. Int J Pharm Comp. 2012 Nov-Dec;16(6):510–2.
28. Whaley PA, Voudrie MA 2nd. Stability of vancomycin in SyrSpend SF. Int J Pharm Comp. 2012 Mar-Apr;16(2):167–9.
29. Voudrie MA, Alexander B, Allen DB. Stability of Verapamil Hydrochloride in SyrSpend SF Compared to Sorbitol Containing Syrup and Suspending Vehicles. Int J Pharm Comp. 2011 May-Jun;15(3):255–8.
30. Polonini HC, Loures S, de Araujo ED, Brandão MA, Ferreira AO. Stability of Allopurinol, Amitriptyline Hydrochloride, Carbamazepine, Domperidone, Isoniazid, Ketoconazole, Lisinopril, Naproxen, Paracetamol (Acetaminophen), and Sertraline Hydrochloride in SyrSpend SF PH4 Oral Suspensions. Int J Pharm Comp. 2016 Sep-Oct;20(5):426–434.
31. Polonini HC, Silva SL, de Almeida TR, Brandão MAF, Ferreira AO. Compatibility of caffeine, carvedilol, clomipramine hydrochloride, folic acid, hydrochlorothiazide, loperamide hydrochloride, methotrexate, nadolol, naltrexone hydrochloride and pentoxifylline in SyrSpend SF PH4 oral suspensions. Eur J Hosp Pharm. 2016 Nov;23(6):352–358.
32. Polonini HC, Silva SL, Loures S, et al. Compatibility of proton pump inhibitors in a preservative-free suspending vehicle. Eur J Hosp Pharm. 2018 May;25(3):150–156.
33. Dijkers E, Nanhekhan V, Thorissen A. Updated Stability Data for Midazolam, Oseltamivir Phosphate, and Propranolol Hydrochloride in SyrSpend SF and Minoxidil in Espumil. Int J Pharm Comp. 2017 May-Jun;2(3):240–241.
34. Ferreira AO, Polonini HC, Loures da Silva S, et al. Stability of Alprazolam, Atropine Sulfate, Glutamine, Levofloxacin, Metoprolol Tartrate, Nitrofurantoin, Ondansetron Hydrochloride, Oxandrolone, Pregabaline, and Riboflavin in SyrSpend SF PH4 Oral Suspensions. Int J Pharm Comp. 2017 May-Jun;21(3):255–263.
35. Ferreira AO, Polonini HC, Loures da Silva S, et al. Stability of Acetazolamide, Baclofen, Dipyridamole, Mebevarine Hydrochloride, Propylthiouracil, Quinidine Sulfate, and Topiramate Oral Suspensions in SyrSpend SF PH4. Int J Pharm Comp. 2017 Jul-Aug; 21(4):339–346.
36. Uriel M, Gómez-Rincón C, Marro D. Stability of regularly prescribed oral liquids formulated with SyrSpend® SF. Pharmazie. 2018 Apr;73(4):196–201.
37. ICH Q2(R1) Validation of Analytical Procedures: Text and Methodology. [Internet.] International Council for Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use, 2005 [geraadpleegd 2020 Jul 20] ICH Q2(R1) Validation of Analytical Procedures: Text and Methodology - ECA Academy (gmp-compliance.org)
38. Allen Jr LV, Compounding, Stability and beyond-use dates. Minneapolis: Paddock Laboratories. Geraadpleegd 2007 Feb 05.
39. Allen LV. The art, science, and technology of pharmaceutical compounding. Washington DC: American Pharmaceutical Association; 2002:493.
40. Cairns, D. Essentials of Pharmaceutical Chemistry. 2nd ed. London: Pharmaceutical Press; 2003:179-l99.
41. Connors KA, Amidon GL, Stella VJ. Chemical stability of pharmaceuticals: a handbook for pharmacists. John Wiley & Sons; 1986.
42. Barbosa FS, Pezzi LC, Sorrentino J, et al. pH Effect on Stability and Kinetics Degradation of Nitazoxanide in Solution. Drug Anal Res. 2020;4(1):12-17.
43. Ferreira AO, Fernandes MA, Polonini HC. Guia Prático da Farmácia Magistral. 5th ed. Juiz de Fora: Pharmabooks; 2018.
44. Gokani RH, Desai KN. Stability Study: Regulatory Requirement. International Journal of Advances in Pharmaceutical Analysis. 2012;2(4):73-78.
45. Parrish RH 2nd. Current trends and emerging priorities in compounded preparations for children. Int J Pharm Comp. 2018 Sep-Oct; 22(5):358–366.
46. Engels MJ, Ciarkowski SL, Rood J, et al. Standardization of compounded oral liquids for pediatric patients in Michigan. Am J Health Syst Pharm. 2016 Jul 1;73(13):981–90.
47. Markman BE, Rosa PC, Koschtschak MR. Assessment of the quality of simvastatin capsules from compounding pharmacies. Rev Saude Publica. 2010 Dec;44(6):1055–62.
48. Marques-Marinho FD, da Costa Zanon JC, Sakurai E, Reis IA, Lima AA, Vianna-Soares CD. Quality evaluation of simvastatin compounded capsules. Braz J Pharm Sci. 2011;47(3):495–502.
49. Colucci RD, Scavone JM, Auty R, Glassner-Cohen L. Quality control of extemporaneously prepared microdose captopril capsules: Weight variation versus content uniformity. Int J Clin Pharmacol Ther. 1994 Jan;32(1):24–5.
50. Raffl M. Quality in pharmaceutical compounding for paediatric patients. EJHP. 2012;19(2):100.
51. Neumann U, Burau D, Spielmann S, et al. Quality of compounded hydrocortisone capsules used in the treatment of children. Eur J Endocrinol. 2017 Aug;177(2):239–242.
52. Cook AK, Nieuwoudt CD, Longhofer SL. Pharmaceutical evaluation of compounded trilostane products. J Am Anim Hosp Assoc. 2012 Jul-Aug;48(4):228–33.
53. Morita MLM, Baldin R, Farias N. Avaliação da qualidade da informação nas requisições e condições das amostras biológicas nos Laboratórios de Saúde Pública Lapa e Ipiranga do município de São Paulo. BEPA, Bol. epidemiol. paul. 2010;7(79):12–22.
Referentie
Citeer als: Dijkers E, Polonini H, Ferreira AO. Doseerhomogeniteit van meer dan honderd SyrSpend SF suspensies onderzocht na bewaren. Nederlands Platform voor Farmaceutisch Onderzoek. 2022;7:a1757.
DOI
https://www.knmp.nl/resolveuid/0b9a8981cbfb423ba5a211a606eff238Open access

Reactie toevoegen