Convulsiedrempelverlaging door antibiotica: contra-indicatiemelding epilepsie alleen voor cefepim en imipenem/cilastatine
- Rubriek: Overzichtsartikel
- Identificatie: 2025;10:e1798
Kernpunten
- Voor alle betalactam-antibiotica en chinolonen werd voorheen een contra-indicatiemelding getoond bij patiënten die bekend zijn met epilepsie.
- Klinische studies beschrijven een verhoogd risico op epileptische insulten voor de antibiotica cefepim en imipenem/cilastatine.
- Bij patiënten die bekend zijn met epilepsie moet wordenoverwogen cefepim en imipenem/cilastatine te vervangen door een alternatief antibioticum. We adviseren om alleen voor deze antibiotica een contra-indicatiemelding te tonen.
Abstract
Lowering of the convulsion threshold by antibiotics: contra-indication alert in epilepsy patients only for cefepime and imipenem/cilastatin
Beta-lactam antibiotics and quinolones are associated with a lower seizure threshold, due to antagonism of the gamma-aminobutyric acid (GABA) receptor. When these antibiotics are prescribed for patients known to have epilepsy, a medication surveillance alert was shown. Based on a literature review, we assessed whether this alert is clinically relevant. For most antibiotics, the occurrence of epileptic seizures is only described in case reports. In most cases, there were additional risk factors, such as liver and kidney function disorders. For cefepime, ceftazidime, ciprofloxacin, and the carbapenems, studies were found that compared the incidence of epileptic seizures between two or more antibiotics. Higher incidences were only found for cefepime and imipenem/cilastatin. In patients known to have epilepsy,preference is given to the antibiotic of first choice, with the exception of cefepime and imipenem/cilastatin. These antibiotics are preferably avoided in patients known to have epilepsy.
Casus
Een 34-jarige vrouw bekend met epilepsie is opgenomen op de intensive care unit (ICU) in verband met een status epilepticus. Ze wordt hiervoor behandeld met midazolam en fenytoïne, waarop verbetering optreedt. In verband met verdenking op aspiratiepneumonie wordt gestart met ceftriaxon 2000 mg elke 24 uur. Het voorschrijfsysteem geeft een medicatiebewakingsmelding van het type contra-indicatie, aangezien betalactam-antibiotica en chinolonen de convulsiedrempel kunnen verlagen, met name bij hoge intraveneuze doseringen. Kan ceftriaxon veilig worden voorgeschreven, of is een alternatief antibioticum meer geschikt?
Inleiding
Toepassing van betalactam-antibiotica en chinolonen bij patiënten met epilepsie in de voorgeschiedenis roept in de praktijk vragen op, omdat deze antibiotica de convulsiedrempel kunnen verlagen. Een infectieus beeld kan dermate ernstig zijn dat snelle actie noodzakelijk is en er niet voldoende tijd is voor uitgebreide analyse. Epileptische aanvallen kunnen door een variëteit van factoren worden uitgelokt, waaronder een infectieuze meningitis of encefalitis, waarbij een snelle en adequate antibiotische behandeling geassocieerd is met een betere uitkomst [1]. Het optreden van epileptische aanvallen heeft veel impact op patiënten, ook bij patiënten bekend met epilepsie die al langere tijd aanvalsvrij waren.
De voorschrijfsystemen in Nederland die gebaseerd zijn op informatie uit de G-Standaard van de KNMP en de Pharmabase van Stichting Health Base, bewaakten op de contra-indicatie epilepsie voor chinolonen en parenteraal toegediende betalactam-antibiotica. Ten tijde van het schrijven van dit artikel was de vraag of deze contra-indicatie klinisch relevant is. En kunnen we op basis van de literatuur een meer gericht advies geven? Om antwoorden op deze vragen te kunnen geven is een literatuuronderzoek uitgevoerd naar de associatie tussen het gebruik van betalactam-antibiotica en chinolonen en het optreden van epileptische aanvallen.
Achtergrond
In verschillende dierstudies is een proconvulsief effect aangetoond van betalactam-antibiotica [2]. De betalactamring vertoont structurele gelijkenis met de neurotransmitter gamma-aminoboterzuur (GABA). Bij penetratie in de cerebrospinale vloeistof kan de betalactamring binden aan de GABA-receptoren en de binding van GABA aan deze receptoren antagoneren. Het gevolg is minder inhibitie van de neuronale activiteit in het centraal zenuwstelsel [3-5]. Penetratie van betalactam-antibiotica in de cerebrospinale vloeistof vindt met name plaats bij supratherapeutische doseringen, al dan niet in combinatie met nierinsufficiëntie [6]. Daarnaast kunnen aandoeningen waarbij de bloed-hersenbarrière betrokken is, zoals meningitis, leiden tot een betere penetratie van antibiotica en hogere spiegels in de cerebrospinale vloeistof [6,7]. Naast betalactam-antibiotica hebben ook chinolonen affiniteit voor de GABA-receptor. In proefdieronderzoek hangt de competitieve remming van de GABA-receptor door chinolonen samen met een pro-epileptogeen effect [8]. Latere onderzoeken hebben ook betrokkenheid van de N-methyl-D-aspartaat (NMDA)-receptoren gesuggereerd [9].
Penicillines
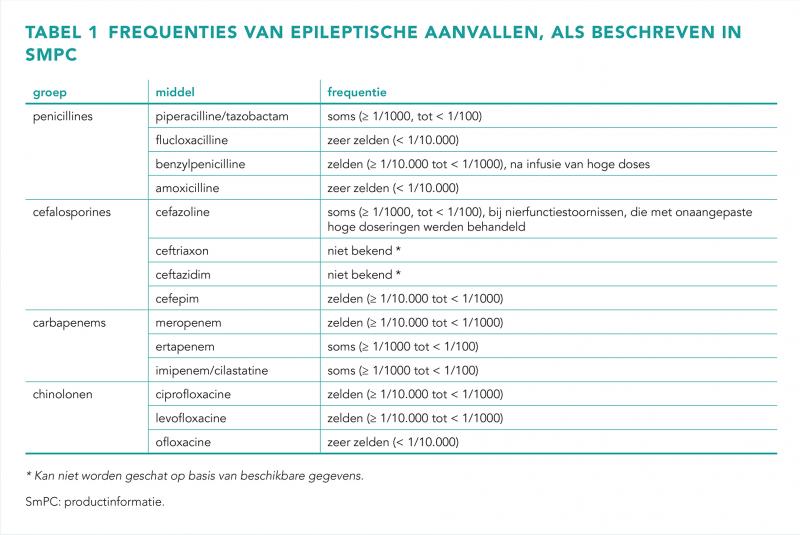
In de literatuur is een beperkt aantal case reports verschenen van patiënten die epileptische aanvallen ontwikkelden na toediening van benzylpenicilline, piperacilline/tazobactam en amoxicilline [6,10,11]. Bij alle patiënten was de dosering te hoog, de nierfunctie (sterk) verminderd, of sprake van uitlokkende factoren die het risico op epileptische aanvallen verhoogden, zoals encefalopathie. Dit correleert ook met de productinformatie (SmPC) van de penicillines voor intraveneuze toediening. De frequentie van epileptische aanvallen verschilt van ‘soms’ (1:100-1:1000) bij piperacilline/tazobactam, tot ‘zelden’ (1:1000-1:10.000) bij benzylpenicilline en ‘zeer zelden’ (< 1:10.000) bij flucloxacilline en amoxicilline, met nadruk op een hoger risico bij nierfunctiestoornis in combinatie met hoge doseringen (tabel 1).
Cefalosporines
Ook voor de cefalosporines is de onderbouwing voor het optreden van epileptische aanvallen veelal beperkt tot beschrijvingen in case reports. Zo zijn er case reports voor ceftriaxon (twee), cefazoline (drie), ceftazidim (zeven) en cefepim (elf) [12-16]. In de meeste gevallen was sprake van een nierfunctiestoornis en was de dosis hier niet voor gecorrigeerd [17,18]. Cefepim, een vierde generatie cefalosporine, lijkt het meest epileptogeen. In een retrospectieve studie van 100 patiënten opgenomen op een ICU en behandeld met cefepim, werd het optreden van neurotoxiciteit onderzocht. In 11 patiënten (11%) werden myoclonieën gezien en in 1 patiënt (1%) een non-convulsieve status epilepticus [19]. Chronische nierschade en het niet aanpassen van de dosis aan de nierfunctie waren risicofactoren voor het optreden van neurotoxiciteit. In een andere retrospectieve studie werd de incidentie van epileptische aanvallen vergeleken tussen 183 patiënten die werden behandeld met cefepim en 745 patiënten die werden behandeld met meropenem. De incidentie in de cefepim-groep was 2,7% versus 0,54% in de meropenem-groep (P < 0,01) [20]. Alle patiënten in de cefepim-groep bij wie epileptische aanvallen optraden, hadden een goede nierfunctie, maar waren bekend met een neurologische aandoening.
In een kleine gerandomiseerde studie die cefepim vergeleek met cefotaxim bij kinderen met bacteriële meningitis, werd geen verschil gevonden in het optreden van epileptische aanvallen. In de groep die met cefepim werd behandeld, kwamen bij 6 van de 43 kinderen epileptische aanvallen voor, vergeleken met 6 van de 47 kinderen die met cefotaxim werden behandeld [21].
Het is mogelijk dat er sprake is van bias bij de waarneming dat cefepim meer epileptogeen is dan andere cefalosporines. Cefepim is meer recent op de markt gekomen, waardoor de aandacht voor en rapportage van deze bijwerking mogelijk beter waren.
Carbapenems
Carbapenems penetreren goed door de bloed-hersenbarrière en zijn daarom geschikt voor het behandelen van infecties in het centraal zenuwstelsel. Er is gesuggereerd dat carbapenems daardoor mogelijk meer epileptogeen zijn dan andere antibiotica [22].
Twee reviews hebben de incidentie van epileptische aanvallen onderzocht in fase III-studies die meropenem vergeleken met andere antibiotica. In een studie die de bijwerkingen in 25 fase III-studies beschreef, was de incidentie van epileptische aanvallen bij meropenem-gebruikers 0,38% (15 van 3911, waarvan 6 met bekende neurologische aandoeningen en 6 met meningitis) en bij cefalosporine-gebruikers 0,37% (7 van 1891, waarvan 2 met bekende neurologische aandoeningen en 3 met meningitis) [23]. Ook patiënten met meningitis, die door dit type infectie een verhoogd risico hebben op epileptische aanvallen, verdroegen meropenem goed. In een andere studie werd de incidentie van geneesmiddelgerelateerde epileptische aanvallen onderzocht bij ouderen en/of patiënten met nierfunctiestoornissen in 26 fase III-studies met meropenem [24]. Studies naar meningitis werden geëxcludeerd. Zowel in de groep die behandeld werd met meropenem (4 van 2790) als in de groep die behandeld werd met cefalosporines (1 van 977) werd een incidentie van 0,1% gevonden. In beide studies werd het verschil niet getoetst op statistische significantie. In een meer recente meta-analyse van 41 studies die meropenem vergeleken met niet-carbapenems werd geen statistisch significant verschil in epileptische aanvallen gezien in risico (risicoverschil 0,02%, 95%-betrouwbaarheidsinterval [BI] −0,04; 0,05) [25].
Met doripenem en ertapenem is minder ervaring opgedaan en is het risico op epileptische aanvallen minder goed onderzocht [25]. In dierstudies heeft doripenem minder epileptische activiteit laten zien dan meropenem [26]. In een meta-analyse van 19 studies die ertapenem vergeleken met niet-carbapenems en 2 studies die doripenem vergeleken met niet-carbapenems, werd voor beide carbapenems geen statistisch significant risicoverschil in incidentie van epileptische aanvallen gevonden (ertapenem 0,02% [95%-BI −0,02; 0,03%] en doripenem −0,7% [95%-BI −1,8; 0,4%]) [25].
Studies suggereren dat de incidentie van epileptische aanvallen bij behandeling met imipenem/cilastatine hoger is dan bij andere carbapenems [22,27]. In dierstudies is een hogere affiniteit van imipenem/cilastatine voor de GABA-A-receptoren aangetoond en daarnaast zou de penetratie van imipenem/cilastatine in de cerebrospinale vloeistof hoger zijn ten opzichte van andere carbapenems [26]. Proefdieronderzoek in muizen liet zien dat cilastatine niet epileptogeen is, waardoor het effect toe te schrijven is aan imipenem [28]. Deze theoretische achtergrond komt overeen met resultaten in de literatuur. Een meta-analyse laat zien dat het risico op epileptische aanvallen bij imipenem/cilastatine hoger is dan bij behandeling met andere carbapenems [25]. Het risicoverschil in deze meta-analyse was in de 107 geïncludeerde studies 0,4% (95%-BI 0,2; 0,7) ten opzichte van niet-carbapenems. In de studies waarbij hogere doseringen werden onderzocht (> 2 gram per dag) liep het risicoverschil op naar 0,8% (95%-BI 0,4; 1,3). Opvallend was dat in de 21 studies die meropenem vergeleken met imipenem, geen verschil werd gevonden (risicoverschil 0,1% (95%-BI −0,3;0,6). Een kanttekening is dat in de meta-analyse meer onderzoeken met imipenem/cilastatine zijn geïncludeerd dan met meropenem, en dat in de meeste studies met meropenem patiënten met een voorgeschiedenis van epileptische aanvallen werden geëxcludeerd.
Naast het effect van carbapenems op de GABA-A-receptor, hebben carbapenems een interactie met valproïnezuur. Eerder is hier al aandacht aan besteed in het NPFO [29]. De combinatie van valproïnezuur met carbapenems leidt tot een daling van de valproïnezuurspiegels en een toename van de aanvalsfrequentie [30,31]. Na start van toediening van ertapenem, imipenem/cilastatine en meropenem daalde de valproïnezuurspiegel met respectievelijk 72%, 42% en 67% [32]. Om deze reden wordt de combinatie van valproïnezuur met carbapenems afgeraden. In de literatuur worden verschillende mechanismen genoemd die hieraan ten grondslag kunnen liggen. Mogelijk wordt de metabolisering van valproïnezuur in glucuronidylvalproïnezuur versneld en de terugvorming van valproïnezuur uit glucuronidylvalproïnezuur geremd [33,34]. Andere mogelijke verklaringen zijn dat carbapenems een effect hebben op het opnameproces in de darm en dat valproïnezuur ophoopt in erytrocyten [35,36].
Chinolonen
In twee gerandomiseerde klinische studies werd het optreden van epileptische aanvallen onderzocht bij gebruik van ciprofloxacine. In de eerste studie kregen 2 van de 61 patiënten in de ciprofloxacine-groep epileptische aanvallen, tegenover 0 van de 37 patiënten in de ceftazidim-groep [37]. Dit verschil werd niet significant getoetst. In de tweede studie kregen 3 van de 202 patiënten in de ciprofloxacine-groep epileptische aanvallen, tegenover 11 van de 200 in de imipenem/cilastatine-groep. Dit verschil was statistisch significant (P = 0,028) [38]. Twee van de drie epileptische aanvallen in de ciprofloxacine-groep deden zich voor een week na het stoppen met de therapie. Zoals eerder beschreven, wordt voor imipenem/cilastatine een hogere incidentie van optreden van epileptische aanvallen vermoed. In een systematische review werd de incidentie van epileptische aanvallen door chinolonen bij kinderen onderzocht [39]. In de 140 geïncludeerde studies werden zelden epileptische aanvallen gezien, namelijk bij 6 van de 21.884 kinderen die werden behandeld met fluorchinolonen (incidentie 0,03%). Bij kinderen met aandoeningen van het centraal zenuwstelsel was de incidentie 2 van 317 kinderen, tegenover 4 van 21.567 bij kinderen zonder aandoeningen van het centraal zenuwstelsel. In een publicatie van Lareb worden zeven casussen beschreven, waarbij epileptische aanvallen ontstonden bij patiënten zonder belaste familieanamnese. Deze ontstonden in de meeste gevallen binnen 48 uur na start van orale therapie met het chinolon [40]. In de literatuur zijn case reports verschenen van epileptische aanvallen bij gebruik van ciprofloxacine (vier case reports), levofloxacine (zes) en ofloxacine (één) [7,12,41,42]. In een groot deel van deze case reports was sprake van aandoeningen van het centraal zenuwstelsel, te hoge doseringen in relatie tot lever- of nierfunctiestoornissen, waardoor de blootstelling aan het chinolon hoger was, of combinaties van geneesmiddelen die de convulsiedrempel verlagen.
Beschouwing
Het optreden van epileptische aanvallen is voor de meeste betalactam-antibiotica en chinolonen alleen beschreven in case reports. In veel gevallen waren er aanvullende risicofactoren, zoals aandoeningen waarbij de bloed-hersenbarrière is aangedaan, hoge doseringen en lever- of nierfunctiestoornissen. Ook wordt het optreden van epileptische aanvallen in de SmPC’s genoemd. Voor cefepim en imipenem/cilastatine zijn in de literatuur aanwijzingen dat deze middelen een hoger risico hebben op epileptische aanvallen ten opzichte van andere antibiotica. Voor meropenem wordt geen verhoogd risico gevonden ten opzichte van de niet-carbapenems, maar in de onderlinge vergelijking met imipenem/cilastatine wordt geen verschil gevonden. Daarnaast werden in de meeste studies met meropenem patiënten met epilepsie geëxcludeerd. Meropenem en imipenem/cilastatine behoren echter tot de reserve-antibiotica, waarbij een alternatief antibioticum in veel gevallen een inferieure behandeling zal zijn. Omdat de incidentie van epileptische aanvallen laag is en alleen voor imipenem/cilastatine een verhoogd risico is gevonden, adviseren we om alleen imipenem/cilastatine te vermijden bij patiënten met epilepsie. Op basis van de SmPC worden ook hogere frequenties van epileptische aanvallen beschreven voor piperacilline/tazobactam en ertapenem, maar dit was niet te onderbouwen met de beschikbare literatuur. Een beperking hierbij is dat de meeste studies niet specifiek in epilepsiepatiënten zijn uitgevoerd en in sommige studies epilepsiepatiënten zelfs zijn uitgesloten. We adviseren daarom om voor cefepim en voor imipenem/cilastatine een contra-indicatiemelding te tonen bij patiënten met epilepsie in de voorgeschiedenis.
Conclusie
Bij de behandeling van infecties bij epilepsiepatiënten gaat de voorkeur uit naar het antibioticum van eerste keuze, met uitzondering van cefepim en imipenem/cilastatine. Terugblikkend op de casus van de 34-jarige patiënte, aan wie ceftriaxon werd voorgeschreven voor een aspiratiepneumonie, zou dit antibioticum op basis van de beschikbare literatuur veilig kunnen worden ingezet. Het tonen van een medicatiebewakingssignaal bij chinolonen en parenteraal toegediende betalactam-antibiotica bij patiënten die bekend zijn met epilepsie lijkt contraproductief, omdat het risico voor de meeste antibiotica niet klinisch relevant is. Dit kan leiden tot vertraging in het toedienen van de eerste dosis en/of tot de keuze van een antibioticum dat niet de eerste keuze is en mogelijk minder effectief kan zijn. Bij ernstige infecties heeft dit juist een negatief effect op de behandeluitkomsten.
De bevindingen zijn voorgelegd aan het Geneesmiddel Informatie Centrum van de KNMP en in samenwerking met Stichting Health Base is het medicatiebewakingssignaal in beide systemen herzien in lijn met onze adviezen.
Verantwoording
Geen belangenverstrengeling gemeld.
De auteurs danken de medewerkers van het Geneesmiddel Informatie Centrum van de KNMP voor hun waardevolle commentaar op een eerdere versie van dit artikel.
Literatuur
1. Proulx N, Fréchette D, Toye B, Chan J, Kravcik S. Delays in the administration of antibiotics are associated with mortality from adult acute bacterial meningitis. QJM. 2005 Apr;98(4):291-8.
2. Van Duijn H, Schwartzkroin PA, Prince DA. Action of penicillin on inhibitory processes in the cat's cortex. Brain Res. 1973 Apr 27;53(2):470-6.
3. Curtis DR, Game CJ, Johnston GA, McCulloch RM, MacLachlan RM. Convulsive action of penicillin. Brain Res. 1972 Aug 11;43(1):242-5.
4. Hori S, Kurioka S, Matsuda M, Shimada J. Inhibitory effect of cephalosporins on gamma-aminobutyric acid receptor binding in rat synaptic membranes. Antimicrob Agents Chemother. 1985 Apr;27(4):650-1.
5. Sugimoto M, Uchida I, Mashimo T, et al. Evidence for the involvement of GABA(A) receptor blockade in convulsions induced by cephalosporins. Neuropharmacology. 2003 Sep;45(3):304-14.
6. Sutter R, Rüegg S, Tschudin-Sutter S. Seizures as adverse events of antibiotic drugs: A systematic review. Neurology. 2015 Oct 13;85(15):1332-41.
7. Tomé AM, Filipe A. Quinolones: review of psychiatric and neurological adverse reactions. Drug Saf. 2011 Jun 1;34(6):465-88.
9. Akahane K, Kato M, Takayama S. Involvement of inhibitory and excitatory neurotransmitters in levofloxacin- and ciprofloxacin-induced convulsions in mice. Antimicrob Agents Chemother. 1993 Sep;37(9):1764-70.
10. Boston Collaborative Drug Surveillance Program. Drug-induced convulsions. Report from Boston Collaborative Drug Surveillance Program. Lancet. 1972 Sep 30;2(7779):677-9.
11. Weinstein L, Lerner PI, Chew WH. Clinical and bacteriologic studies of the effect of "massive" doses of penicillin G on infections caused by gram-negative bacilli. N Engl J Med. 1964 Sep 10;271:525-33.
12. Misra UK, Kalita J, Chandra S, Nair PP. Association of antibiotics with status epilepticus. Neurol Sci. 2013 Mar;34(3):327-31.
13. Kim A, Kim JE, Paek YM, et al. Cefepime- Induced Non-Convulsive Status Epilepticus (NCSE). J Epilepsy Res. 2013 Jun 30;3(1):39-41.
14. Thabet F, Al Maghrabi M, Al Barraq A, Tabarki B. Cefepime-induced nonconvulsive status epilepticus: case report and review. Neurocrit Care. 2009;10(3):347-51.
15. Martínez-Rodríguez JE, Barriga FJ, Santamaria J, et al. Nonconvulsive status epilepticus associated with cephalosporins in patients with renal failure. Am J Med. 2001 Aug;111(2):115-9.
16. Fernández-Torre JL, Martínez-Martínez M, González-Rato J, et al. Cephalosporin-induced nonconvulsive status epilepticus: clinical and electroencephalographic features. Epilepsia. 2005 Sep;46(9):1550-2.
17. Deshayes S, Coquerel A, Verdon R. Neurological Adverse Effects Attributable to β-Lactam Antibiotics: A Literature Review. Drug Saf. 2017 Dec;40(12):1171-1198.
18. Bechtel TP, Slaughter RL, Moore TD. Seizures associated with high cerebrospinal fluid concentrations of cefazolin. Am J Hosp Pharm. 1980 Feb;37(2):271-3.
19. Fugate JE, Kalimullah EA, Hocker SE, Clark SL, Wijdicks EFM, Rabinstein AA. Cefepime neurotoxicity in the intensive care unit: a cause of severe, underappreciated encephalopathy. Crit Care. 2013 Nov 7;17(6):R264.
20. Tanaka A, Takechi K, Watanabe S, Tanaka M, Suemaru K, Araki H. Comparison of the prevalence of convulsions associated with the use of cefepime and meropenem. Int J Clin Pharm. 2013 Oct;35(5):683-7.
21. Sáez-Llorens X, Castaño E, García R, et al. Prospective randomized comparison of cefepime and cefotaxime for treatment of bacterial meningitis in infants and children. Antimicrob Agents Chemother. 1995 Apr;39(4):937-40.
22. Miller AD, Ball AM, Bookstaver PB, Dornblaser EK, Bennett CL. Epileptogenic potential of carbapenem agents: mechanism of action, seizure rates, and clinical considerations. Pharmacotherapy. 2011 Apr;31(4):408-23.
23. Norrby SR, Newell PA, Faulkner KL, Lesky W. Safety profile of meropenem: international clinical experience based on the first 3125 patients treated with meropenem. J Antimicrob Chemother. 1995 Jul;36 Suppl A:207-23.
24. Cunha BA. Meropenem in elderly and renally impaired patients. Int J Antimicrob Agents. 1998 May;10(2):107-17.
25. Cannon JP, Lee TA, Clark NM, Setlak P, Grim SA. The risk of seizures among the carbapenems: a meta-analysis. J Antimicrob Chemother. 2014 Aug;69(8):2043-55.
26. Horiuchi M, Kimura M, Tokumura M, Hasebe N, Arai T, Abe K. Absence of convulsive liability of doripenem, a new carbapenem antibiotic, in comparison with beta-lactam antibiotics. Toxicology. 2006 May 1;222(1-2):114-24.
27. Calandra GB, Ricci FM, Wang C, Brown KR. The efficacy results and safety profile of imipenem/cilastatin from the clinical research trials. J Clin Pharmacol. 1988 Feb;28(2):120-7.
28. Williams PD, Bennett DB, Comereski CR. Animal model for evaluating the convulsive liability of beta-lactam antibiotics. Antimicrob Agents Chemother. 1988 May;32(5):758-60.
29. Derijks-Engwegen JYMN, Derijks LJJ. Interactie tussen valproïnezuur en meropenem: waarde van de vrije concentratie. Nederlands Platform voor Farmaceutisch Onderzoek. 2018;3:a1665.
30. Huang CR, Lin CH, Hsiao SC, et al. Drug interaction between valproic acid and carbapenems in patients with epileptic seizures. Kaohsiung J Med Sci. 2017;33(3):130-136.
31. Haroutiunian S, Ratz Y, Rabinovich B, Adam M, Hoffman A. Valproic acid plasma concentration decreases in a dose-independent manner following administration of meropenem: a retrospective study. J Clin Pharmacol. 2009 Nov;49(11):1363-9.
32. Wu CC, Pai TY, Hsiao FY, Shen LJ, Wu FL. The effect of different carbapenem antibiotics (ertapenem, imipenem/cilastatin, and meropenem) on serum valproic acid concentrations. Ther Drug Monit. 2016 Oct;38(5):587-92.
33. Mori H, Takahashi K, Mizutani T. Interaction between valproic acid and carbapenem antibiotics. Drug Metab Rev. 2007;39(4):647-57.
34. Nakajima Y, Mizobuchi M, Nakamura M, et al. Mechanism of the drug interaction between valproic acid and carbapenem antibiotics in monkeys and rats. Drug Metab. Dispos. 2004 Dec;32:1383–91.
35. Torii M, Takiguchi Y, Izumi M, Fukushima T, Yokota M. Carbapenem antibiotics inhibit valproic acid transport in caco-2 cell monolayers. Int J Pharm. 2002 Feb 21;233(1-2):253-6.
36. Omoda K, Murakami T, Yumoto R, et al. Increased erythrocyte distribution of valproic acid in pharmacokinetic interaction with carbapenem antibiotics in rat and human. J Pharm Sci. 2005 Aug;94(8):1685-93.
37. Fass RJ, Plouffe JF, Russell JA. Intravenous/oral ciprofloxacin versus ceftazidime in the treatment of serious infections. Am J Med. 1989 Nov 30;87(5A):164S-168S.
38. Fink MP, Snydman DR, Niederman MS, et al. Treatment of severe pneumonia in hospitalized patients: results of a multicenter, randomized, double-blind trial comparing intravenous ciprofloxacin with imipenem-cilastatin. The Severe Pneumonia Study Group. Antimicrob Agents Chemother. 1994 Mar;38(3):547-57.
39. Neame M, King C, Riordan A, et al. Seizures and quinolone antibiotics in children: a systematic review of adverse events. Eur J Hosp Pharm. 2020 Mar;27(2):60-64.
40. Lareb. Convulsies bij gebruik van ciprofloxacine en andere fluorchinolonen. Gebu. 2002;36(8):90-91.
41. Kuula LSM, Viljemaa KM, Backman JT, Blom M. Fluoroquinolone-related adverse events resulting in health service use and costs: A systematic review. PLoS One. 2019 Apr 26;14(4):e0216029.
42. Bellon A, Perez-Garcia G, Coverdale JH, Chacko RC. Seizures associated with levofloxacin: case presentation and literature review. Eur J Clin Pharmacol. 2009 Oct;65(10):959-62.
Referentie
Citeer als: Aarts J, der Nederlanden AM, Sturm TT, Engelsman J, Becker ML. Convulsiedrempelverlaging door antibiotica: contra-indicatiemelding epilepsie alleen voor cefepim en imipenem/cilastatine. Nederlands Platform voor Farmaceutisch Onderzoek. 2025;10:a1798.
DOI
https://www.knmp.nl/resolveuid/59b7f48eaf8e428b8810947466a5fb3bOpen access

Reactie toevoegen